Clear Sky Science · fr
Les canaux HCN révèlent une physiologie conservée et divergente chez les neurones pyramidaux supragranulaires des primates
Pourquoi les différences d’organisation cérébrale importent
Les humains pensent et agissent manifestement différemment des souris, mais les neuroscientifiques cherchent encore à comprendre ce que cela signifie pour les cellules nerveuses individuelles qui composent nos cerveaux. Cette étude se concentre sur un ensemble particulier de neurones dans les couches supérieures du cortex — des cellules qui contribuent à relier différentes zones cérébrales — et pose la question de savoir si une propriété électrique clé qui distingue les neurones humains de ceux des rongeurs est propre à l’homme ou partagée entre primates. La réponse éclaire la manière dont les cerveaux de primates traitent l’activité rythmique lente qui soutient la perception, la mémoire et l’attention.
Canaux spécifiques qui façonnent le rythme neuronal
Les neurones communiquent grâce à de faibles signaux électriques. Ces signaux sont fortement modulés par des pores dans la membrane cellulaire appelés canaux ioniques. Les auteurs se concentrent sur les canaux HCN, qui s’ouvrent discrètement lorsque le potentiel d’un neurone devient plus négatif puis le ramènent progressivement vers son niveau de repos. Ce courant autorégulateur rend les neurones les plus réactifs aux entrées dans les bandes lentes « delta » et « thêta » (environ 1–8 cycles par seconde), des fréquences courantes dans les ondes cérébrales pendant le sommeil, la navigation et l’attention soutenue. Des travaux antérieurs avaient montré que les neurones pyramidaux des couches supérieures humaines présentent des propriétés HCN particulièrement marquées par rapport aux souris, suggérant que ces canaux pourraient contribuer à ce qui rend le cortex humain singulier.
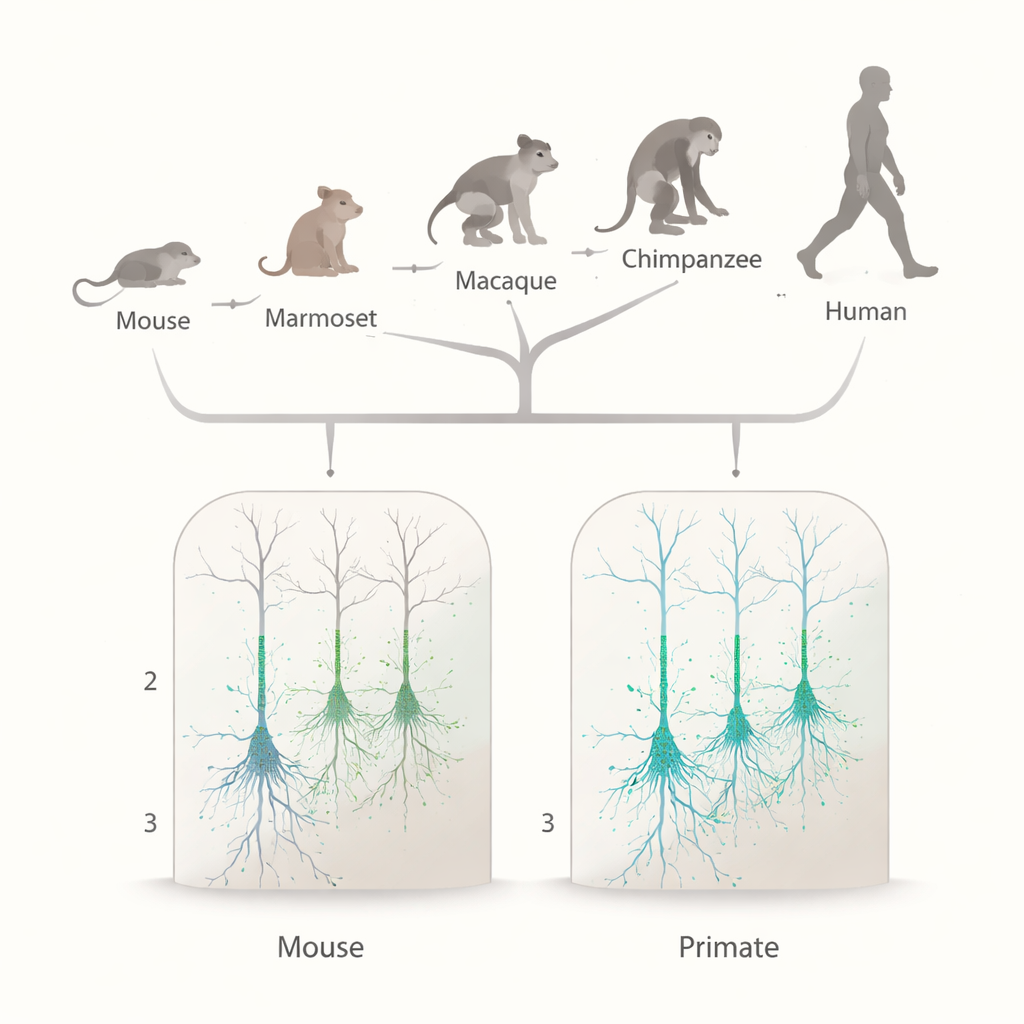
Recherche de la même signature électrique chez les primates
Pour déterminer si cet enrichissement en HCN est uniquement humain ou partagé par les primates, l’équipe a comparé l’activité génique et le comportement électrique des neurones de plusieurs espèces. À partir de jeux de données de séquençage ARN nucléaire unique, ils ont d’abord mesuré l’expression du gène HCN1 et d’une protéine auxiliaire appelée TRIP8b (codée par PEX5L) dans les neurones excitateurs des couches supérieures du cortex chez des singes du Nouveau Monde, des singes de l’Ancien Monde, des grands singes et des humains, et ont comparé ces résultats à des données de souris. Dans toutes les espèces de primates, HCN1 et TRIP8b étaient largement exprimés dans les neurones excitateurs des couches supérieures, à des niveaux similaires à une classe de neurones des couches profondes déjà connue pour dépendre fortement des canaux HCN. Chez la souris, en revanche, HCN1 était beaucoup moins fréquent dans ces cellules des couches supérieures. Cela suggère un schéma général aux primates plutôt qu’une particularité humaine.
Tester des neurones vivants de singes
Les auteurs ont ensuite obtenu des coupes cérébrales vivantes de deux espèces de macaques et de singes écureuils, et ont enregistré l’activité de plus de 500 neurones pyramidaux des couches supérieures dans les cortex temporal et moteur. Ils ont utilisé des stimuli de courant astucieux pour sonder si les cellules présentaient une « résonance membranaire » — une préférence pour des oscillations dans une bande de fréquence particulière — signature d’une conductance HCN active. De nombreux neurones des trois espèces de singes ont résonné au-dessus de 2 Hz, en particulier dans le cortex moteur, indiquant une forte implication des HCN. D’autres mesures, telles qu’un « sag » caractéristique du potentiel lors d’une injection de courant négatif et une coupure plus rapide du filtrage passe-bas, ont également corroboré une activité HCN répandue. Dans le cortex temporal du macaque à queue de cochon, les effets liés aux HCN s’intensifiaient pour les neurones situés plus profondément au sein des couches supérieures, reflétant des observations antérieures dans le gyrus temporal moyen humain.
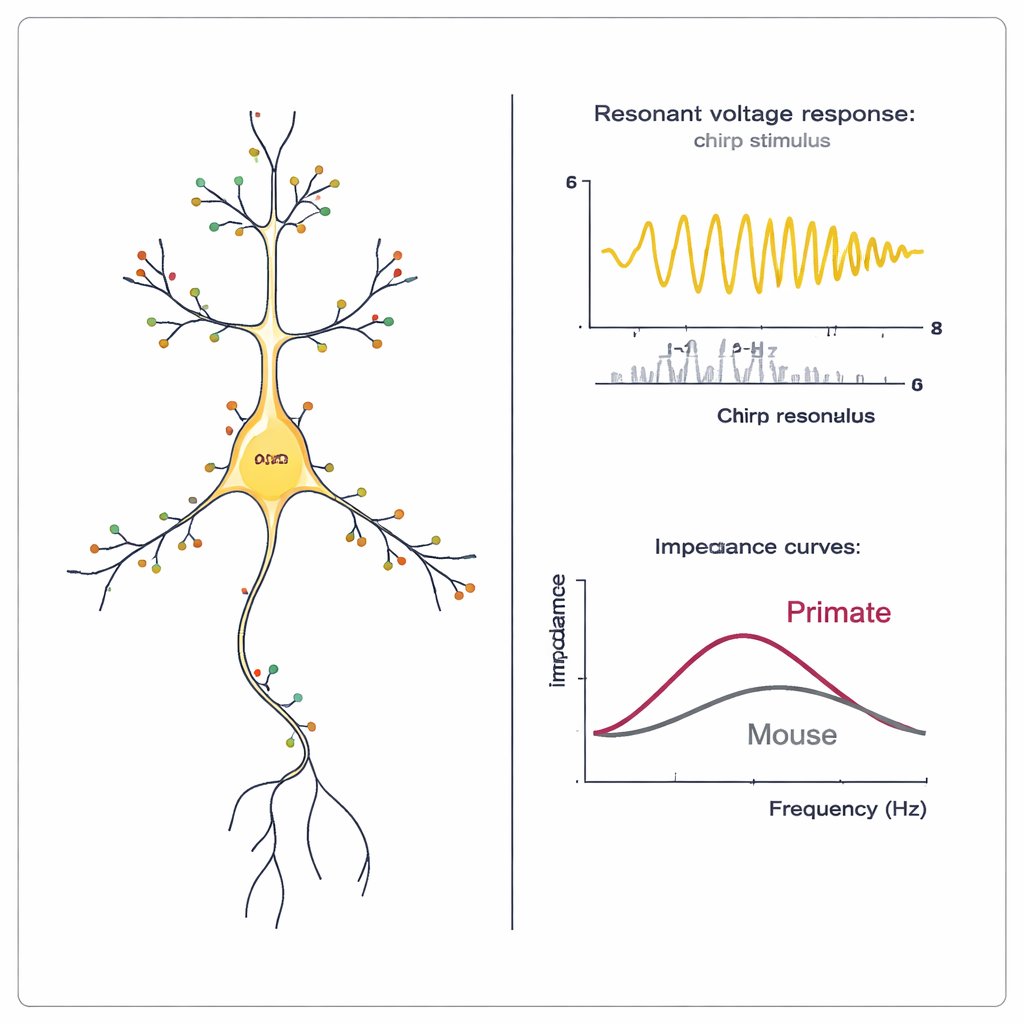
Bloquer les canaux et comparer humains et macaques
Pour confirmer que les canaux HCN sont bien la cause de ces effets, les chercheurs ont appliqué un bloqueur spécifique, le ZD7288, sur des tranches de cortex temporal de macaque. Lorsque les canaux HCN étaient bloqués, les neurones devenaient plus résistants électriquement, leur potentiel de repos se décalait vers des valeurs plus négatives, et à la fois le sag et la résonance disparaissaient essentiellement. L’amplitude du changement de résonance et de sag suivait l’évolution de la résistance d’entrée, ce qui implique que les neurones présentant les signatures HCN les plus marquées avaient aussi la conductance HCN la plus importante. Enfin, en combinant enregistrements électriques et expression génique des mêmes cellules via la méthode Patch-seq, l’équipe a pu aligner les neurones de macaque et d’humain sur des types transcriptomiques correspondants. Pour un grand type de couche supérieure (L2/3 IT_1), les propriétés liées aux HCN — y compris la résonance et le sag — augmentaient avec la profondeur depuis la surface cérébrale dans les deux espèces et corrélaient avec l’expression de HCN1. Fait intéressant, au sein de ce type cellulaire, les neurones de macaque présentaient un comportement dépendant des HCN encore plus marqué que leurs homologues humains, tandis qu’un second type de couche supérieure (L2/3 IT_3) montrait seulement de faibles différences entre espèces.
Ce que cela signifie pour le traitement de l’information par les cerveaux de primates
Globalement, l’étude montre que l’expression et la fonction renforcées des canaux HCN dans les neurones pyramidaux des couches supérieures sont une caractéristique conservée chez les primates, et non une adaptation uniquement humaine. Comparés aux rongeurs, les primates ont des couches corticales supérieures plus épaisses et des neurones aux dendrites plus longs et plus ramifiés. Une conductance HCN forte aide ces grandes cellules à intégrer les entrées de manière plus uniforme sur leur arborisation dendritique et à les accorder sur les rythmes lents delta/thêta qui dominent l’activité corticale des primates. De subtiles variations entre types cellulaires, zones cérébrales et espèces — comme les effets HCN particulièrement prononcés dans un type de neurone de macaque — peuvent fournir une flexibilité supplémentaire pour l’affinage de la cognition. Mais le message fondamental est clair : les spécialisations électriques autrefois considérées comme propres aux neurones corticaux humains semblent en réalité relever d’une stratégie primate partagée pour gérer un flux d’information complexe et rythmique.
Citation: Radaelli, C., Schmitz, M., Liu, XP. et al. HCN channels reveal conserved and divergent physiology in supragranular pyramidal neurons in primate species. Commun Biol 9, 279 (2026). https://doi.org/10.1038/s42003-026-09558-2
Mots-clés: canaux HCN, cortex des primates, neurones pyramidaux, rythmes delta thêta, Patch-seq