Clear Sky Science · fr
La thérapie dynamique stimulée par radionucléide induit des voies complémentaires de mort cellulaire immunogénique par nécroptose et apoptose
Retourner les ruses du cancer contre lui-même
Le cancer est réputé pour échapper à nos meilleurs traitements, en particulier les tumeurs mammaires agressives qui se disséminent dans l’organisme. Cette étude explore une approche inventive appelée thérapie dynamique stimulée par radionucléide (RaST), qui utilise des traceurs d’imagerie médicale et des nanoparticules activées par la lumière pour tuer les cellules cancéreuses d’une manière qui réveille aussi le système immunitaire. Pour le lecteur, ce travail est important car il suggère comment des outils d’imagerie existants et des matériaux intelligents pourraient être réaffectés pour créer un contrôle du cancer plus durable, porté par l’immunité, plutôt que de simples réductions temporaires de tumeur.
Une nouvelle façon d’éclairer les tumeurs de l’intérieur
Les traitements classiques à base de lumière n’agissent que là où un faisceau externe peut atteindre, comme la peau ou les tumeurs superficielles. RaST contourne cette limite en utilisant un sucre radioactif, semblable au traceur déjà employé en TEP, qui se concentre naturellement dans les cellules cancéreuses à croissance rapide. Lorsque ce traceur traverse la tumeur, il émet une faible lueur bleue connue sous le nom de rayonnement de Cerenkov. Les chercheurs ont conçu de minuscules nanoparticules de dioxyde de titane recouvertes d’une protéine ciblant le cancer, de sorte qu’elles se dirigent aussi vers la tumeur. Quand le traceur et les nanoparticules se rencontrent, la lumière interne active les particules, lesquelles génèrent alors des bouffées d’espèces réactives de l’oxygène — des molécules très réactives qui endommagent les cellules cancéreuses de l’intérieur.
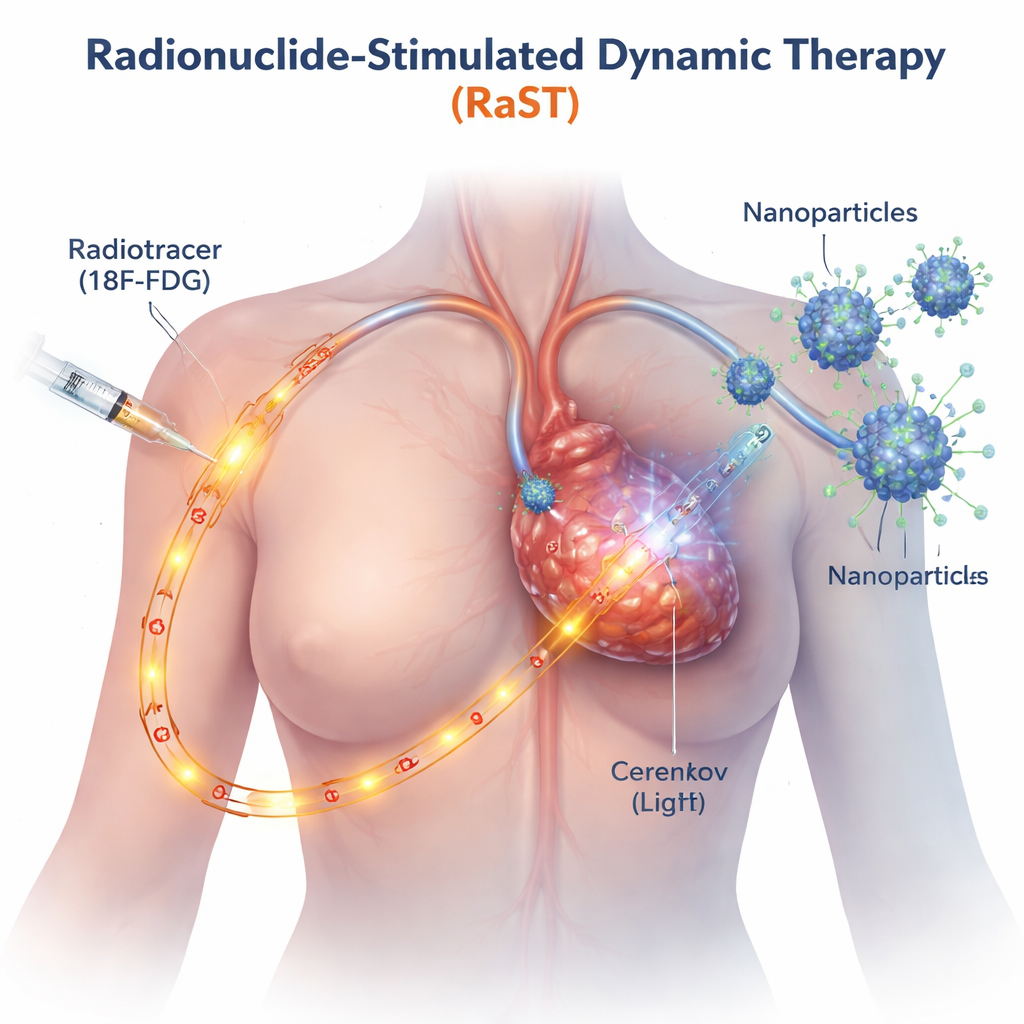
Déclencher deux voies distinctes de mort cellulaire
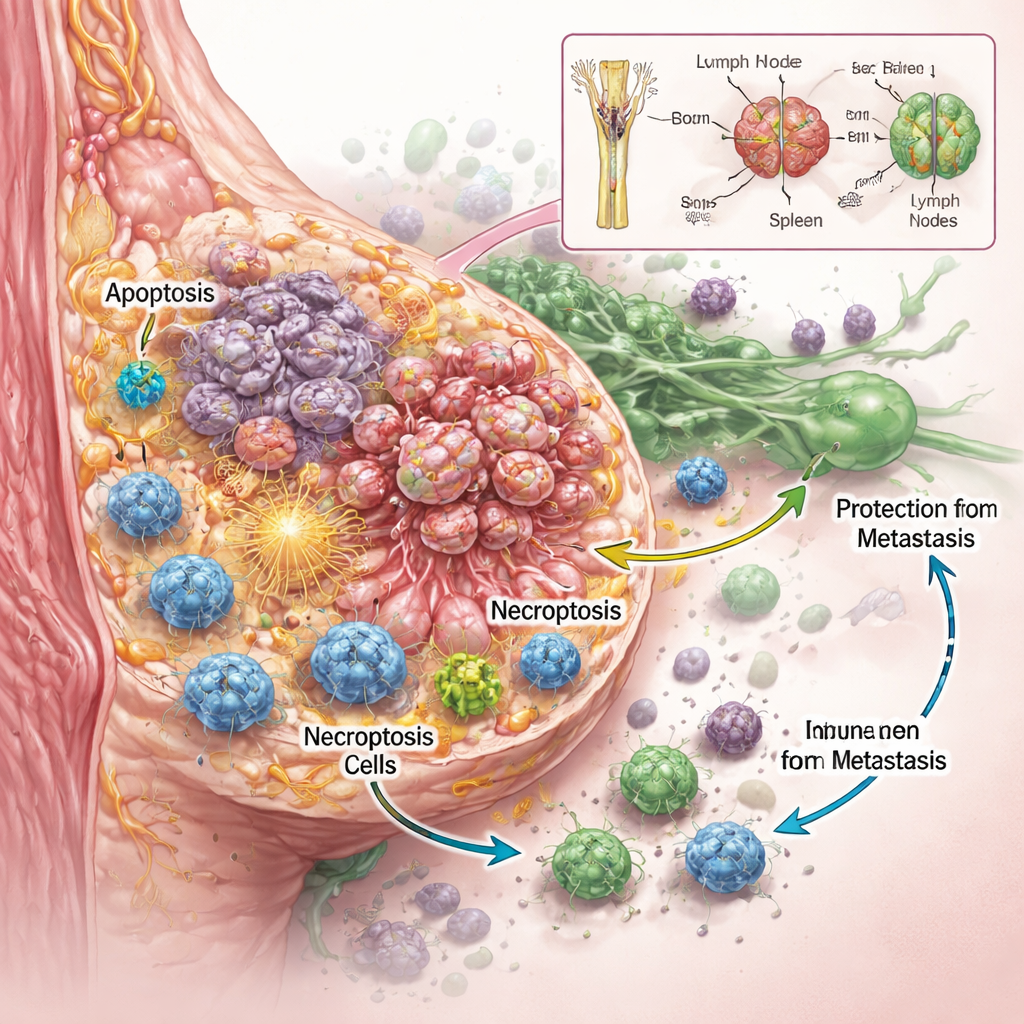
L’équipe voulait savoir non seulement si RaST tuait les cellules cancéreuses, mais comment. En utilisant plusieurs lignées cellulaires mammaires agressives en laboratoire, ils ont constaté que des doses finement réglées de traceur radioactif et de nanoparticules agissaient de concert pour endommager les cellules tumorales plus efficacement que chaque composant isolé, même dans des types connus pour résister à la chimiothérapie standard. Des images détaillées et des mesures protéiques ont révélé que RaST activait simultanément deux programmes régulés de mort cellulaire. L’un était l’apoptose, souvent décrite comme un « suicide » cellulaire, où la cellule se démonte de façon ordonnée. L’autre était la nécroptose, une forme plus explosive de mort où la cellule gonfle, se rompt et libère des signaux de détresse moléculaires dans son environnement. Ces signaux, connus sous le nom de molécules associées aux dommages et de cytokines inflammatoires, peuvent servir de balises qui attirent et activent les cellules immunitaires.
Mobiliser le système immunitaire pour un contrôle durable
Pour évaluer si ce mode inflammatoire d’élimination tumorale avait un impact in vivo, les chercheurs ont testé RaST dans des modèles murins du cancer du sein. Chez des souris dépourvues de défenses immunitaires clés, RaST a eu peu d’effet sur la croissance tumorale ou la dissémination pulmonaire, malgré une importante mort cellulaire locale. Mais chez des souris immunocompétentes, le même traitement a produit des réponses tumorales partielles et complètes et a empêché les métastases pulmonaires. Les tumeurs traitées par RaST se sont remplies de cellules immunitaires — en particulier des cellules myéloïdes telles que les macrophages et les cellules dendritiques — qui sont aptes à engloutir les débris et à présenter des fragments tumoraux aux lymphocytes T. Des analyses sanguines ont montré des vagues de signaux stimulant et régulant l’immunité au fil du temps, suggérant que RaST déclenche d’abord une attaque contre le cancer puis bascule vers un état plus équilibré à mesure que les tumeurs diminuent ou se stabilisent.
Chasser les reliquats cachés et prévenir les rechutes
Même chez des souris dont les tumeurs semblaient totalement guéries par RaST, un colorant d’imagerie hautement sensible a ensuite révélé de petites poches de cellules cancéreuses résiduelles logées dans des ganglions lymphatiques. Fait remarquable, ces animaux n’ont pas développé de nouvelles tumeurs ni de métastases à distance pendant de nombreux mois. Des analyses chimiques ont montré que les nanoparticules de dioxyde de titane, initialement abondantes dans les os et le foie, se sont progressivement redistribuées vers la rate et les ganglions lymphatiques — précisément les centres où patrouillent les cellules immunitaires. Cette migration lente maintient probablement une source locale d’oxygène réactif disponible pour les cellules immunitaires, les aidant à reconnaître et contrôler ces reliquats tumoraux cachés avant qu’ils ne puissent repousser ou se propager.
Ce que cela pourrait signifier pour la prise en charge future du cancer
En termes simples, ce travail montre que RaST n’est pas seulement une autre manière d’empoisonner les cellules tumorales. En combinant des traceurs radioactifs, des nanoparticules sensibles à la lumière et les défenses naturelles du corps, il pousse les cellules cancéreuses vers deux formes de mort programmée qui alertent fortement le système immunitaire. Chez des animaux immunocompétents, cela conduit à un contrôle durable de tumeurs mammaires agressives et bloque les métastases, même lorsque quelques cellules subsistent dans les ganglions lymphatiques. Bien qu’il reste beaucoup à faire avant que cette approche puisse être testée largement chez l’humain, l’étude ouvre la voie à des traitements futurs qui ne visent pas seulement à réduire la taille des tumeurs, mais à remodeler la relation entre cancer, mort cellulaire et immunité pour que l’organisme contribue à garder la maladie sous contrôle sur le long terme.
Citation: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Mots-clés: cancer du sein, nanoparticules, immunothérapie, thérapie par radionucléides, nécroptose