Clear Sky Science · fr
La glycophagie est une voie bilatérienne ancienne soutenant l’adaptation métabolique par l’évolution structurale de STBD1
Comment les huîtres révèlent des astuces énergétiques cachées
Les animaux survivant aux périodes difficiles puisent dans des réserves d’énergie, mais ils ne reposent pas tous sur le même type de « batterie ». Cette étude porte sur l’huître du Pacifique et montre que, contrairement à de nombreux autres animaux qui misent sur les lipides, les huîtres dépendent fortement du sucre stocké sous forme de glycogène. Les travaux mettent au jour une voie de recyclage cellulaire peu connue — la glycophagie — qui permet aux huîtres de vider et de reconstituer rapidement leurs réserves de sucre, et retracent l’évolution de ce système à travers le règne animal.
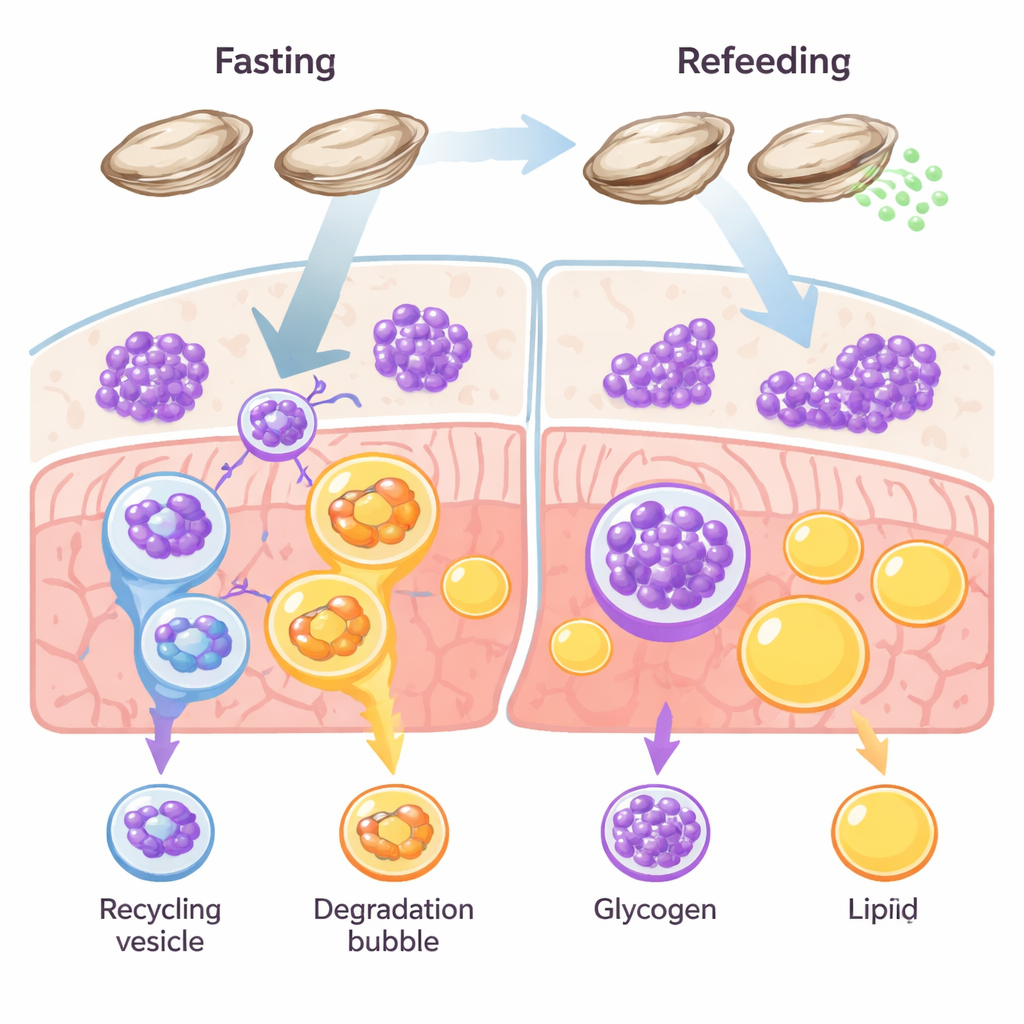
Une stratégie de survie axée sur le sucre
La plupart des animaux gèrent plusieurs réserves d’énergie, principalement des lipides et du glycogène. Chez les vertébrés, comme les poissons et les mammifères, les graisses dominent généralement les réserves à long terme. Les huîtres enfreignent cette règle. Leurs tissus sont riches en glycogène, et des travaux antérieurs suggéraient que ces mollusques consomment surtout du sucre, plutôt que des graisses, lors de la privation alimentaire ou de la production de gamètes. Les auteurs ont cherché à vérifier si la glycophagie — une dégradation ciblée du glycogène à l’intérieur des cellules — joue le rôle de voie de survie principale chez les huîtres durant le jeûne et la reprise alimentaire.
Observer les cellules passer du stockage à la dépense
L’équipe a privé d’alimentation des huîtres du Pacifique pendant deux semaines, puis les a réalimentées, en suivant la réponse de leurs tissus au fil du temps. Pendant le jeûne, des colorations microscopiques ont montré une augmentation des marqueurs d’autophagie — signaux de « nettoyage » cellulaire — précisément là où le glycogène était stocké, tandis que le glycogène lui-même diminuait. Les réserves lipidiques, en revanche, ont peu évolué. Quand les huîtres ont été réalimentées, le glycogène est rapidement revenu et les signaux d’autophagie ont chuté. Parallèlement, les niveaux d’une protéine réceptrice clé appelée STBD1, qui relie spécifiquement le glycogène à la machinerie d’autophagie, ont augmenté et diminué en phase avec l’utilisation du glycogène. Un autre récepteur associé au recyclage des lipides, p62, est resté globalement stable. Ensemble, ces profils indiquent une voie de recyclage dédiée centrée sur le sucre : la glycophagie, et non la lipophagie des graisses, assure l’essentiel de l’équilibre énergétique chez l’huître.
Le crochet moléculaire qui saisit le glycogène
La glycophagie repose sur STBD1 agissant comme un crochet moléculaire : il se lie au glycogène et le transmet à de petits adaptateurs qui construisent des vésicules de recyclage. Chez l’huître, STBD1 s’est avéré organisé différemment par rapport à son homologue de vertébrés. La protéine d’huître porte sa région de liaison au glycogène, connue sous le nom de domaine CBM20, à l’extrémité N-terminale, alors que STBD1 des vertébrés place ce même module à l’extrémité C-terminale et comporte une queue hydrophobe supplémentaire qui l’ancre aux membranes cellulaires. Des modèles informatiques et des simulations suggèrent que l’agencement N-terminal chez l’huître confère au CBM20 une prise plus forte et plus polyvalente sur les chaînes sucrées ramifiées. Des expériences en laboratoire confirment ces résultats : la STBD1 d’huître purifiée liait le glycogène plus fortement que les STBD1 de poisson ou de souris, et lorsque toutes les versions étaient exprimées dans des cellules humaines, la protéine d’huître provoquait une baisse plus marquée du glycogène lors d’autophagie induite.
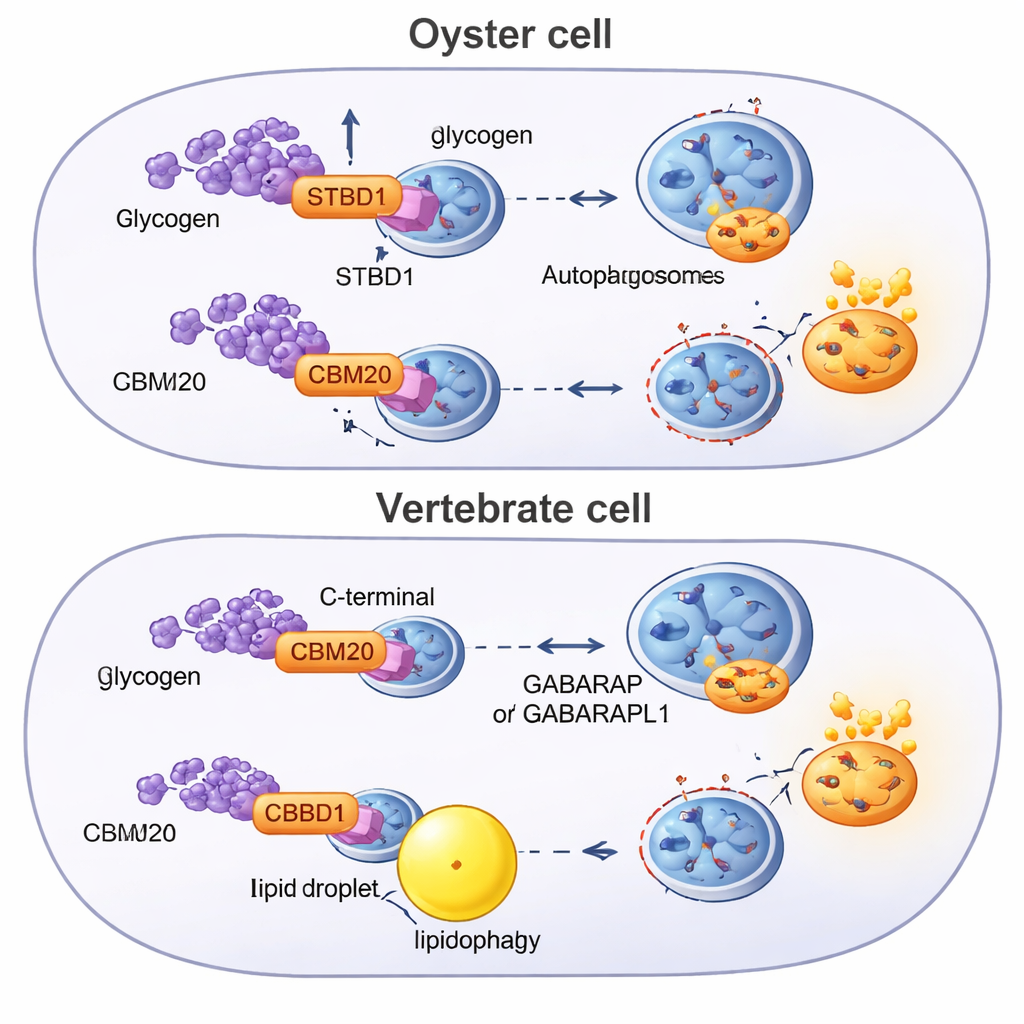
Réagencer une voie ancienne chez les animaux
Pour comprendre l’origine de ce système, les chercheurs ont analysé les génomes de dizaines d’animaux à la recherche de protéines contenant CBM20 et ont construit des arbres évolutifs. Ils ont constaté que STBD1 est une invention des bilatériens — apparaissant chez l’ancêtre commun des animaux à plan corporel bilatéral — mais que sa structure a été remaniée dans différentes lignées. Les huîtres et d’autres lophotrochozoaires conservent généralement le design ancestral avec CBM20 en position N-terminale, parfois même en dupliquant le module de liaison au sucre. Les chordés, le groupe qui inclut les vertébrés, présentent une version distincte où le CBM20 a été déplacé vers la queue de la protéine. Ce réarrangement corrèle avec une liaison au glycogène plus faible et avec une stratégie métabolique qui mise davantage sur la dégradation des graisses via la lipophagie, soutenue par d’autres récepteurs d’autophagie et protéines adaptatrices que les huîtres n’ont pas.
Ce que cela signifie pour les choix énergétiques de la vie
Pour le grand public, le message est que les animaux ont évolué plusieurs façons de faire face aux pénuries d’énergie. Les huîtres illustrent une stratégie ancienne centrée sur le sucre : une version de STBD1 à haute affinité saisit rapidement le glycogène et l’achemine vers les unités de recyclage cellulaires, faisant de la glycophagie une source d’énergie majeure en période de stress. Les vertébrés, en revanche, semblent avoir échangé une partie de cette forte liaison au sucre contre une approche plus équilibrée ou orientée vers les lipides, soutenue par des partenaires protéiques et des architectures de domaines différents. En reliant la structure fine des protéines aux choix de carburant au niveau de l’organisme, cette étude montre comment de petits « recâblages » moléculaires peuvent aider différentes branches de l’arbre animal à s’adapter à leurs environnements et modes de vie.
Citation: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
Mots-clés: glycophagie, métabolisme du glycogène, biologie de l’huître, autophagie, évolution du métabolisme