Clear Sky Science · fr
Réagencement épigénétique et métabolique dans les phéochromocytomes et paragangliomes métastatiques induit par des mutations SDHB
Pourquoi ces tumeurs rares comptent
Les phéochromocytomes et les paragangliomes sont des tumeurs rares qui proviennent de cellules nerveuses productrices d’hormones, souvent à proximité des glandes surrénales. La plupart évoluent lentement et peuvent être guéries par chirurgie, mais environ un cas sur cinq finit par se propager à d’autres organes, devenant potentiellement mortel. Cette étude pose une question simple mais cruciale : qu’est‑ce qui fait que certaines de ces tumeurs deviennent dangereuses ? En explorant en profondeur la façon dont ces cancers activent ou silencent leurs gènes et comment ils se nourrissent, les chercheurs mettent au jour une faiblesse cachée qui pourrait un jour être ciblée par de nouveaux traitements.
De la croissance tranquille à la dissémination mortelle
L’équipe s’est concentrée sur les tumeurs portant des altérations d’un gène appelé SDHB. SDHB aide les mitochondries — les centrales énergétiques de la cellule — à faire fonctionner une étape du cycle de Krebs, une voie centrale de production d’énergie. Lorsque SDHB est altéré, une molécule nommée succinate s’accumule, et les cellules commencent à se comporter comme si elles vivaient en hypoxie, même lorsque ce n’est pas le cas. Les chercheurs ont étudié des tissus provenant de 34 patients, comparant des tumeurs restées localisées à des tumeurs déjà disséminées. En utilisant une carte haute résolution de la « méthylation » de l’ADN, qui montre comment des marques chimiques augmentent ou diminuent l’expression des gènes, ils ont découvert que les tumeurs métastatiques présentaient un profil plus marqué de silencement génique que les tumeurs bénignes, en particulier lorsque SDHB était muté.
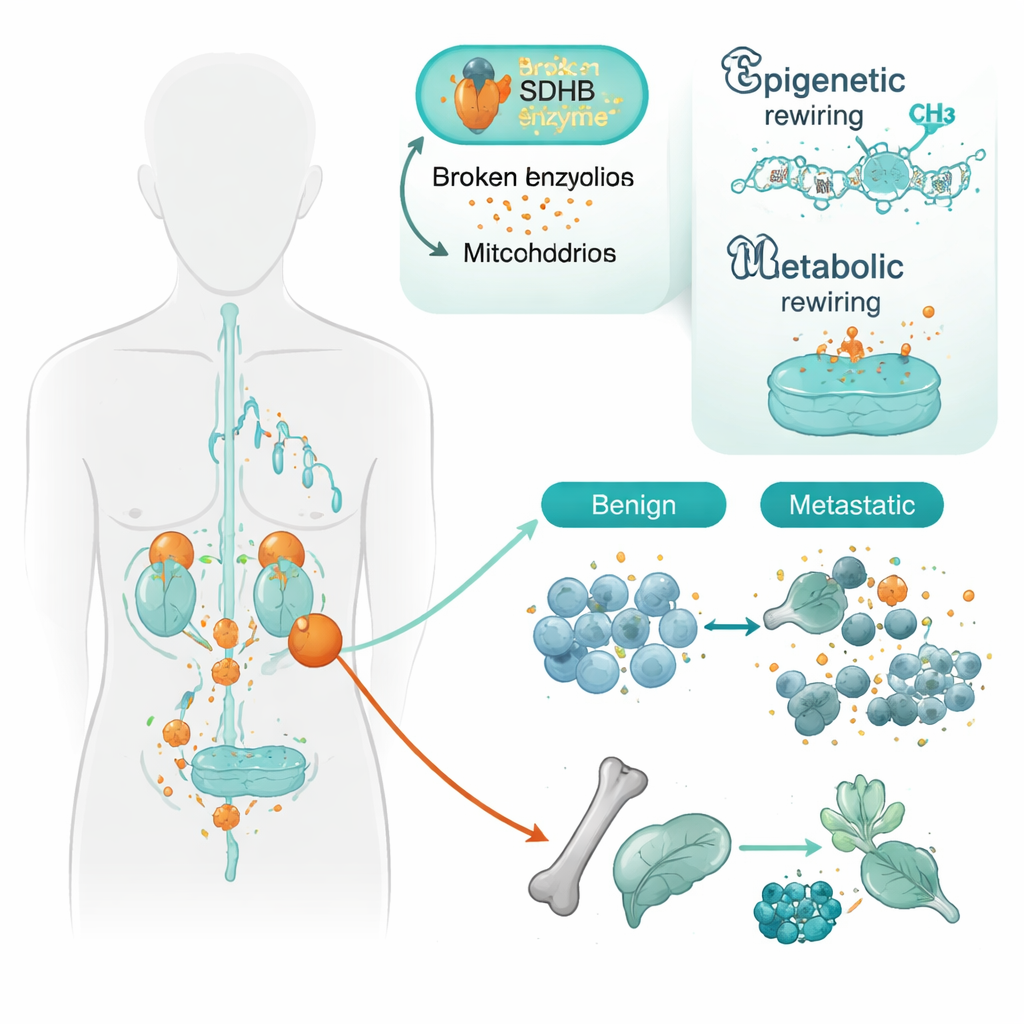
Reprogrammation de l’identité cellulaire
Beaucoup des gènes silencés dans les tumeurs agressives sont ceux qui aident les cellules de type nerveux à mûrir et à conserver leur identité spécialisée. Il s’agit notamment de familles de gènes qui dirigent l’adhésion cellulaire, l’organisation de l’ADN et la détermination du type cellulaire. Un exemple marquant est le gène d’adhésion cellulaire PCDHGC3. Même dans les tumeurs SDHB mutées non disséminées, la région de contrôle de ce gène était déjà partiellement désactivée ; dans les tumeurs métastatiques, le silencement était encore plus prononcé. Un autre gène, SATB2, impliqué dans l’organisation de larges domaines d’ADN, était quant à lui silencé uniquement dans les tumeurs métastatiques, indépendamment du statut SDHB. Ensemble, ces profils suggèrent que la perte de SDHB « prépare » les cellules à un état moins mature et plus mobile, et que des modifications épigénétiques supplémentaires favorisent ensuite leur détachement et leur dissémination.
Réorientation du métabolisme des sucres
De façon surprenante, toutes les modifications ne consistaient pas en un arrêt d’expression. Un plus petit ensemble de gènes devenait moins méthylé et plus actif, et ceux‑ci étaient fortement impliqués dans l’entrée des sucres dans les cellules. Parmi eux, le gène transporteur du fructose SLC2A5 se distinguait. Son produit, connu sous le nom de GLUT5, fait entrer le fructose — un sucre courant dans les fruits et dans de nombreux aliments transformés — dans les cellules. Dans des modèles cellulaires exposés à de faibles niveaux d’oxygène, SLC2A5 s’est progressivement activé, tandis que d’autres transporteurs de sucre répondaient de façon moins cohérente. Les auteurs ont ensuite établi des cultures cellulaires dérivées de tumeurs PPGL de patients et montré que, lorsque le glucose était rare, l’ajout de fructose aidait ces cellules à continuer à se diviser, en particulier en conditions de faible oxygène qui reproduisent l’environnement tumoral.
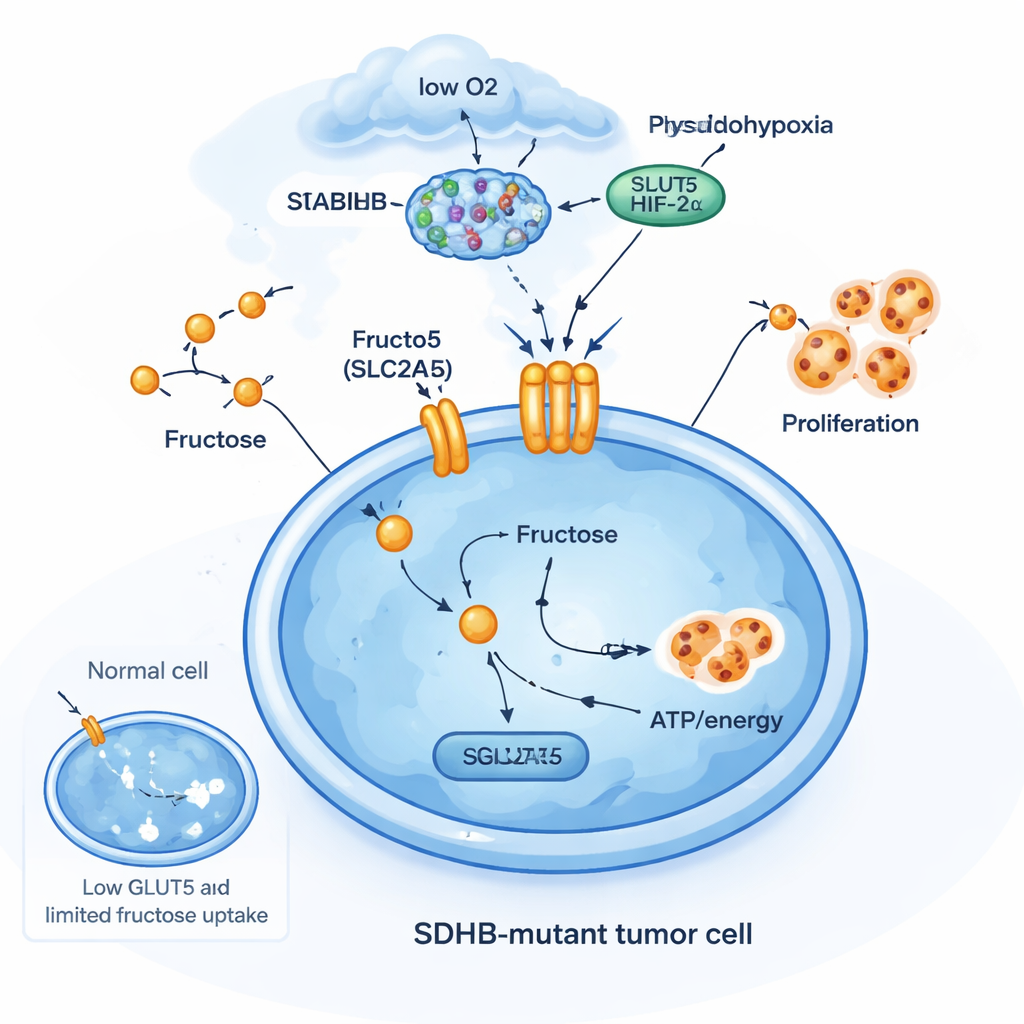
Un tour de survie alimenté par le fructose
Pour comprendre pourquoi les mutations SDHB sont importantes ici, l’équipe a édité plusieurs types cellulaires pour supprimer SDHB. Dans des cellules de type chromaffine provenant de la surrénale et dans une lignée de cancer rénal caractérisée par une activation constante du facteur sensoriel d’oxygène HIF2α, la perte de SDHB a augmenté les niveaux de SLC2A5. Mais dans des lignées tumorales plus courantes dépourvues de ces caractéristiques neuroendocrines ou de HIF2α, le même knock‑out de SDHB n’a pas activé SLC2A5. Cela montre que le transporteur de fructose ne fait pas partie d’une réponse au stress générique ; il s’agit d’une adaptation très spécifique à certains types cellulaires déjà en état de « pseudo‑hypoxie ». Dans ces cellules, la perte de SDHB, l’accumulation de succinate et l’activité de HIF2α coopèrent pour ouvrir une nouvelle porte métabolique : l’entrée de fructose pour alimenter la croissance lorsque l’oxygène et le glucose sont limités.
Que signifie tout cela pour les patients
En termes simples, l’étude révèle un double basculement dans les PPGL métastatiques porteurs de mutations SDHB. D’abord, leur système de contrôle de l’ADN est réorganisé pour pousser les cellules vers un état moins spécialisé et plus plastique, sujet à l’invasion. Ensuite, leur système énergétique est réorienté pour puiser dans le fructose comme carburant alternatif dans des niches hostiles, pauvres en oxygène et en glucose. En identifiant le transporteur de fructose SLC2A5/GLUT5 comme acteur clé de ce processus, ce travail pointe vers un talon d’Achille possible : bloquer l’entrée ou le métabolisme du fructose pourrait affamer sélectivement ces tumeurs tout en épargnant la plupart des tissus normaux. Bien que de tels traitements ne soient pas encore disponibles, cartographier ce paysage épigénétique et métabolique est une étape cruciale vers des thérapies plus précises, centrées sur le métabolisme, pour les patients atteints de PPGL SDHB‑mutés à haut risque.
Citation: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Mots-clés: phéochromocytome, paragangliome, mutation SDHB, épigénétique, métabolisme du fructose