Clear Sky Science · fr
Analyse multi-omique des réseaux de signalisation humains de PHACTR1
Pourquoi ce gène vasculaire vous concerne
Les infarctus, les AVC et l’hypertension renvoient tous à l’état de santé de nos vaisseaux sanguins. Un seul gène, PHACTR1, est apparu à plusieurs reprises dans de larges études génétiques sur ces pathologies, mais les chercheurs n’en comprenaient pas encore la raison. Cette étude a utilisé un examen à grande échelle, « toutes couches confondues », à l’intérieur de cellules humaines pour cartographier ce que fait réellement PHACTR1, révélant comment il peut influencer la croissance cellulaire, l’utilisation de l’énergie et la gestion du fer — des processus qui façonnent en fin de compte la santé des artères.
Un balayage global à l’intérieur des cellules
Plutôt que de se concentrer sur une molécule à la fois, les chercheurs ont utilisé une stratégie dite multi-omique — mesurant simultanément des milliers d’ARN, de protéines, de petits métabolites et de lipides dans les cellules. Ils ont modifié des cellules humaines pour qu’elles produisent soit un excès de PHACTR1, soit une expression réduite du gène, reproduisant des différences génétiques naturelles observées chez l’humain. En comparant ces cellules altérées à des témoins normaux à travers quatre couches moléculaires, puis en soumettant les données à des logiciels de voies biochimiques sophistiqués, ils ont construit une carte globale de la façon dont la variation de PHACTR1 se répercute dans la machinerie interne de la cellule. 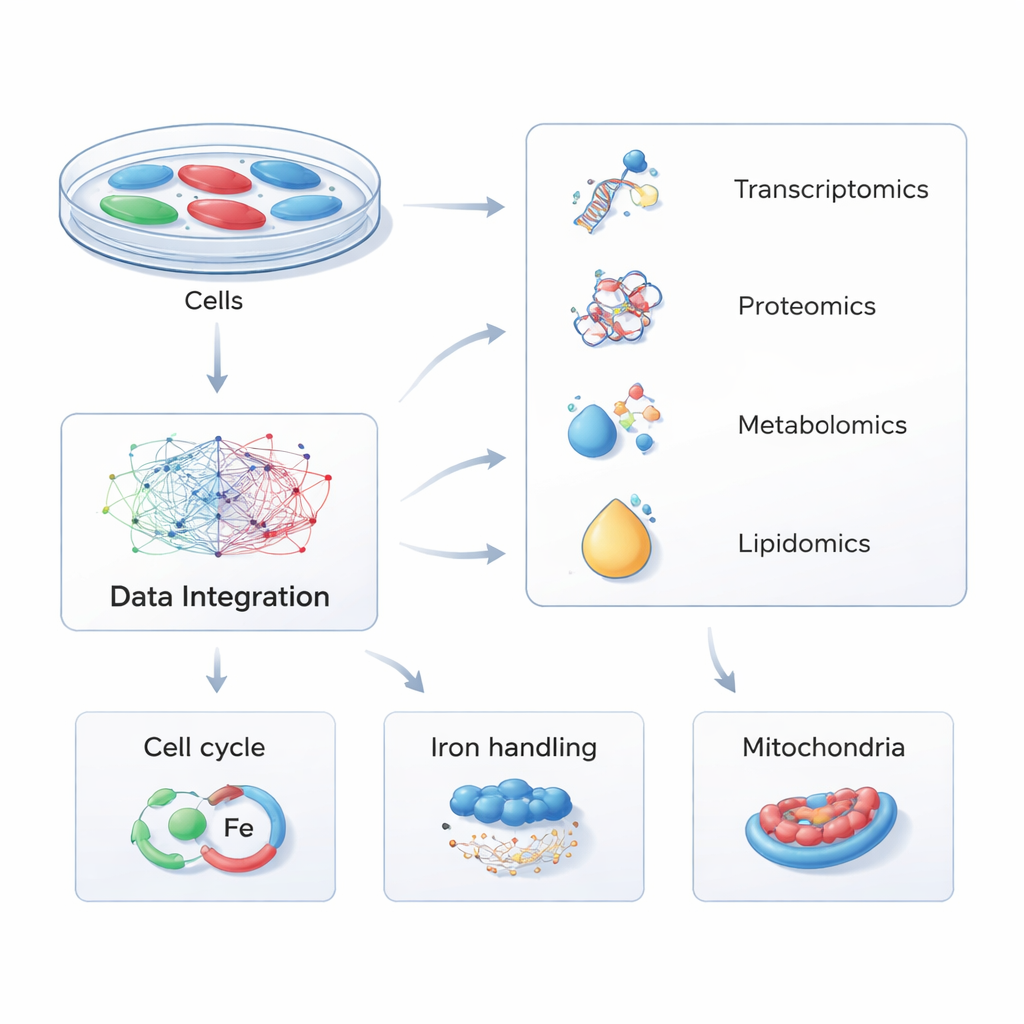
Au-delà du squelette cellulaire : contrôler les cycles de croissance
PHACTR1 était surtout connu pour aider à organiser l’ossature interne de la cellule composée de filaments d’actine. Les nouvelles données montrent qu’il intervient aussi fortement dans le contrôle du cycle cellulaire — la chorégraphie par laquelle la cellule copie son ADN et se divise. Les cellules avec un excès de PHACTR1 sont sorties de la phase de repos G1 et se sont accumulées dans les phases de copie de l’ADN et de préparation à la division, avec moins de cellules parvenant à entrer en mitose complète. Des régulateurs clés tels que la cycline B1, Cdt1 et d’autres protéines du cycle cellulaire étaient modifiés. Lorsque l’équipe a répété les expériences dans des cellules endothéliales humaines primaires — les cellules qui tapissent les vaisseaux — ils ont de nouveau observé des changements dans ces régulateurs centraux du cycle. Cela suggère que PHACTR1 contribue à décider quand les cellules vasculaires se reposent, se divisent ou s’arrêtent, un équilibre crucial à la fois pour réparer la paroi des vaisseaux et pour la formation d’excroissances tissulaires dangereuses.
Gérer le fer et se protéger des dommages
L’intégration multi-omique a également mis en évidence des voies liées au fer et une forme spécialisée de mort cellulaire liée au fer, appelée ferroptose. Bien que les cellules n’aient pas activement subi de ferroptose, l’augmentation de PHACTR1 a réduit les niveaux de protéines majeures de gestion du fer, y compris la chaîne lourde de la ferritine (la principale coque de stockage du fer) et l’hème oxygénase 1 (qui recycle le fer issu de l’hème). Dans les cellules endothéliales primaires, PHACTR1 modifiait de façon similaire ces protéines et des défenseurs clés contre les dommages oxydatifs. Comme une mauvaise gestion du fer peut alimenter l’inflammation, le stress oxydatif et la fragilité des plaques artérielles, ces résultats suggèrent que PHACTR1 pourrait régler la manière dont les cellules vasculaires stockent et détoxifient le fer, affectant potentiellement la vulnérabilité à certaines maladies vasculaires.
Mitrochondries, énergie et santé des artères
Une autre surprise fut le rôle de PHACTR1 dans les mitochondries, les centrales énergétiques de la cellule. L’équipe a trouvé la protéine PHACTR1 dans des mitochondries isolées et observé que la modification de ses niveaux restructurait le réseau mitochondrial. Lorsque PHACTR1 était élevé, les mitochondries étaient plus allongées, et une protéine appelée Drp1 présentait une modification chimique en un site qui réduit la fragmentation mitochondriale. Les niveaux d’une protéine échafaudage, AKAP1, qui aide à organiser la signalisation à la surface mitochondriale, variaient en phase avec PHACTR1. Ces changements structurels correspondaient à des altérations de la production d’énergie : un PHACTR1 élevé réduisait la production mitochondriale d’ATP et était lié à l’accumulation de certains dérivés d’acides gras suggérant une oxydation lipidique ralentie, tandis qu’un PHACTR1 faible poussait les cellules à dépendre davantage de la glycolyse (brûlage du sucre). Des analyses d’échantillons d’artères humaines ont montré que PHACTR1 et AKAP1 ont tendance à être activés ensemble, reliant directement ce circuit de contrôle mitochondrial aux vaisseaux réels. 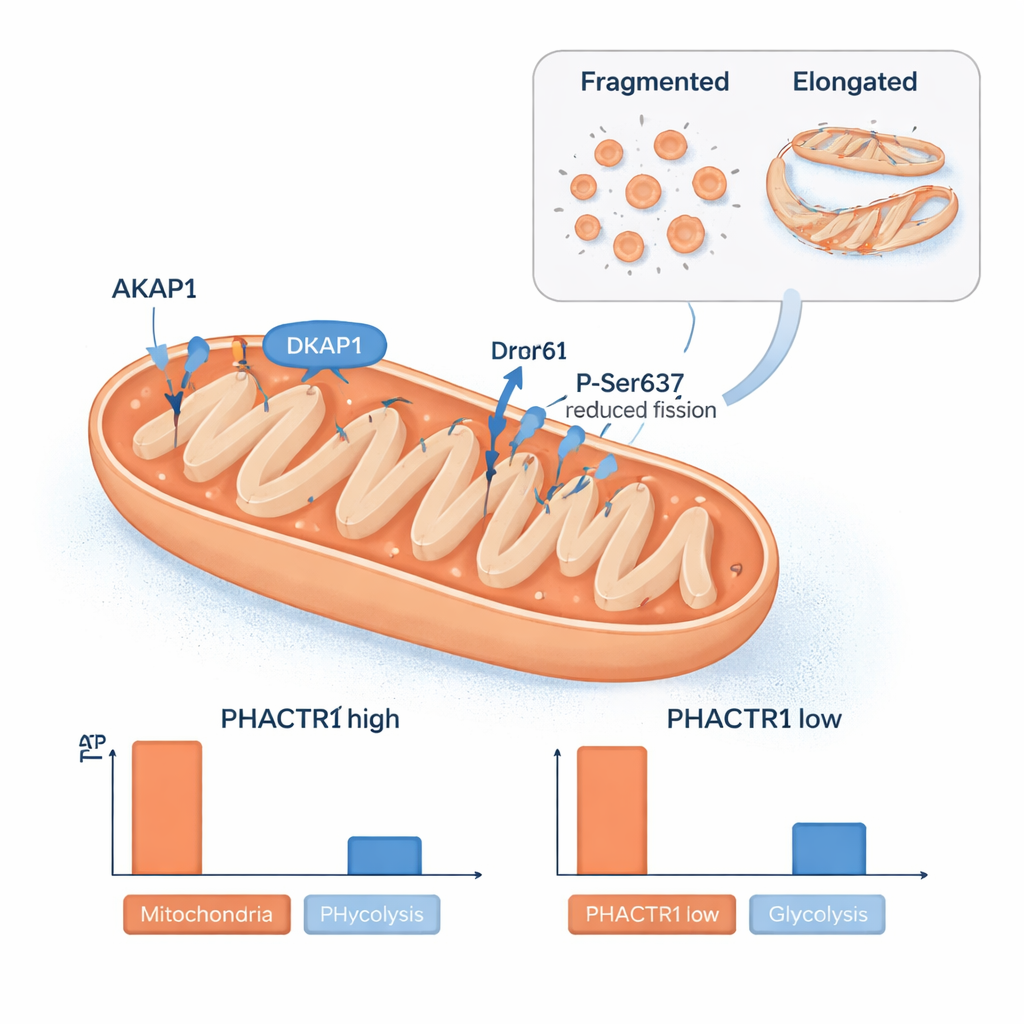
Que signifie tout cela pour les vaisseaux sanguins
Dans l’ensemble, ce travail montre que PHACTR1 n’est pas un gène à usage unique mais un coordonnateur majeur qui touche la division cellulaire, le stockage du fer et le métabolisme énergétique des cellules vasculaires. En cartographiant ces connexions à l’échelle de milliers de molécules, l’étude aide à expliquer pourquoi des variations naturelles de PHACTR1 sont associées à un large éventail de maladies vasculaires — de la maladie coronarienne aux déchirures artérielles spontanées et à la migraine. Pour le grand public, le message est qu’un gène repéré par la génétique humaine est désormais rattaché à des comportements cellulaires concrets qui influencent la croissance des plaques, la stabilité des vaisseaux et l’équilibre énergétique. À long terme, comprendre ces réseaux contrôlés par PHACTR1 pourrait ouvrir la voie à des thérapies plus ciblées qui rééquilibrent les cycles cellulaires, la gestion du fer ou la fonction mitochondriale chez les personnes à risque de maladie cardiovasculaire.
Citation: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Mots-clés: PHACTR1, maladie vasculaire, multi-omique, mitochondries, métabolisme du fer