Clear Sky Science · fr
Cibler PAK4 favorise la pyroptose induite par la gemcitabine dans le cancer du pancréas via l’axe NLRP1/caspase-3/GSDME
Pourquoi tuer les cellules cancéreuses de façon « explosive » pourrait compter
Le cancer du pancréas fait partie des cancers les plus meurtriers et même nos meilleurs médicaments chimiothérapeutiques finissent souvent par perdre de leur efficacité lorsque les tumeurs deviennent résistantes. Cette étude explore un renversement surprenant : le même médicament, la gemcitabine, peut tuer les cellules cancéreuses d’une manière plus explosive et inflammatoire appelée pyroptose — à condition qu’un « frein » moléculaire clé nommé PAK4 soit désactivé. Comprendre et cibler ce frein pourrait améliorer l’efficacité des traitements existants pour de nombreux patients.
Un cancer tenace qui se défait des traitements
L’adénocarcinome canalaire pancréatique est le plus souvent diagnostiqué tardivement et répond mal aux traitements, de sorte que la gemcitabine reste un médicament de référence malgré ses limites. La gemcitabine tue habituellement les cellules par apoptose, une forme ordonnée et silencieuse de mort cellulaire programmée. Mais plus de la moitié des tumeurs pancréatiques examinées dans cette étude produisaient des niveaux élevés d’une protéine appelée GSDME, qui peut transformer cette mort silencieuse en pyroptose — une forme rapide et « explosive » de mort cellulaire qui endommage la membrane cellulaire et libère des signaux inflammatoires. Cela pose une question centrale : si les tumeurs peuvent subir la pyroptose, pourquoi tant d’entre elles résistent-elles encore à la gemcitabine ?
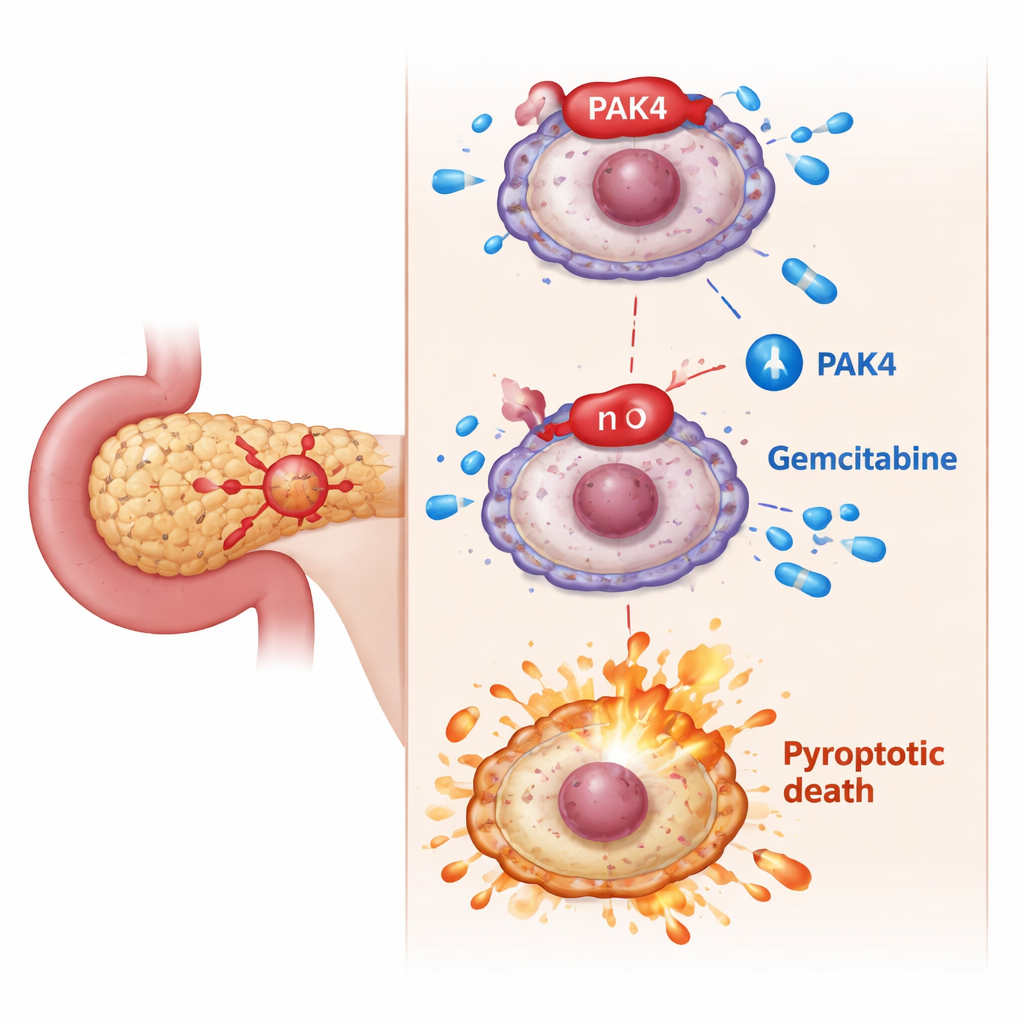
Le frein caché : PAK4 bloque la mort cellulaire « incendiaire »
Les chercheurs se sont intéressés à PAK4, une protéine promotrice de croissance connue pour être hyperactive dans le cancer du pancréas et associée à une mauvaise réponse à la gemcitabine. Dans des expériences cellulaires, les cellules cancéreuses présentant de hauts niveaux de PAK4 étaient plus difficiles à tuer avec la gemcitabine. Lorsque l’équipe a réduit PAK4, la gemcitabine est devenue beaucoup plus létale : les cellules présentaient les caractéristiques classiques de la pyroptose — gonflement, bulles en forme de ballon, rupture des membranes et libération accrue du contenu intracellulaire. Au niveau moléculaire, ce basculement dépendait de la coupure de GSDME en un fragment actif par une autre protéine, la caspase-3. Bloquer la caspase-3 empêchait GSDME de déclencher la pyroptose, confirmant que PAK4 agit normalement pour contenir cette voie de mort.
Comment PAK4 démantèle l’alarme de mort de la cellule
En approfondissant, les scientifiques ont découvert que PAK4 n’attaque pas GSDME directement. Il sabote plutôt un « capteur d’alarme » en amont appelé NLRP1. Chez les patients, des niveaux plus élevés de NLRP1 étaient associés à une meilleure survie, ce qui suggère qu’il aide l’organisme à contenir les tumeurs. Dans les cellules cancéreuses, lorsque NLRP1 était supprimé, la mort cellulaire induite par la gemcitabine et l’activation de GSDME diminuaient fortement, montrant que NLRP1 alimente la machinerie de la pyroptose. Les niveaux de PAK4 et de NLRP1 étaient inversement corrélés dans les échantillons tumoraux : là où PAK4 était élevé, NLRP1 était bas. L’étude a montré que PAK4 actif agit via une autre protéine, la ligase E3 Mdm2, pour marquer NLRP1 en vue d’une destruction par le système d’élimination cellulaire. En marquant NLRP1 de cette manière, PAK4 empêche l’activation d’une réaction en chaîne — via la caspase-9 et la caspase-3 — qui aboutirait normalement à une pyroptose pilotée par GSDME.
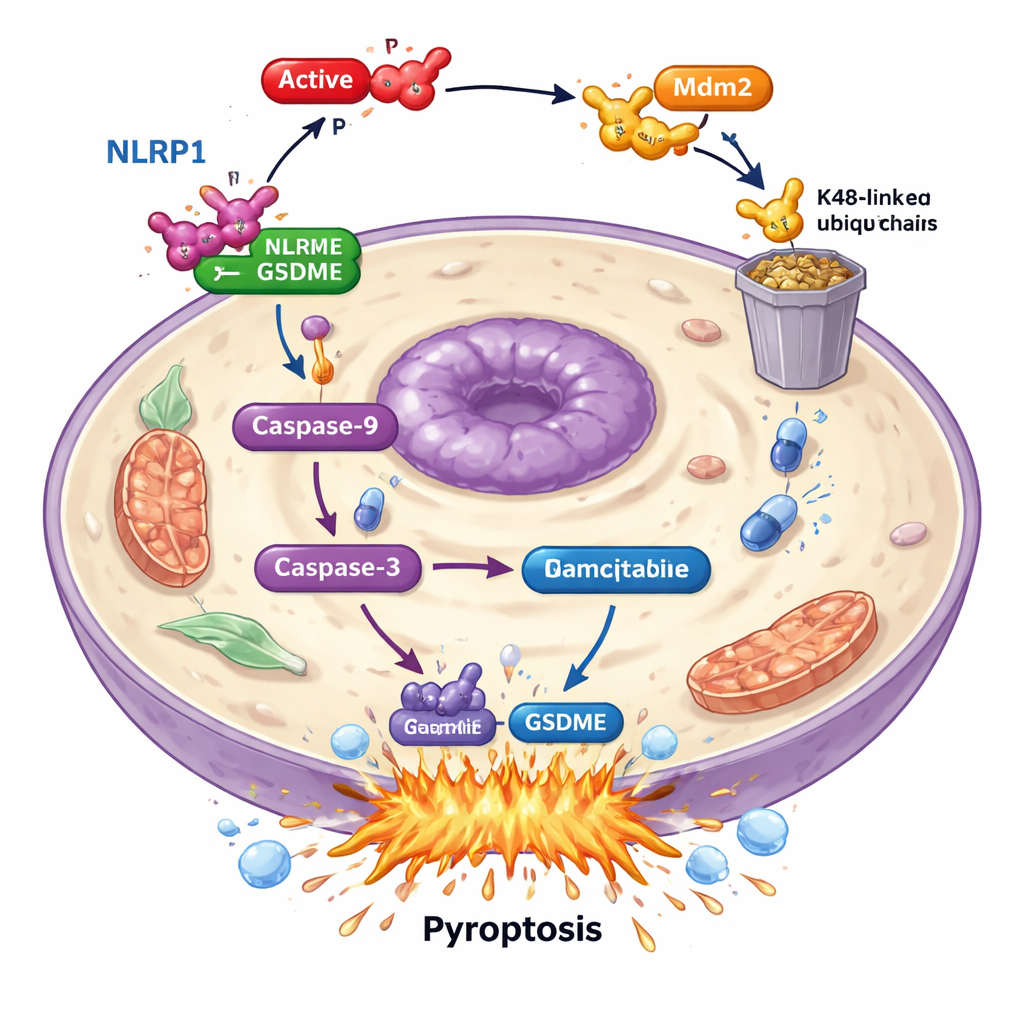
Couper PAK4 pour suralimenter la chimiothérapie
Parce que PAK4 joue le rôle de frein sur la pyroptose, l’équipe a testé si bloquer son activité pouvait réactiver le pouvoir létal de la gemcitabine. Ils ont utilisé un inhibiteur de PAK4 de petite molécule appelé PF-3758309. Seul, cet inhibiteur poussait déjà les cellules du cancer du pancréas vers la pyroptose, augmentant l’activation de la caspase-3, la coupure de GSDME et la rupture de la membrane cellulaire. Lorsqu’il était combiné à la gemcitabine, l’effet était encore plus prononcé : plus de cellules mouraient par pyroptose et les marqueurs moléculaires de la voie de mort étaient amplifiés. Chez des souris porteuses de tumeurs pancréatiques humaines, soit la réduction de PAK4 soit le traitement par l’inhibiteur de PAK4 rendait la gemcitabine plus efficace pour réduire les tumeurs et augmentait les marqueurs pyroptotiques au sein des cancers.
Ce que cela signifie pour les patients et les traitements futurs
En termes simples, ce travail révèle une serrure moléculaire — PAK4 — qui empêche les cellules du cancer du pancréas de mourir d’une manière particulièrement destructive sous chimiothérapie. En désactivant PAK4, les cliniciens pourraient pousser les tumeurs traitées par la gemcitabine vers la pyroptose, rendant le médicament plus efficace et stimulant potentiellement la réponse immunitaire contre le cancer. Bien que des travaux supplémentaires sur des modèles dérivés de patients et des essais cliniques soient nécessaires, l’étude propose une feuille de route claire : cibler la voie PAK4–Mdm2–NLRP1–GSDME pour convertir des tumeurs résistantes en tumeurs sensibles, en utilisant des médicaments déjà disponibles dans des combinaisons mieux réfléchies.
Citation: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Mots-clés: cancer du pancréas, résistance à la gemcitabine, pyroptose, PAK4, thérapie ciblée