Clear Sky Science · fr
WDR62 est nécessaire à la prolifération correcte et à la différenciation précoce des myoblastes squelettiques
Pourquoi la croissance musculaire exige un timing précis
Nos muscles n’augmentent pas simplement de volume parce que nous nous entraînons ; ils croissent et se réparent via une chorégraphie précise de cellules souches qui doivent se diviser, attendre, puis finalement se transformer en muscle fonctionnel. Cet article dissèque le rôle d’une protéine souvent négligée, WDR62, pour maintenir cette chorégraphie en rythme. Lorsque WDR62 est absente ou défectueuse, les muscles deviennent plus petits et les cellules qui devraient se multiplier patiemment se précipitent trop vite vers des fibres matures, laissant trop peu de cellules en réserve pour la force et la réparation à long terme.
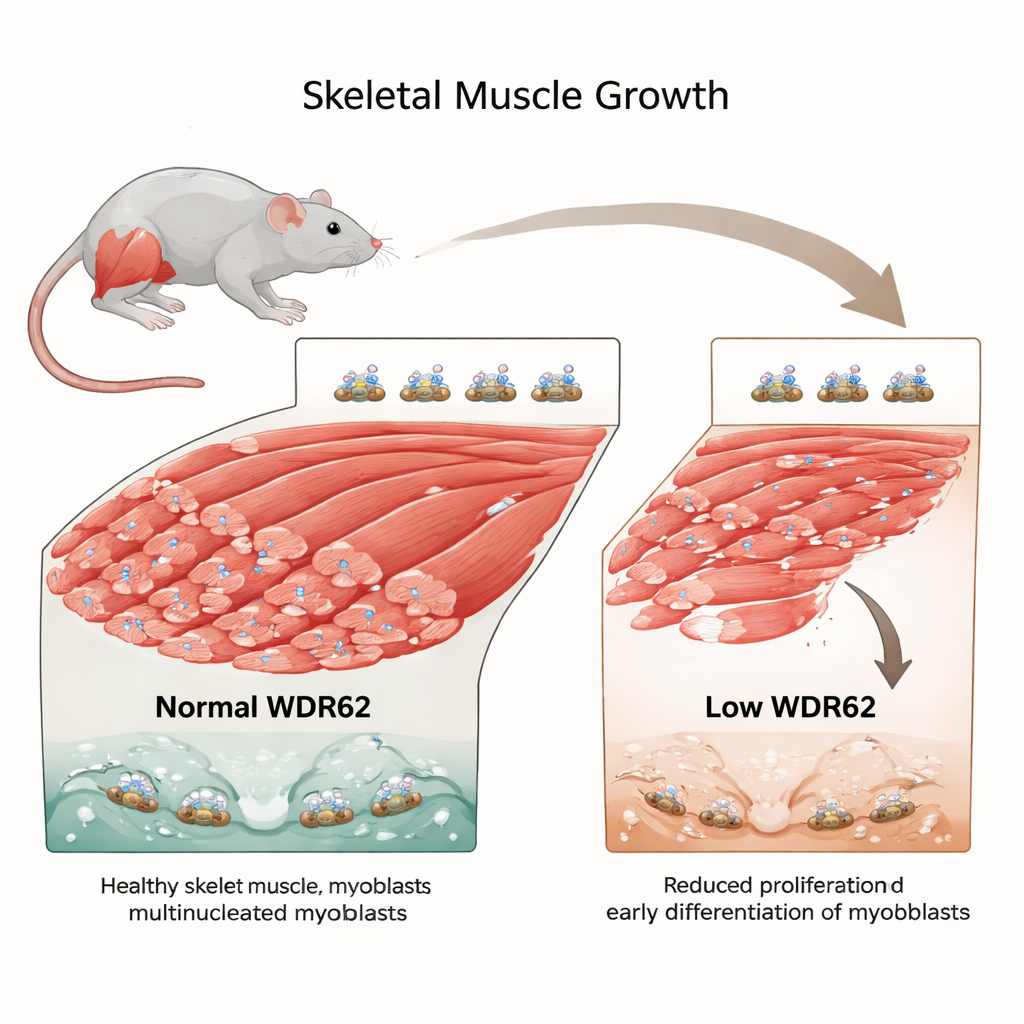
Un organisateur caché à l’intérieur des cellules souches musculaires
WDR62 est une protéine qui se localise à de minuscules structures cellulaires appelées centrosomes, qui aident à organiser l’échafaudage tirant les chromosomes lors de la division cellulaire. WDR62 a déjà été associée au développement cérébral, où sa perte peut provoquer un cerveau plus petit parce que les cellules souches précoces cessent de se diviser trop tôt. Les auteurs se sont demandé si un phénomène similaire se produisait dans le muscle squelettique, où des cellules souches spécialisées — appelées cellules satellites — s’activent après une blessure, se divisent plusieurs fois en myoblastes, puis fusionnent pour construire ou réparer les fibres musculaires. Si WDR62 aide ces cellules à se diviser correctement dans le cerveau, pourrait-elle aussi être cruciale pour former un muscle sain ?
Muscles plus petits et développement précipité
Pour tester cela, l’équipe a étudié des souris conçues pour ne pas avoir de WDR62 fonctionnelle. Même sans blessure, deux muscles de la patte, importants pour le mouvement — le tibial antérieur et l’extenseur digitorum longus — étaient visiblement plus petits que chez des souris normales. Au microscope, l’architecture musculaire de base paraissait normale, mais il y avait légèrement moins de fibres au total, ce qui suggère qu’il n’y avait pas assez de myoblastes disponibles pour construire un muscle de taille normale. Lorsqu’ils ont provoqué une lésion du muscle par une toxine standard qui force la régénération, la séquence globale de réparation semblait globalement normale. Cependant, environ une semaine après la blessure, les souris déficientes en WDR62 présentaient plus de fibres nouvellement formées et immatures que leurs homologues saines, ce qui suggère que leurs myoblastes se différenciaient et fusionnaient plus tôt qu’ils ne devraient.
Effets conservés des mouches aux cellules en culture
Pour voir si ce comportement était fondamental et pas seulement une curiosité chez la souris, les auteurs se sont tournés vers la drosophile, qui possède aussi des cellules précurseures musculaires dans son aile en développement. La réduction de Wdr62 dans ces myoblastes de mouche a entraîné moins de cellules précurseures et davantage de divisions asymétriques — des scissions cellulaires produisant une cellule de type souche et une fille plus engagée. Trop de ces divisions asymétriques épuise la réserve de cellules souches, comme observé dans le cerveau de souris. Parallèlement, l’équipe a utilisé une lignée cellulaire musculaire murine classique, C2C12, cultivée en lames. Lorsqu’ils ont réduit l’expression de WDR62 dans ces cellules, moins de cellules entraient dans le cycle cellulaire et se divisaient, mais celles qui le faisaient commençaient à fusionner en fibres musculaires précoces légèrement en avance sur le calendrier, pointant encore une fois vers un compromis : une prolifération réduite associée à une différenciation prématurée.
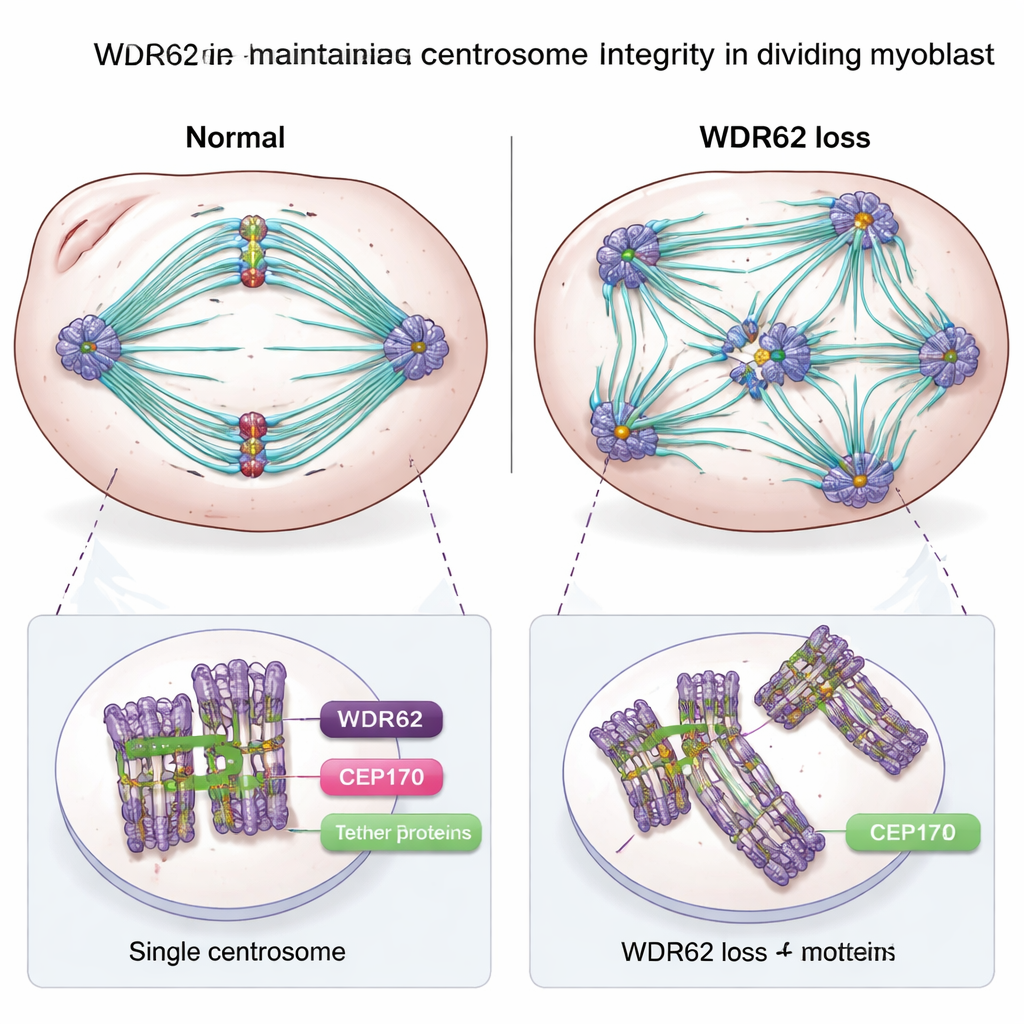
Les « plates-formes » cellulaires perdent leur équilibre
En approfondissant, les chercheurs ont examiné les centrosomes eux-mêmes. Dans des myoblastes sains, chaque cellule en division possède typiquement deux centrosomes, chacun avec une paire de centrioles et des liens soigneusement régulés qui les maintiennent dans la bonne configuration. Dans les myoblastes déficients en WDR62, de nombreuses cellules présentaient au contraire des centrioles en excès et plusieurs centrosomes, accompagnés de schémas anormaux de cohésion entre eux. Ce type de confusion structurelle perturbe la formation ordonnée du fuseau séparant les chromosomes, ralentissant ou compromettant la division cellulaire. L’équipe a également montré que WDR62 aide à recruter une autre protéine du centrosome, CEP170, lors de la transition du myoblaste divisé vers la cellule musculaire précoce fusionnée. Ensemble, ces fonctions suggèrent que WDR62 fait partie intégrante de la machinerie qui préserve l’intégrité du centrosome pendant la prolifération et aide à réorganiser cette machinerie lorsque les cellules s’engagent à devenir muscle.
Ce que cela signifie pour la santé musculaire
Pour un non-spécialiste, le message clé est que construire et réparer le muscle ne consiste pas seulement à faire croître des cellules ; il s’agit de préserver un stock sain de cellules précurseures et de décider exactement quand elles doivent cesser de se diviser et commencer à mûrir. WDR62 agit comme un responsable du contrôle qualité aux centres de construction internes de la cellule, en veillant à ce que les myoblastes se divisent proprement et dans la bonne orientation avant de fusionner en fibres. Lorsqu’elle manque, les myoblastes se divisent de manière moins fiable et s’engagent trop tôt vers une identité musculaire, conduisant avec le temps à des muscles plus petits et à une réserve de cellules réparatrices réduite. Comprendre cet équilibre pourrait éventuellement orienter des stratégies pour traiter les affections de fonte musculaire, où préserver ou restaurer le réservoir de cellules souches musculaires est tout aussi important qu’encourager leur croissance.
Citation: Ho, U.Y., Shohayeb, B., Kamei, H. et al. WDR62 is required for proper proliferation and early differentiation of skeletal myoblasts. Commun Biol 9, 259 (2026). https://doi.org/10.1038/s42003-026-09537-7
Mots-clés: cellules souches musculaires, différenciation des myoblastes, intégrité du centrosome, WDR62, régénération du muscle squelettique