Clear Sky Science · fr
La réversion fœtale depuis des lignées diverses soutient le réservoir de cellules souches intestinales et confère une résilience au stress
Comment l’intestin se répare sous le feu
L’épithélium intestinal est l’un des tissus les plus actifs de votre corps. Il digère les aliments, absorbe les nutriments et protège contre les microbes, tout en se renouvelant tous les quelques jours. Cet article explore comment cette surface fragile survit à des assauts sévères — de l’inflammation à la chimiothérapie — en réinitialisant temporairement des cellules vers un état plus fœtal et plus souple qui aide l’intestin à se réparer et à résister aux dommages.
La chaîne de production quotidienne de l’intestin
Dans un intestin sain, un groupe spécialisé de cellules appelées cellules colonnaires à la base des cryptes (CBC) occupe le fond de petits puits nommés cryptes. Ces cellules de type souche se divisent constamment et envoient leurs descendants vers le haut, en direction des villosités qui bordent la lumière intestinale. Au cours de ce trajet, les cellules mûrissent en rôles différents, comme les entérocytes absorbants qui captent les nutriments, ou les cellules sécrétoires qui produisent du mucus et des composés antimicrobiens. Dans des conditions normales, ce flux haut-bas maintient le renouvellement et l’ordre de l’épithélium intestinal.
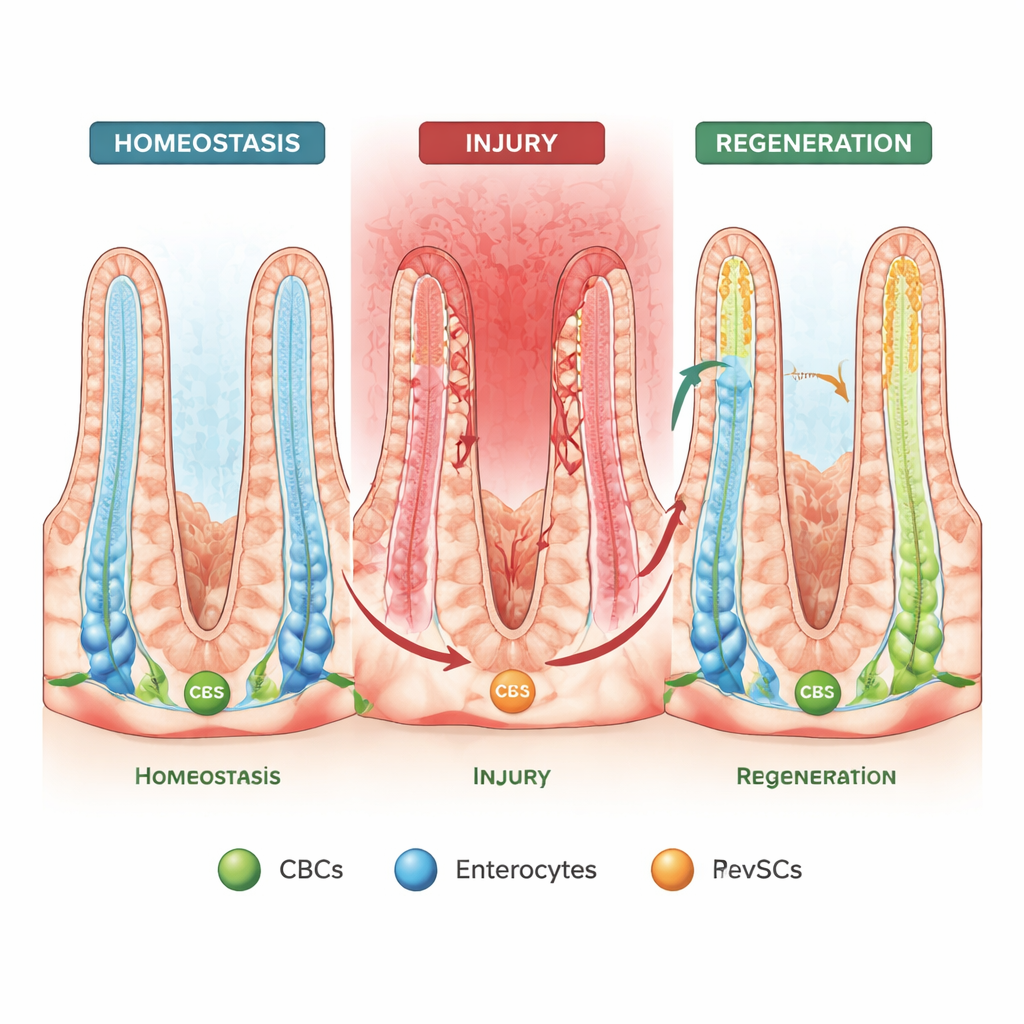
Des cellules capables d’inverser la chaîne de production
Lorsque l’épithélium est endommagé et que les CBC disparaissent, des travaux antérieurs ont montré que certaines cellules matures peuvent « remonter » la crypte et retrouver des capacités de type souche, un comportement qualifié de plasticité spatiale. Un deuxième phénomène, plus récent, est la « réversion fœtale », où les cellules adoptent un programme d’expression génique rappelant l’intestin en développement. Dans cette étude, les auteurs relient ces deux idées en utilisant des organoïdes (mini-intestins), du séquençage ARN unicellulaire et le traçage de lignée chez la souris. Ils identifient une population spéciale de type fœtal, nommée cellules souches de réveil (revSCs), qui peut émerger à la fois des CBC et d’entérocytes absorbants ordinaires, puis régénérer l’ensemble des types cellulaires intestinaux.
Les mini-intestins révèlent une flexibilité cachée
Pour observer ces changements, l’équipe a cultivé des organoïdes intestinaux de souris et d’humain dans deux gels différents. Dans la Matrigel, les organoïdes se comportaient comme un tissu adulte normal, riche en CBC et en cellules matures. Dans un gel de collagène, en revanche, les organoïdes étaient dominés par des cellules de type revSC avec un profil génique fœtal. Des analyses unicellulaires ont montré que les revSCs pouvaient être retracées le long de deux parcours principaux : à partir des CBC classiques et à partir des entérocytes absorbants. Des expériences de tri ont confirmé que les CBC ont la capacité la plus élevée de se convertir en revSCs, mais des cellules encore plus matures pouvaient aussi le faire si elles étaient placées dans l’environnement approprié. De manière cruciale, des revSCs purifiées pouvaient être replacées dans la Matrigel et régénéraient alors des CBC et toutes les lignées intestinales majeures, prouvant que l’état de type fœtal est à la fois réversible et pleinement fonctionnel.
Les cellules de la villosité et les blessures in vivo
L’étude va plus loin en demandant si cette flexibilité apparaît en dehors du laboratoire. Les chercheurs ont marqué des entérocytes dans les villosités de souris puis ont soit cultivé des fragments de villosités, soit exposé les animaux à un médicament chimiothérapeutique toxique pour l’intestin, le 5-fluorouracile (5-FU). En collagène, des fragments de villosités — normalement considérés comme pauvres en cellules souches — ont formé de nouveaux organoïdes affichant les caractéristiques des revSCs, puis ont retrouvé des marqueurs de CBC lorsqu’on les a replacés en conditions standard. Lorsqu’ils ont été transplantés dans des modèles de colite, ces organoïdes « dérivés de villosités » ont reconstruit un épithélium intestinal sain. Chez des souris vivantes traitées au 5-FU, les entérocytes marqués ont commencé à exprimer des marqueurs de revSCs, puis sont réapparus plus tard sous forme de longues bandes clonales incluant de nouveaux CBC à la base des cryptes, confirmant que des cellules matures étaient intervenues pour reconstituer le pool de cellules souches.
Des équipes de réparation résistantes au stress
Pourquoi emprunter cette voie fœtale temporaire ? Les auteurs montrent que les revSCs résistent beaucoup mieux au stress. Lorsque les organoïdes ont été mis au défi par le 5-FU, ceux en Matrigel ont rétréci et présenté des programmes géniques étendus liés aux dommages de l’ADN et à une prolifération frénétique. Les organoïdes cultivés en collagène, riches en revSCs, ont au contraire continué de croître et montré une réponse plus calme et ciblée. Les analyses géniques ont révélé une activité plus élevée des systèmes antioxydants, des protéines anti-apoptotiques et des chaperons de choc thermique — des boucliers moléculaires qui aident les cellules à survivre à l’inflammation et aux agressions toxiques. Des schémas similaires ont été observés chez la souris et chez l’humain, et les mêmes gènes de revSC sont élevés dans des intestins humains enflammés.
Ce que cela signifie pour les maladies intestinales et les thérapies
Pour un non-spécialiste, la conclusion est que l’épithélium intestinal possède un plan de secours d’urgence intégré. Lorsque l’inflammation ou les médicaments menacent ses cellules souches habituelles, à la fois les cellules souches et les cellules absorbantes ordinaires peuvent temporairement revenir à un état fœtal, résistant au stress, de type revSC. À partir de là, elles peuvent recréer le compartiment normal de cellules souches et reconstruire le tissu. Ce travail unifie deux concepts de régénération — la plasticité spatiale et la réversion fœtale — en une hiérarchie de réparation unique, et suggère que tirer parti soigneusement de ce programme fœtal flexible pourrait améliorer les traitements de pathologies telles que la maladie inflammatoire de l’intestin et le cancer colorectal, tout en avertissant qu’une réversion mal contrôlée pourrait favoriser la croissance tumorale.
Citation: Kirino, S., Uefune, F., Miyake, K. et al. Fetal reversion from diverse lineages sustains the intestinal stem cell pool and confers stress resilience. Commun Biol 9, 255 (2026). https://doi.org/10.1038/s42003-026-09533-x
Mots-clés: cellules souches intestinales, régénération tissulaire, plasticité cellulaire, maladie inflammatoire de l’intestin, organoïdes