Clear Sky Science · fr
La fluvastatine supprime l’initiation et la progression du cancer du sein en ciblant CYP4Z1
Pourquoi un médicament contre le cholestérol compte pour le cancer du sein
De nombreuses femmes traitées pour un cancer du sein développent des anomalies des lipides sanguins et restent exposées au risque de récidive ou de dissémination. Cette étude examine une idée intrigante : une pilule courante pour réduire le cholestérol, la fluvastatine, pourrait-elle être repositionnée pour ralentir ou prévenir le cancer du sein en neutralisant une protéine qui alimente des cellules tumorales particulièrement dangereuses, de type cellulaire souche ?
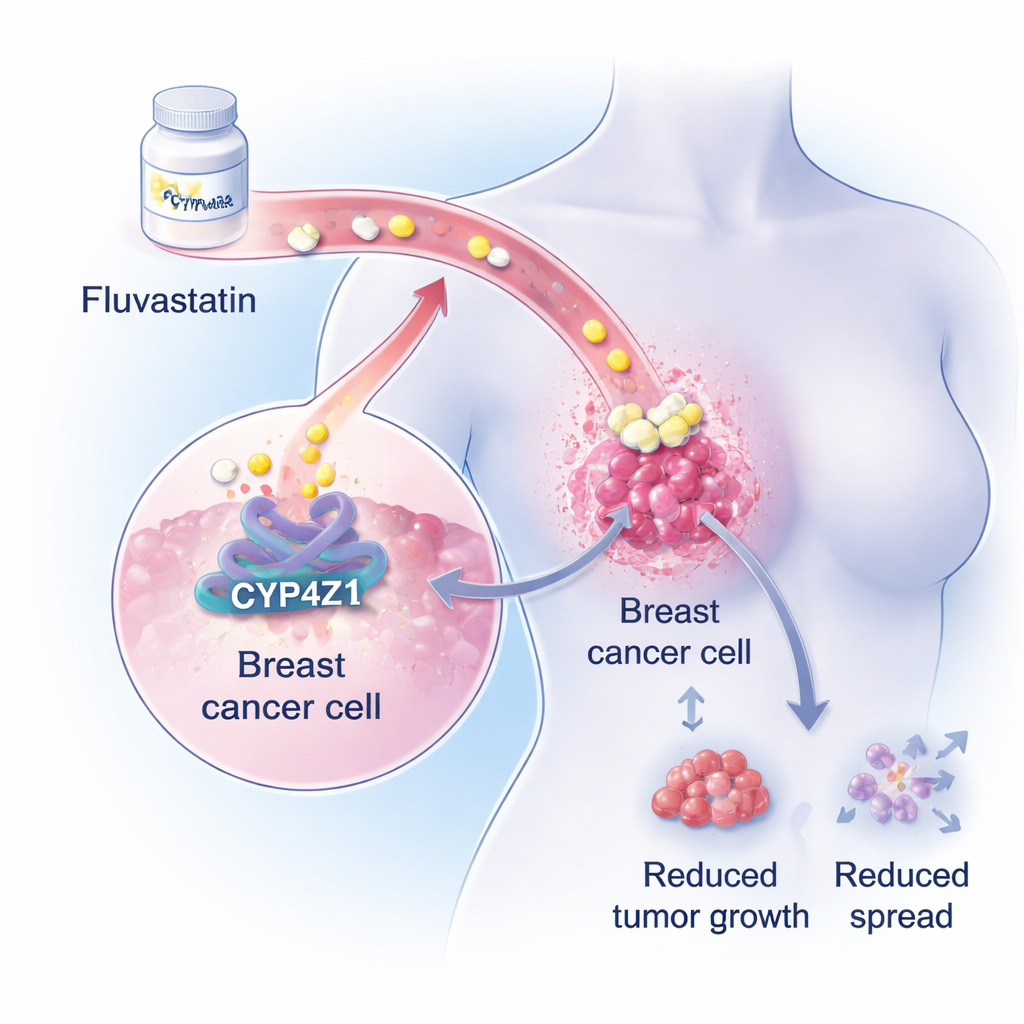
Un moteur caché à l’intérieur des tumeurs mammaires
Les chercheurs se concentrent sur une protéine peu connue nommée CYP4Z1, présente à des niveaux élevés dans les cellules du cancer du sein mais pas dans le tissu mammaire sain. Des travaux antérieurs montraient que CYP4Z1 aide les cellules cancéreuses à adopter des caractéristiques de cellules souches — capables de s’auto-renouveler indéfiniment, de résister à la chimiothérapie et de relancer des tumeurs après traitement. Dans de larges analyses génétiques et biochimiques, l’équipe montre maintenant qu’une activité excessive de CYP4Z1 stimule fortement les voies de synthèse lipidique dans les cellules cancéreuses mammaires, en particulier la production de triglycérides, une graisse de stockage majeure. Parce que de nombreuses patientes atteintes du cancer du sein développent déjà des perturbations lipidiques pendant la chimiothérapie, ce rôle promoteur des graisses suggère une ouverture pour des médicaments hypolipémiants existants.
Repositionner la fluvastatine, de la santé cardiaque aux soins du cancer
Pour tester cette idée, les scientifiques ont criblé une petite bibliothèque de 23 médicaments approuvés par la FDA utilisés pour abaisser les lipides sanguins. La fluvastatine, une statine largement prescrite pour l’hypercholestérolémie, est apparue comme remarquable : elle bloquait directement l’activité enzymatique de CYP4Z1 de manière dépendante de la dose. À des concentrations beaucoup moins toxiques pour les cellules mammaires normales que pour les cellules cancéreuses, la fluvastatine réduisait fortement des marqueurs clés de « stemness », la capacité des cellules cancéreuses du sein à former des « spheres tumorales » flottantes et leur aptitude à migrer et envahir des barrières de type tissulaire dans des essais in vitro. Elle rendait aussi les cellules tumorales plus sensibles au médicament de chimiothérapie adriamycine, suggérant qu’elle pourrait renforcer les traitements existants.
Mettre le médicament à l’épreuve chez l’animal
L’équipe a ensuite évalué la fluvastatine dans des modèles murins. Chez des souris implantées avec des cellules humaines de cancer du sein, des traitements périodiques par fluvastatine ont ralenti la croissance tumorale, abaissé les niveaux d’un marqueur de stemness (ALDH1A1) et du marqueur de division cellulaire Ki67 dans les tumeurs, et réduit le nombre de nodules métastatiques apparus dans les poumons. De manière importante, les souris recevant de la fluvastatine ont maintenu leur poids corporel et n’ont montré aucune anomalie majeure du sang ou de la moelle osseuse, soutenant un profil de sécurité favorable à la dose testée. Dans un modèle génétique plus réaliste — des souris génétiquement modifiées pour développer des tumeurs mammaires induites par un gène cancérogène — les chercheurs ont par ailleurs introduit CYP4Z1 humain dans le tissu mammaire. Ces souris ont développé davantage de lésions précancéreuses et cancéreuses, et plus de métastases hépatiques et pulmonaires, que les témoins. Le traitement par fluvastatine a réduit de manière substantielle à la fois le nombre de lésions mammaires et de métastases à distance, en particulier chez les souris portant le gène CYP4Z1 supplémentaire.
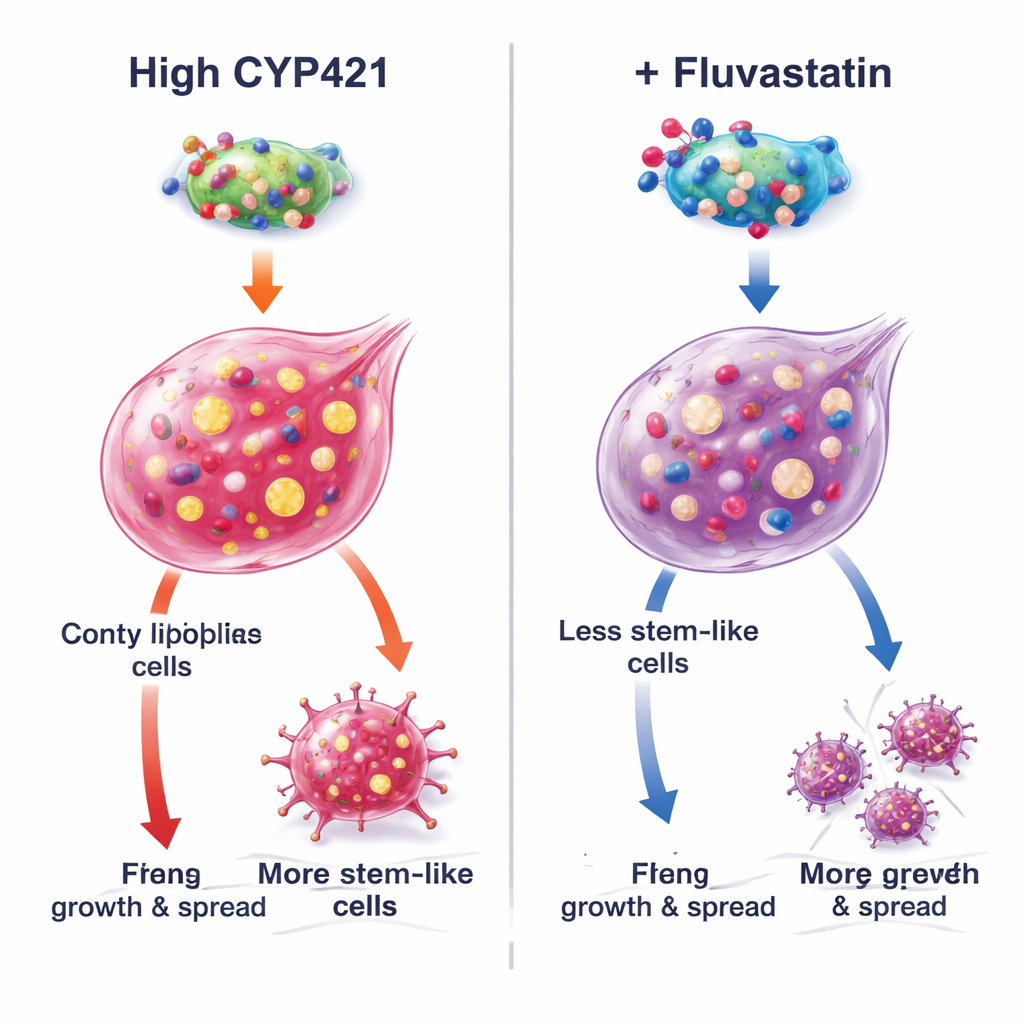
Comment la fluvastatine désarme une protéine pro-cancer
Pour comprendre le mécanisme, les auteurs ont combiné modélisation informatique et ingénierie protéique précise. Ils ont prédit que la fluvastatine s’insère dans le site actif de CYP4Z1 au niveau de trois acides aminés critiques (Lys109, Pro444 et Arg450). Lorsque ces sites ont été mutés, l’activité de CYP4Z1 a chuté et la fluvastatine n’a plus pu l’inhiber davantage, confirmant ces positions comme points d’ancrage. Dans des cellules dépourvues naturellement de CYP4Z1, l’introduction de la protéine normale augmentait la stemness et activait la signalisation pro-croissance PI3K/AKT, tandis que la fluvastatine renversait ces effets. Les versions mutées de CYP4Z1 étaient moins puissantes et moins sensibles au médicament. Des expériences supplémentaires ont montré que l’effet de la fluvastatine s’affaiblissait lorsque la production de triglycérides était artificiellement augmentée, ou lorsque CYP4Z1 était réduit par knockdown, soulignant que les effets les plus forts du médicament proviennent du blocage de cette protéine spécifique et de ses conséquences sur la synthèse lipidique plutôt que d’une induction de mort cellulaire par ferroptose dépendante du fer.
Ce que cela signifie pour les patientes
Dans l’ensemble, l’étude suggère que la fluvastatine, au-delà de son effet hypocholestérolémiant, peut freiner les stades les plus précoces et la dissémination ultérieure du cancer du sein dans des modèles expérimentaux en ciblant CYP4Z1, une protéine qui stimule le métabolisme lipidique et le comportement de type cellule souche dans les tumeurs. Comme la fluvastatine est déjà approuvée et que sa sécurité est bien caractérisée, ces résultats ouvrent une voie prometteuse vers des essais cliniques plus rapides en tant que thérapie adjuvante, en particulier chez les patientes dont les tumeurs expriment fortement CYP4Z1. Bien que des travaux supplémentaires soient nécessaires pour tester cette approche chez l’humain et pour identifier d’éventuelles cibles additionnelles du médicament, la recherche ouvre la possibilité d’intégrer un médicament cardiaque familier dans une nouvelle stratégie contre les cancers du sein agressifs et à risque élevé de récidive.
Citation: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Mots-clés: cancer du sein, fluvastatine, cellules souches cancéreuses, métabolisme des lipides, repositionnement de médicaments