Clear Sky Science · fr
miARNs différentiellement exprimés dans le cortex temporal de patients atteints de la maladie d’Alzheimer et leur association à la pathologie tau
Pourquoi ces petits interrupteurs cérébraux comptent en cas d’Alzheimer
La maladie d’Alzheimer prive progressivement les personnes de leur mémoire et de leur autonomie, et nous ne disposons toujours pas de traitements capables de l’arrêter ou de l’inverser. Cette étude examine certains des plus petits interrupteurs de régulation du cerveau — de courtes molécules d’ARN appelées microARNs — qui contribuent à décider quelles protéines les cellules produisent. En analysant des tissus cérébraux de personnes atteintes d’Alzheimer, les chercheurs ont cherché à savoir si des modifications de ces microARNs s’associent à une caractéristique clé de la maladie : l’accumulation et la propagation de la protéine tau anormale à l’intérieur des cellules cérébrales.
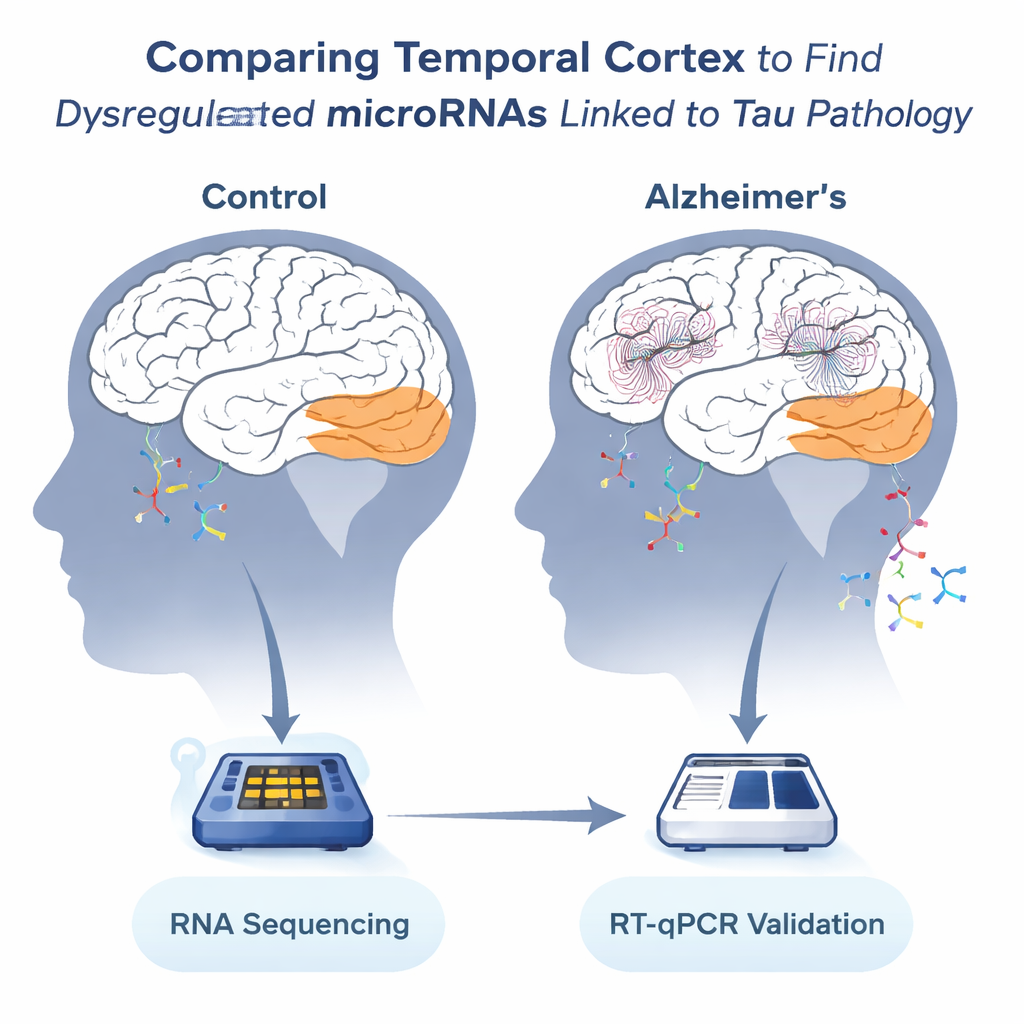
Examiner les messages dans une région cérébrale vulnérable
L’équipe s’est concentrée sur le cortex temporal, une région importante pour le langage et la mémoire fortement touchée dans la maladie d’Alzheimer. Après le décès, des échantillons de 36 individus — 13 sans Alzheimer et 23 atteints — ont été prélevés dans deux banques de cerveau européennes. Les scientifiques ont extrait l’ARN de ces tissus et utilisé le séquençage à haut débit pour recenser des centaines de microARNs différents. Parce que les tissus cérébraux se dégradent après la mort, ils ont soigneusement vérifié la qualité de l’ARN et sélectionné 19 échantillons présentant une intégrité acceptable pour l’analyse la plus détaillée, puis utilisé les 36 échantillons pour confirmer leurs résultats principaux.
Découvrir une signature de microARNs liée à l’Alzheimer
Parmi 449 microARNs détectés, 13 se sont distingués comme systématiquement altérés dans le cortex temporal des malades d’Alzheimer. Huit étaient réduits et cinq augmentés par rapport aux cerveaux témoins. Plusieurs des signaux les plus marqués impliquaient des microARNs déjà suspectés d’avoir un rôle dans l’Alzheimer : miR-129-5p, miR-132-3p et miR-146b-5p étaient tous plus bas, tandis que miR-151a-5p était plus élevé. Ces molécules sont abondantes dans le cerveau et régulent des réseaux de gènes impliqués dans la santé neuronale. En utilisant une seconde technique plus ciblée (RT-qPCR), les auteurs ont validé que ces mêmes microARNs changeaient dans le même sens, même en incluant des échantillons de moindre qualité, renforçant la confiance dans la réalité du schéma observé.
Relier les petits interrupteurs à l’aggravation des enchevêtrements tau
La sévérité de l’Alzheimer dans le cerveau est souvent classée par stade de Braak, qui reflète l’étendue de la propagation des enchevêtrements de tau dans différentes régions. Les chercheurs ont constaté que les niveaux de miR-129-5p, miR-132-3p et miR-146b-5p déclinaient régulièrement avec l’augmentation du stade de Braak, tandis que miR-151a-5p avait tendance à monter. Ils ont également mesuré directement dans les mêmes échantillons une forme fortement phosphorylée de tau, susceptible de former des enchevêtrements. Les cerveaux présentant davantage de cette tau anormale montraient le même profil : moins de miR-129-5p, miR-132-3p et miR-146b-5p, et plus de miR-151a-5p. Autrement dit, les modifications des microARNs suivaient à la fois la stadification microscopique et les signes biochimiques de la pathologie tau, suggérant qu’elles sont étroitement liées au processus pathologique plutôt que de simples passagers aléatoires.
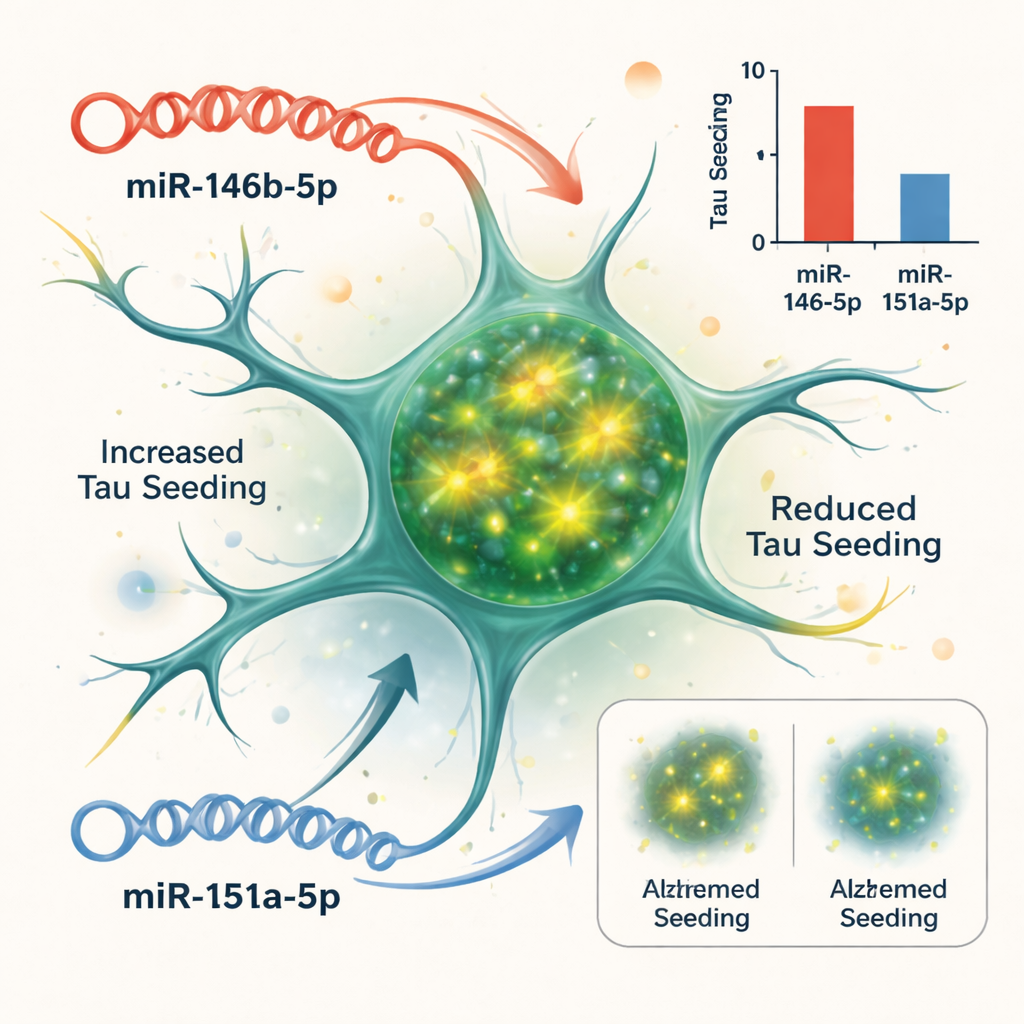
Tester la causalité dans un modèle cellulaire
La corrélation n’implique pas la causalité, aussi l’équipe a-t-elle eu recours à un système cellulaire qui rend compte de la facilité avec laquelle la tau peut « ensemencer » de nouveaux agrégats. Ils ont utilisé des cellules biosenseures conçues pour s’illuminer lorsque des fibres de tau se forment à l’intérieur d’elles. Lorsqu’ils ont ajouté du matériel riche en tau issu de cerveaux d’Alzheimer, les cellules produisaient un signal fluorescent fort. En augmentant ou en bloquant des microARNs spécifiques dans ces cellules, les chercheurs ont pu voir lesquels modifiaient cet ensemencement de la tau. Deux microARNs se sont démarqués : l’augmentation de miR-146b-5p aggravait l’ensemencement de la tau, tandis que son blocage le réduisait ; à l’inverse, l’augmentation de miR-151a-5p atténuait l’ensemencement de la tau, alors que son inhibition le rendait plus robuste. Les autres microARNs testés ont eu peu d’effet dans cet essai.
Ce que cela peut signifier pour le diagnostic et le traitement futurs
Pour comprendre ce que ces microARNs pourraient faire, les auteurs ont utilisé des outils informatiques pour cartographier leurs cibles géniques prédictes sur des voies biologiques connues. Les microARNs régulés à la baisse — en particulier miR-129-5p, miR-132-3p et miR-146b-5p — étaient liés à des réseaux impliqués dans la survie neuronale, la signalisation chimique aux synapses et des voies associées à l’Alzheimer. Cela suggère que la perte de leur influence régulatrice normale pourrait perturber simultanément plusieurs systèmes protecteurs, tandis que l’augmentation de miR-151a-5p pourrait représenter une tentative tardive et partielle du cerveau pour contrer l’agrégation de la tau. Bien que ce travail repose sur des tissus post-mortem et des modèles cellulaires simplifiés, il renforce l’idée que des microARNs spécifiques reflètent et modulent la pathologie tau. À long terme, mesurer ces molécules dans le liquide céphalo-rachidien ou le sang pourrait aider à suivre l’évolution de la maladie, et ajuster précisément leurs niveaux dans le cerveau pourrait offrir une nouvelle voie pour ralentir ou prévenir la propagation de la tau toxique.
Citation: Nagaraj, S., Quintanilla-Sánchez, C., Ando, K. et al. Differentially expressed miRNAs in the temporal cortex of Alzheimer’s disease patients and their association to tau pathology. Commun Biol 9, 253 (2026). https://doi.org/10.1038/s42003-026-09530-0
Mots-clés: Maladie d’Alzheimer, microARN, pathologie tau, cortex temporal, neurodégénérescence