Clear Sky Science · fr
Le blocage ciblé de l’épissage des gènes peut déréguler des microARN primaires intégrés dans des introns
Messages cachés au sein de nos gènes
De nombreuses nouvelles thérapies géniques agissent en modifiant les messages ARN de nos cellules, mais ces ARN contiennent souvent des « notes en marge » que les chercheurs commencent à peine à comprendre. Cet article montre que des médicaments conçus pour corriger un épissage défectueux peuvent, par accident, augmenter de petites molécules régulatrices enfouies dans les introns — les séquences non codantes entre les segments de gène — avec des effets inattendus sur le câblage et le développement du cerveau.
Des thérapies géniques qui réécrivent l’ARN
Les oligonucléotides antisens, ou ASO, sont de courts fragments synthétiques d’acide nucléique qui se fixent à l’ARN et modifient sa lecture ou son traitement. Plusieurs ASO sont déjà testés ou utilisés pour des maladies génétiques rares, en particulier celles causées par des défauts d’épissage — l’étape qui recoud les segments codants d’un gène. La plupart des tests de sécurité vérifient si un ASO restaure la protéine adéquate et évite des effets secondaires évidents. Mais de nombreux gènes portent aussi des ARN non codants, y compris des microARN, à l’intérieur de leurs introns. Ces petites molécules peuvent fortement moduler l’activité des gènes, et jusqu’à la moitié des microARN connus chez les vertébrés proviennent d’introns. L’étude examine la question suivante : que deviennent ces microARN intégrés lorsque l’on force des changements d’épissage avec des ASO ?
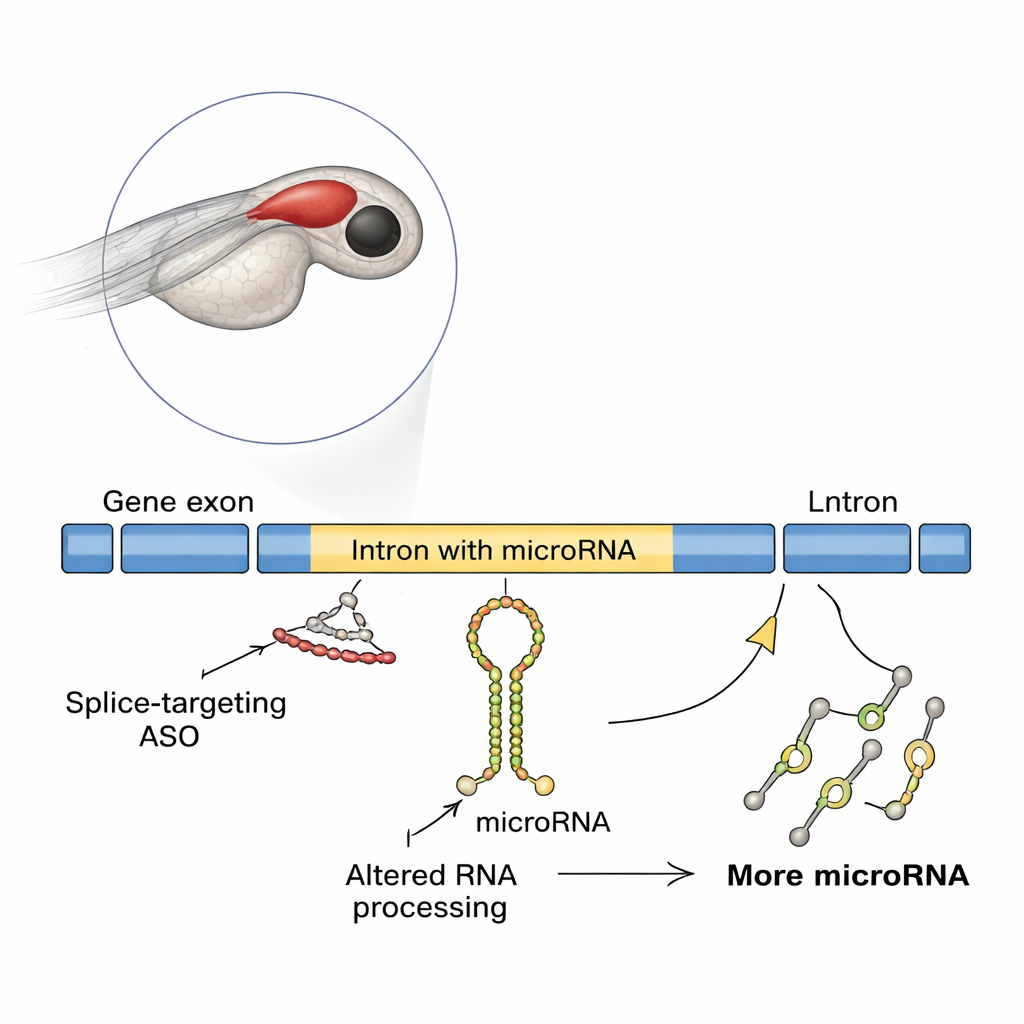
Un effet surprenant dans le cerveau de poissons en développement
Les chercheurs ont utilisé le poisson zèbre, un modèle vertébré populaire dont les embryons transparents facilitent le suivi du développement du cerveau. Ils se sont concentrés sur un gène appelé slit3, qui guide les fibres nerveuses et contient un microARN nommé mir-218a-1 dans l’un de ses introns. Lorsque l’équipe a bloqué le démarrage de la traduction de slit3, le développement des axones hypophysaires sécréteurs d’hormones semblait normal. Mais lorsqu’ils ont utilisé un autre ASO qui bloquait l’épissage à un site d’épissage spécifique de slit3, les axones qui devaient se projeter vers l’hypophyse postérieure étaient fortement réduits, alors même que le nombre de neurones producteurs d’ocytocine restait le même. Des analyses moléculaires ont montré que cet ASO bloquant l’épissage provoquait la rétention de l’intron dans l’ARN du gène, augmentant de manière inattendue les niveaux du transcrit de slit3, de son long intron et du transcrit primaire intronique de mir-218a-1.
Le microARN, et non la perte de protéine, cause les défauts
Pour déterminer l’origine du problème axonal, les auteurs ont comparé plusieurs scénarios. Bloquer uniquement le mir-218a-1 mature n’a pas modifié les niveaux de slit3, et un ASO distinct ciblant un autre site d’épissage proche du microARN n’a pas entraîné de défauts axonaux ni d’augmentation de mir-218a-1. Surtout, lorsque l’ASO bloquant l’épissage de slit3 a été combiné à un ASO neutralisant mir-218a-1, le câblage axonal s’est largement rétabli. De même, chez des poissons zèbre génétiquement dépourvus de mir-218a-1, le même ASO bloquant l’épissage de slit3 n’a plus provoqué de défauts axonaux, tandis que l’injection d’un mimic synthétique de mir-218a pouvait reproduire le phénotype chez des poissons normaux. Ces expériences indiquent qu’une élévation du microARN intronique — plutôt qu’une protéine Slit3 tronquée — est le principal moteur de la perturbation développementale.
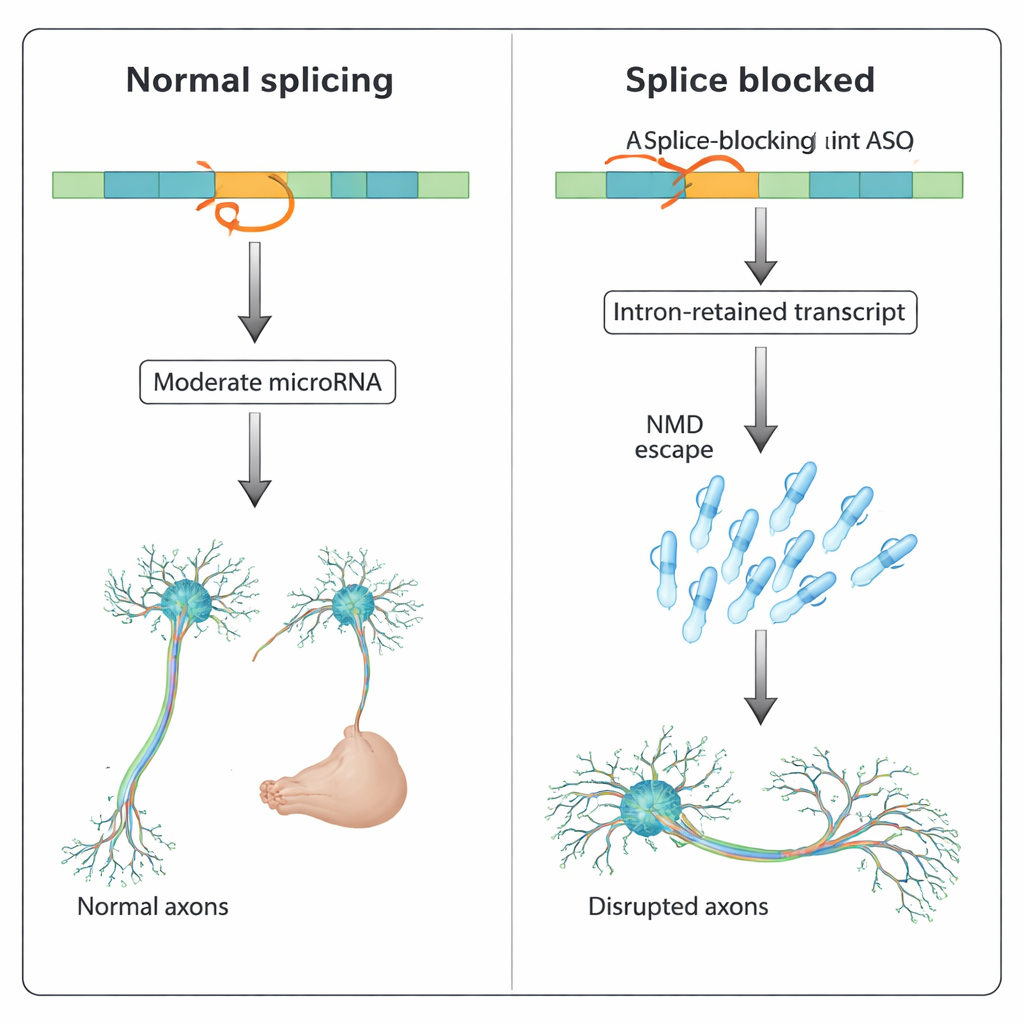
Un schéma plus large affectant plusieurs gènes
L’équipe s’est ensuite demandé si cet effet était unique à slit3. Ils ont scruté le génome du poisson zèbre et trouvé des dizaines de gènes codant pour des protéines qui hébergent des microARN introniques, beaucoup étant impliqués dans le développement et la signalisation. Deux de ces gènes, pank2 et dnm2a, avaient déjà montré de graves problèmes développementaux lorsque leur épissage était bloqué par des ASO, notamment une accumulation de liquide cérébral, un gonflement cardiaque et des déformations corporelles — des problèmes que les knockouts génétiques des mêmes gènes n’avaient pas reproduits. Dans cette étude, la co‑injection d’ASO ciblant spécifiquement les microARN introniques mir-103 (dans pank2) ou mir-199-5p (dans dnm2a) a partiellement sauvé ces phénotypes induits par les ASO. Dans certains cas, le blocage du microARN a également restauré l’expression du gène hôte, tandis que dans d’autres non, ce qui suggère qu’une augmentation de l’activité microARN peut être nocive même lorsque les changements globaux de niveaux sont modestes.
Ce que cela signifie pour les traitements futurs
Les résultats montrent que les ASO ciblant l’épissage peuvent faire plus que provoquer un saut d’exons ou une rétention d’intron : ils peuvent stabiliser des transcrits avec intron retenu qui échappent au contrôle qualité cellulaire et augmenter les microARN primaires introniques, lesquels désorganisent ensuite des réseaux de gènes cibles. Dans les neurones en développement, une telle activité microARN incontrôlée peut déformer la croissance des axones et la connectivité. Pour les développeurs de médicaments, cela signifie que des phénotypes inhabituels ou « hors‑cible » observés chez l’animal ne proviennent pas toujours de voies génériques de toxicité comme l’activation de p53, mais d’effets non voulus sur des ARN introniques cachés. Comparer soigneusement des ASO bloquant la traduction et des ASO bloquant l’épissage, et surveiller l’expression des microARN introniques, pourrait aider à détecter ces risques tôt et à affiner la conception des ASO avant qu’ils n’atteignent les patients.
Citation: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Mots-clés: oligonucléotides antisens, microARN, épissage de l’ARN, développement du poisson zèbre, sécurité des thérapies géniques