Clear Sky Science · fr
Le nimbolide atténue le SDRA et la colite ulcéreuse en perturbant l’activation de l’inflammasome NLRP3
Pourquoi il est important de maîtriser une inflammation incontrôlée
De nombreuses maladies graves, allant de l’insuffisance pulmonaire potentiellement mortelle aux affections intestinales douloureuses, ne sont pas seulement causées par des microbes ou des blessures : elles résultent aussi d’une réponse immunitaire excessive. Cette étude examine si un composé naturel appelé nimbolide, extrait de l’arbre neem, peut servir de « frein » précis sur une puissante machinerie inflammatoire à l’intérieur de nos cellules immunitaires, ouvrant potentiellement une voie plus sûre pour traiter des affections telles que le syndrome de détresse respiratoire aiguë (SDRA) et la colite ulcéreuse.
Une alarme problématique au sein des cellules immunitaires
Au cœur de ce récit se trouve un système d’alarme moléculaire appelé inflammasome NLRP3. Lorsque les cellules immunitaires détectent un danger — signaux d’infection, tissus endommagés ou cristaux — l’inflammasome peut se monter comme une structure en trois parties : le senseur NLRP3, l’adaptateur ASC et l’enzyme Caspase‑1. Une fois assemblé, ce complexe active des messagers puissants tels que IL‑1β et IL‑18 et peut déclencher une forme inflammatoire de mort cellulaire appelée pyroptose. Si cette réponse aide à éliminer les menaces, son sur‑activation contribue à des maladies chroniques et aiguës, notamment l’arthrite, des complications du diabète, la maladie d’Alzheimer, le SDRA et les maladies inflammatoires intestinales. Les industriels ont tenté de maîtriser NLRP3 avec des composés synthétiques, mais de nombreux candidats ont échoué en raison de toxicité, d’effets indésirables ou d’un mauvais comportement pharmacologique, laissant un besoin clair d’inhibiteurs plus sûrs et plus sélectifs.
Découverte d’un inhibiteur végétal puissant
Les chercheurs ont criblé 126 composés naturels pour identifier ceux qui bloquaient le mieux la libération d’IL‑1β par des cellules immunitaires de souris. Le nimbolide est ressorti comme particulièrement efficace, réduisant la sécrétion d’IL‑1β de plus de 80 % aux doses testées. Des expériences complémentaires ont montré que le nimbolide réduisait fortement l’activation de la Caspase‑1, la libération d’IL‑1β et la pyroptose dans des macrophages dérivés de la moelle osseuse de souris, avec une puissance similaire à celle d’un médicament de référence appelé MCC950. Fait important, le nimbolide n’affectait pas la libération d’autres médiateurs immunitaires tels que l’IL‑6, ce qui suggère une action ciblée plutôt qu’une suppression générale de l’immunité. Testé contre différents stimuli activant NLRP3 — par exemple l’ATP, la nigéricine, les cristaux d’alum et l’imiquimod — le nimbolide a réduit de façon constante l’activité de l’inflammasome, y compris dans des cellules humaines THP‑1. En revanche, il n’inhibait pas deux inflammasomes apparentés, AIM2 et NLRC4, ce qui souligne sa spécificité pour NLRP3.
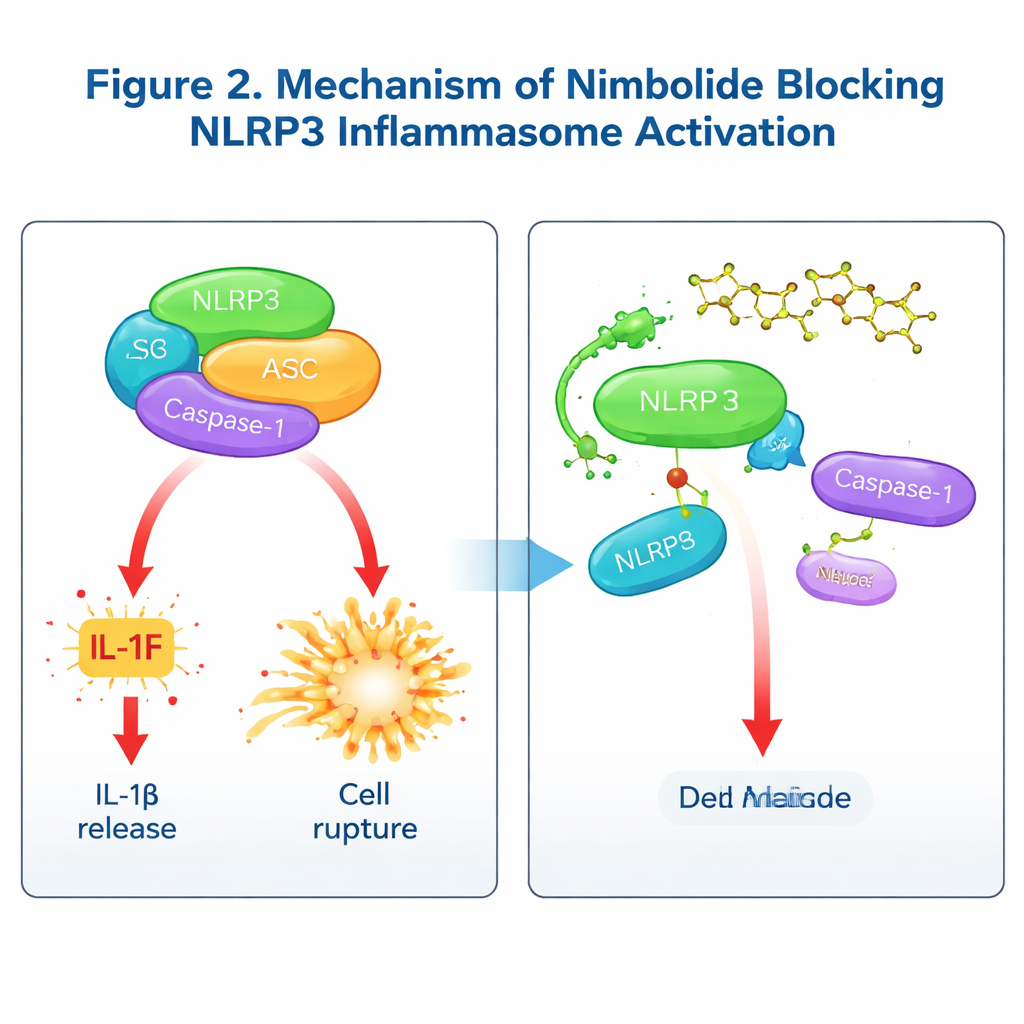
Comment le nimbolide bloque la machine inflammatoire
Pour comprendre le mode d’action du nimbolide, l’équipe a cherché à savoir s’il interfère avec les premières étapes de « priming » contrôlées par la voie NF‑κB, ou avec les étapes ultérieures où l’inflammasome s’assemble physiquement. Un traitement à court terme administré après le priming a laissé intacts les principaux signaux et l’expression génique du priming, tout en réduisant IL‑1β et l’activation de la Caspase‑1, montrant que le nimbolide agit principalement sur l’étape d’assemblage. Des tests biochimiques détaillés ont révélé que le nimbolide n’altère pas les flux de potassium ou de calcium, les dommages mitochondriaux, ni l’interaction de NLRP3 avec sa protéine auxiliaire NEK7. En revanche, il perturbe la liaison cruciale entre NLRP3 et ASC, réduit l’agrégation d’ASC en « specks » et empêche NLRP3 de former des oligomères de haut ordre. À l’aide d’essais de liaison et de modélisation moléculaire, les auteurs ont montré que le nimbolide se fixe directement sur la région NACHT de NLRP3 à un acide aminé précis, la Lys565. Quand ce site est muté, le nimbolide ne protège plus NLRP3 de la dégradation ni ne rompt son association avec ASC, confirmant la Lys565 comme point d’ancrage clé. Il est notable que, alors que d’autres médicaments ciblent souvent l’activité ATPase de NLRP3, le nimbolide bloque l’assemblage sans affecter l’utilisation d’ATP, offrant ainsi un mode d’action distinct.
Évaluation du nimbolide dans des modèles de maladie pulmonaire et intestinale
L’équipe a ensuite évalué si cet effet moléculaire se traduit par une protection réelle dans des modèles de maladie. Chez des souris exposées à une toxine bactérienne pour induire un SDRA, un traitement au nimbolide avant l’insulte a réduit les lésions tissulaires pulmonaires, l’accumulation de liquide et la fuite de protéines dans les espaces aériens. On observait moins de cellules immunitaires infiltrantes dans les poumons et des taux plus bas d’IL‑1β dans le tissu pulmonaire et le sang. Des bénéfices similaires ont été obtenus dans un modèle où la toxine était administrée directement dans les voies aériennes. Dans un modèle distinct de colite ulcéreuse, où les souris ingéraient un produit chimique blessant le côlon, le nimbolide a limité la perte de poids, amélioré la consistance des selles et les scores de saignement, préservé la longueur du côlon et réduit les signes microscopiques d’inflammation et d’érosion tissulaire, parallèlement à une baisse d’IL‑1β dans le côlon. De manière cruciale, chez des souris génétiquement modifiées dépourvues de NLRP3, la maladie était déjà moins sévère et le nimbolide n’apportait plus de bénéfice supplémentaire, ce qui souligne que ses effets protecteurs dépendent du blocage de NLRP3.
Ce que cela pourrait signifier pour les traitements futurs
Pour un public non spécialiste, la leçon centrale est que le nimbolide agit comme un frein intelligent sur l’un des commutateurs inflammatoires les plus puissants de l’organisme. En se fixant sur un site précis de NLRP3 et en empêchant l’inflammasome de s’assembler, il calme l’inflammation excessive dans les poumons et l’intestin sans désactiver largement les défenses immunitaires. Bien que le nimbolide doive encore être amélioré pour des aspects tels que la stabilité et la formulation avant de pouvoir devenir un médicament, ce travail le positionne comme un point de départ prometteur — et comme un modèle — pour concevoir la prochaine génération de traitements ciblant les maladies drivées par NLRP3, comme le SDRA et la colite ulcéreuse.
Citation: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Mots-clés: nimbolide, inflammasome NLRP3, inflammation, détresse respiratoire aiguë, colite ulcéreuse