Clear Sky Science · fr
MAT2A augmente la transcription de PARN via SRF pour accélérer la glycolyse et favoriser la progression maligne dans l’ostéosarcome
Pourquoi cette étude sur le cancer des os est importante
L’ostéosarcome est le cancer osseux le plus fréquent chez les enfants et les adolescents, et les traitements ont peu évolué depuis des décennies. De nombreux jeunes patients ont encore un pronostic réservé, en particulier lorsque la tumeur se propage ou résiste à la chimiothérapie. Cette étude met en lumière une protéine « interrupteur maître » jusque-là méconnue, MAT2A, qui aide les cellules d’ostéosarcome à proliférer, à réorienter leur utilisation d’énergie et à former des tumeurs agressives — et montre qu’un médicament ciblant MAT2A peut ralentir ou réduire ces tumeurs dans des modèles expérimentaux.
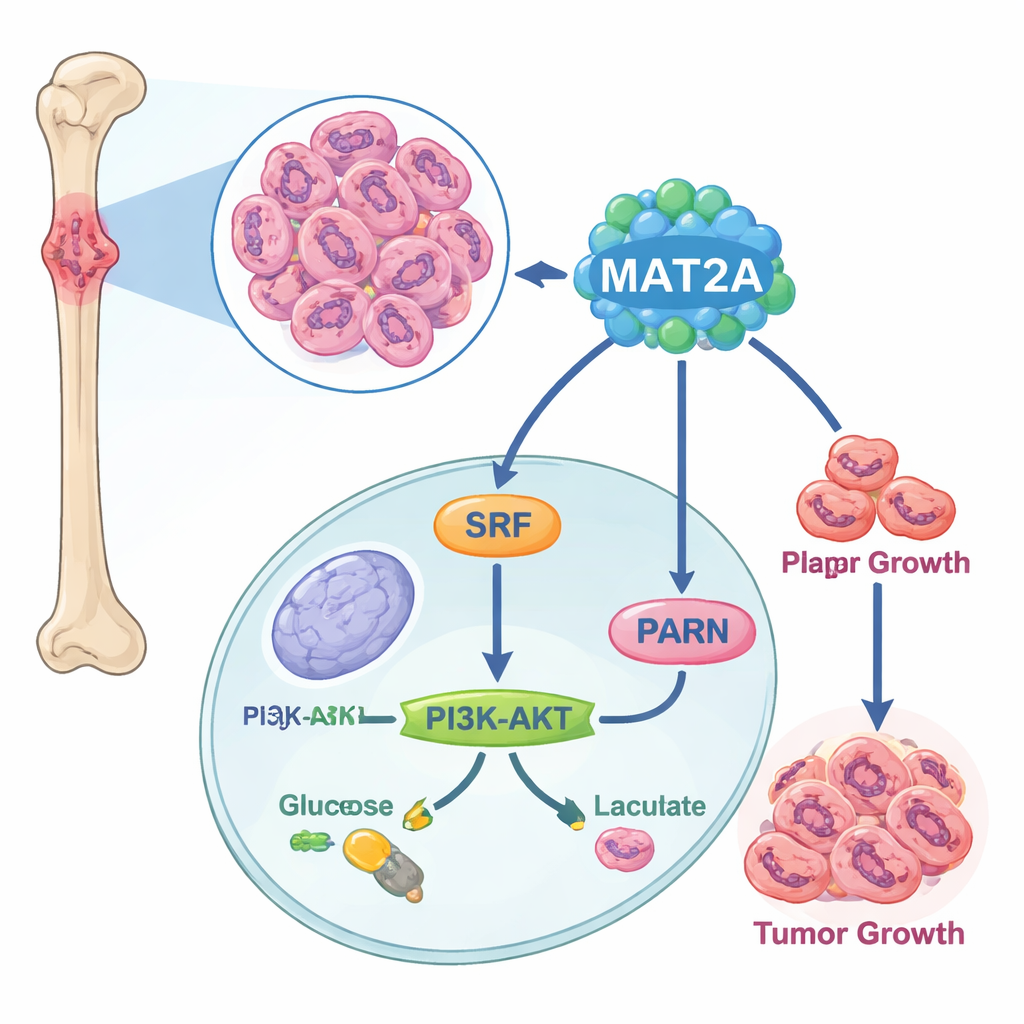
Un moteur caché à l’intérieur des cellules tumorales
Les chercheurs ont commencé par comparer des échantillons d’os cancéreux et du tissu osseux normal au niveau de la cellule unique. Ils ont constaté que le tissu d’ostéosarcome contenait plus de cellules contribuant à la tumeur et moins de cellules immunitaires, et qu’un gène en particulier — MAT2A — était anormalement actif dans les cellules cancéreuses. Des analyses de bases de données publiques et de lignées cellulaires en culture ont confirmé que les niveaux de MAT2A étaient beaucoup plus élevés dans l’ostéosarcome que dans les cellules osseuses saines, et que les patients présentant une expression élevée de MAT2A avaient tendance à présenter des maladies plus avancées et une atteinte des ganglions lymphatiques. Cela a placé MAT2A au centre de l’attention en tant que potentiel moteur de la maladie plutôt que simple spectateur.
Réduire MAT2A ralentit la croissance tumorale
Pour tester l’importance réelle de MAT2A dans le comportement tumoral, l’équipe a utilisé des outils génétiques pour diminuer l’expression de MAT2A dans des lignées cellulaires d’ostéosarcome. Lorsque MAT2A était silencieux, les cellules cancéreuses se divisaient plus lentement et étaient plus susceptibles d’entrer en apoptose. Chez des souris porteuses de ces cellules modifiées, les tumeurs croissaient beaucoup plus lentement et restaient nettement plus petites, alors que le poids corporel des animaux restait stable. Ces expériences montrent que les cellules d’ostéosarcome dépendent fortement de MAT2A pour leur survie et leur capacité à former des tumeurs.
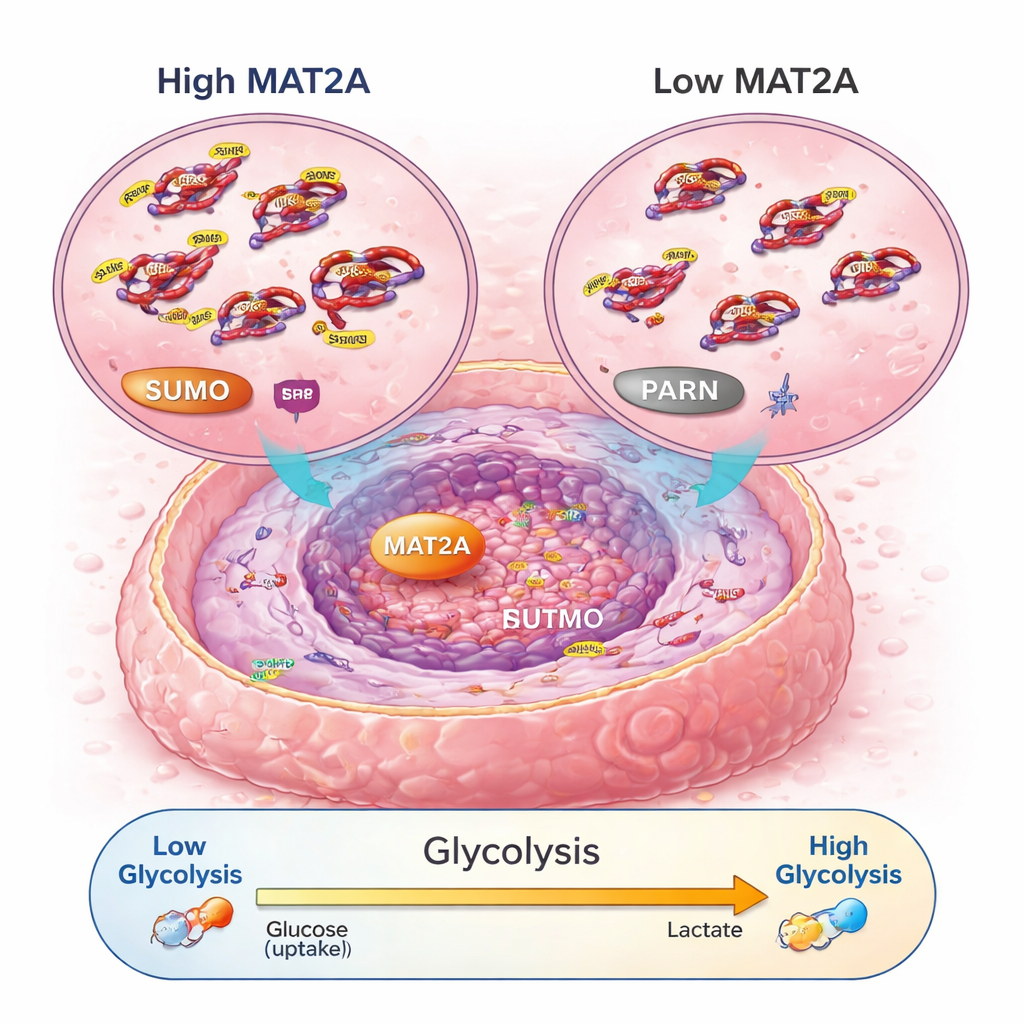
Une cascade de signalisation qui augmente l’utilisation du carburant cellulaire
En creusant davantage, les scientifiques ont découvert que MAT2A fait plus que son rôle métabolique habituel. Dans le noyau, il se lie à un facteur de transcription nommé SRF, contribuant à maintenir SRF stable et actif en favorisant une marque chimique appelée SUMO. En retour, SRF active un gène nommé PARN, qui stimule ensuite la voie bien connue PI3K–AKT et augmente la machinerie de la glycolyse aérobie — un mode rapide mais inefficace de production d’énergie que favorisent les cellules cancéreuses. Lorsque MAT2A était réduit, les cellules cancéreuses produisaient moins d’ATP (leur monnaie énergétique), captaient moins de glucose, fabriquaient moins d’acide lactique et retournaient vers une respiration plus calmee et dépendante de l’oxygène. Perturber PARN ou AKT annulait les effets pro-croissance et pro-glycolyse de MAT2A, confirmant que cette cascade — MAT2A vers SRF vers PARN vers PI3K–AKT — constitue un circuit clé d’énergie et de croissance dans l’ostéosarcome.
Un rôle non traditionnel et une cible pharmacologique
De manière frappante, une version de MAT2A dépourvue de son activité enzymatique normale soutenait malgré tout la stabilité de SRF et l’activation de PARN, ce qui signifie que ce rôle promoteur du cancer n’exige pas sa réaction chimique habituelle. MAT2A agit plutôt comme une échafaudage organisant d’autres protéines. Cela a des implications pratiques : les médicaments n’ont pas nécessairement besoin de bloquer son centre catalytique pour affaiblir les tumeurs. Les chercheurs ont testé un inhibiteur de petite molécule nommé FIDAS‑5, conçu pour cibler MAT2A, à la fois en culture cellulaire et chez la souris. Le traitement a réduit SRF nucléaire, abaissé PARN et la signalisation PI3K–AKT, atténué la glycolyse, ralenti la croissance cellulaire et induit la mort des cellules cancéreuses. Chez la souris, FIDAS‑5 a réduit ou ralenti les tumeurs sans perte de poids notable, suggérant des effets secondaires tolérables dans ce contexte.
Ce que cela signifie pour les patients et les thérapies futures
Pour un public non spécialiste, le message principal est que les cellules d’ostéosarcome dépendent de MAT2A pour maintenir leurs programmes de croissance et leur « moteur » de consommation du sucre à plein régime. En stabilisant des protéines de contrôle clés et en renforçant une chaîne de signaux, MAT2A aide les tumeurs à croître plus vite et à devenir plus agressives. Bloquer cette protéine — soit par des méthodes basées sur les gènes, soit par un médicament comme FIDAS‑5 — coupe cet appui, forçant les cellules cancéreuses à ralentir, à brûler moins frénétiquement leur énergie et finalement à mourir. Bien qu’il reste beaucoup de travail avant que de tels traitements n’atteignent la clinique, cette étude positionne MAT2A comme une nouvelle cible prometteuse dans la lutte contre le cancer des os, ouvrant une voie potentielle vers des thérapies plus précises et moins toxiques pour les jeunes patients.
Citation: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Mots-clés: ostéosarcome, MAT2A, métabolisme du cancer, voie PI3K AKT, thérapie ciblée