Clear Sky Science · fr
Analyse computationnelle de l’hétérogénéité des épitopes dans des immunomarquages à partir de séries de dilutions d’anticorps
Pourquoi la qualité du marquage par anticorps importe
Qu’il s’agisse de suivre des cellules cancéreuses ou de diagnostiquer des infections, la biologie moderne s’appuie largement sur des anticorps qui « éclairent » des molécules spécifiques à l’intérieur des cellules. Pourtant, de nombreux laboratoires font face à un problème récurrent : des marquages trop faibles, trop bruyants ou simplement trompeurs. Cet article présente une méthode informatique pratique pour extraire davantage d’information d’une série de dilutions d’anticorps classique, aidant les chercheurs à ajuster leurs marquages pour obtenir des images plus propres, des mesures plus fiables et même de nouvelles façons de marquer plusieurs cibles dans un seul canal de couleur. 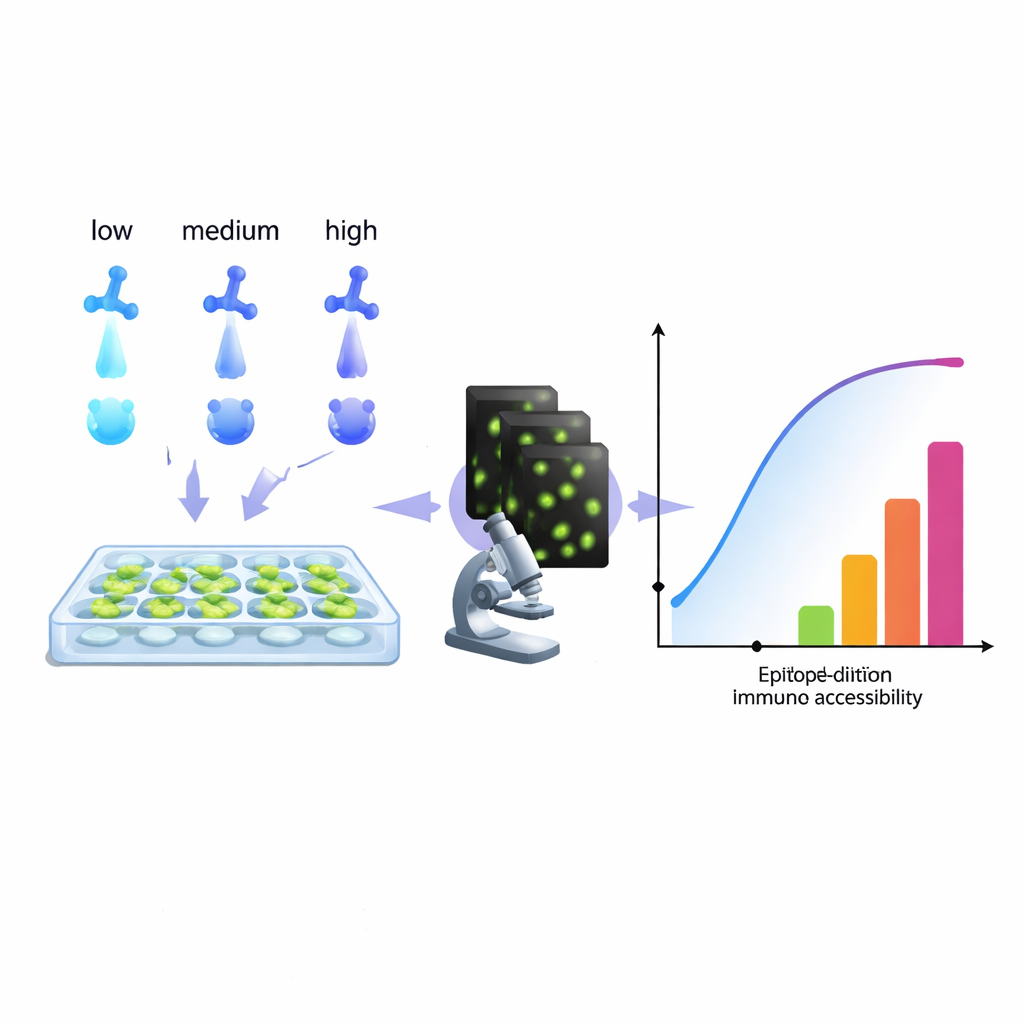
Comment les scientifiques règlent habituellement les marquages par anticorps
Lorsqu’ils mettent en place une expérience d’immunomarquage, les chercheurs devinent généralement une concentration d’anticorps à partir de la fiche technique, testent quelques dilutions, et choisissent celle qui « a l’air bien ». En réalité, d’innombrables facteurs minuscules — conformation des protéines, encombrement à l’intérieur des cellules, pH, et la capacité de l’anticorps à se faufiler jusqu’à sa cible — déterminent si un anticorps adhère ou est lessivé. Les méthodes traditionnelles mesurant l’affinité des anticorps, comme la résonance plasmonique de surface, fonctionnent mieux sur des protéines purifiées déposées sur des surfaces artificielles, pas sur des cellules ou tissus densément peuplés. Les valeurs obtenues peuvent donc ne pas refléter le système biologique réel où l’anticorps est utilisé. En conséquence, les laboratoires peuvent sans le savoir choisir des concentrations qui augmentent un fond flou ou masquent des cibles importantes mais moins accessibles.
Transformer une simple série de dilutions en « cartes d’accessibilité »
Les auteurs proposent une approche différente : considérer une série de dilutions d’anticorps standard comme un jeu de données riche et l’ajuster avec un modèle qui reflète ce que l’imagerie observe réellement — des anticorps qui restent liés même après des lavages répétés. En analysant la façon dont le signal croît en fonction de la concentration, leur algorithme reconstruit un « histogramme d’accessibilité ». Plutôt que de tenter d’isoler des constantes de liaison chimiques pures, cet histogramme regroupe les sites cibles en « classes d’épitope » techniques selon la facilité avec laquelle ils se colorent dans des conditions réelles. Un même épitope biologique peut apparaître dans plusieurs classes si, par exemple, il est facile d’accès sur une partie d’une cellule et plus difficile dans une région encombrée. Fait crucial, cette méthode fonctionne directement à partir des mesures au microscope, sans avoir besoin de protéines purifiées ni de matériel supplémentaire : tout laboratoire capable de réaliser une série de dilutions et de quantifier la fluorescence peut, en principe, construire de tels histogrammes. 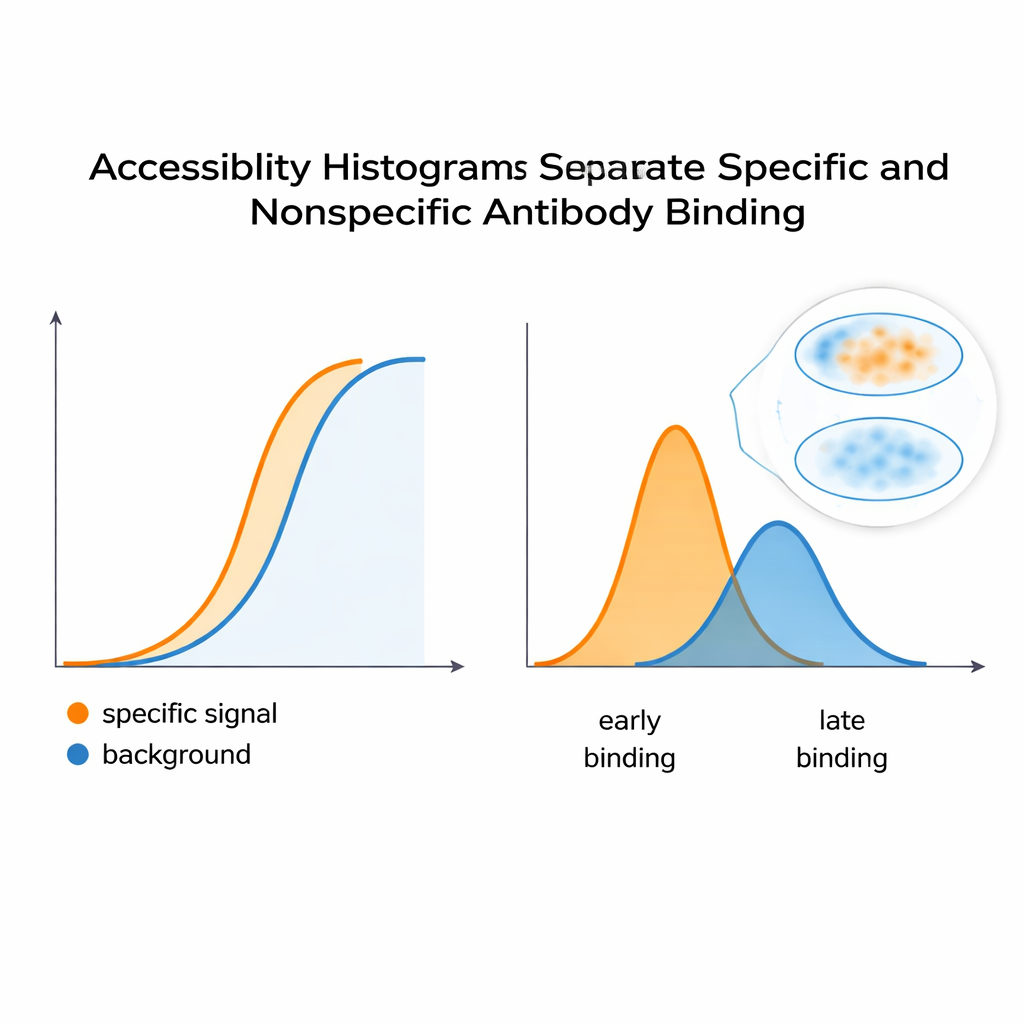
Séparer le vrai signal du bruit de fond
Pour vérifier que ces histogrammes captent réellement le comportement du marquage, l’équipe a construit un système contrôlé utilisant des cellules HeLa et deux anticorps monoclonaux : l’un reproduisant un signal souhaité et spécifique, l’autre simulant un bruit de fond indésirable. Lorsqu’ils étaient mélangés, la courbe de fluorescence combinée ressemblait à une réponse lisse et unique — rien d’évident ne laissait deviner deux contributeurs distincts. Mais l’analyse computationnelle a scindé cette courbe en pics séparés dans l’histogramme d’accessibilité, révélant au moins deux classes d’épitope sous-jacentes. Une stratégie similaire appliquée à un anticorps reconnaissant un site sensible à la conformation sur une sous-unité régulatrice de la PKA a montré que des changements de conformation — déclenchés par une molécule appelée cAMP — déplaçaient la distribution des épitopes accessibles. Cela suggère que la méthode peut signaler quand la structure des protéines s’ouvre ou se ferme, modifiant la facilité avec laquelle les anticorps peuvent se lier à l’intérieur des cellules.
Choisir de meilleures dilutions et marquer davantage avec une seule couleur
Parce que chaque pic de l’histogramme d’accessibilité contribue principalement sur une certaine plage de concentrations, les auteurs utilisent ces pics comme guide pour choisir des dilutions « idéales ». Les pics de faible accessibilité qui n’apparaissent qu’à des niveaux d’anticorps très élevés sont susceptibles d’inclure des liaisons non spécifiques, tandis que les premiers pics reflètent souvent la cible visée. En modélisant la façon dont les pics individuels construisent la courbe dose–réponse globale, l’équipe peut proposer des dilutions qui maximisent le signal spécifique avant que des pics problématiques n’apparaissent — parfois bien plus diluées que les recommandations du fabricant. Ils étendent ensuite cette idée en une forme astucieuse de « multiplexage computationnel ». En marquant le même échantillon fixé à plusieurs reprises avec des concentrations choisies, en imageant après chaque étape et en soustrayant les images précédentes des suivantes, ils isolent des signaux liés à différentes classes d’accessibilité, détachant ainsi efficacement plusieurs cibles au sein d’un seul canal de fluorescence.
Ce que cela signifie pour le travail de laboratoire quotidien
Concrètement, ce travail transforme une étape de dépannage de routine — réaliser une série de dilutions d’anticorps — en un outil quantitatif. Les histogrammes d’accessibilité aident les scientifiques à repérer la complexité cachée des marquages, à choisir des dilutions qui réduisent le bruit trompeur, et, dans certains cas, à séparer des signaux qui se chevauchent sans recourir à des étiquettes fluorescentes supplémentaires. Bien que le modèle sous-jacent soit volontairement simple et ne capture pas tous les détails moléculaires, il est conçu pour être facile à utiliser et suffisamment robuste pour des données du monde réel. S’il était largement adopté, cette approche pourrait rendre les techniques basées sur les anticorps — de l’imagerie de base aux tests diagnostiques — plus fiables, plus informatives et moins tributaires de l’essai-erreur.
Citation: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Mots-clés: marquage par anticorps, immunofluorescence, accessibilité des épitopes, réponse à la dose, multiplexage computationnel