Clear Sky Science · fr
Progrès stratégiques pour les études structurales par cryo‑EM des petits (‹100 kDa) GPCR
Pourquoi de minuscules interrupteurs cellulaires comptent pour la médecine
Une grande partie de la médecine moderne agit en modulant discrètement de minuscules interrupteurs situés dans nos membranes cellulaires, appelés récepteurs couplés aux protéines G (GPCR). Ces interrupteurs détectent des hormones, des odeurs et des médicaments, et environ un tiers de tous les médicaments approuvés ciblent ces récepteurs. Pour concevoir des traitements plus sûrs et plus intelligents, les scientifiques ont besoin d’images 3D détaillées de ces récepteurs, en particulier sous leur forme « inactive » ou éteinte, que beaucoup de médicaments visent spécifiquement. Cet article explique comment les chercheurs apprennent à visualiser certains des plus petits GPCR par cryo‑microscopie électronique (cryo‑EM), une méthode d’imagerie puissante capable d’observer des molécules vitrifiées dans un état proche de la nature.
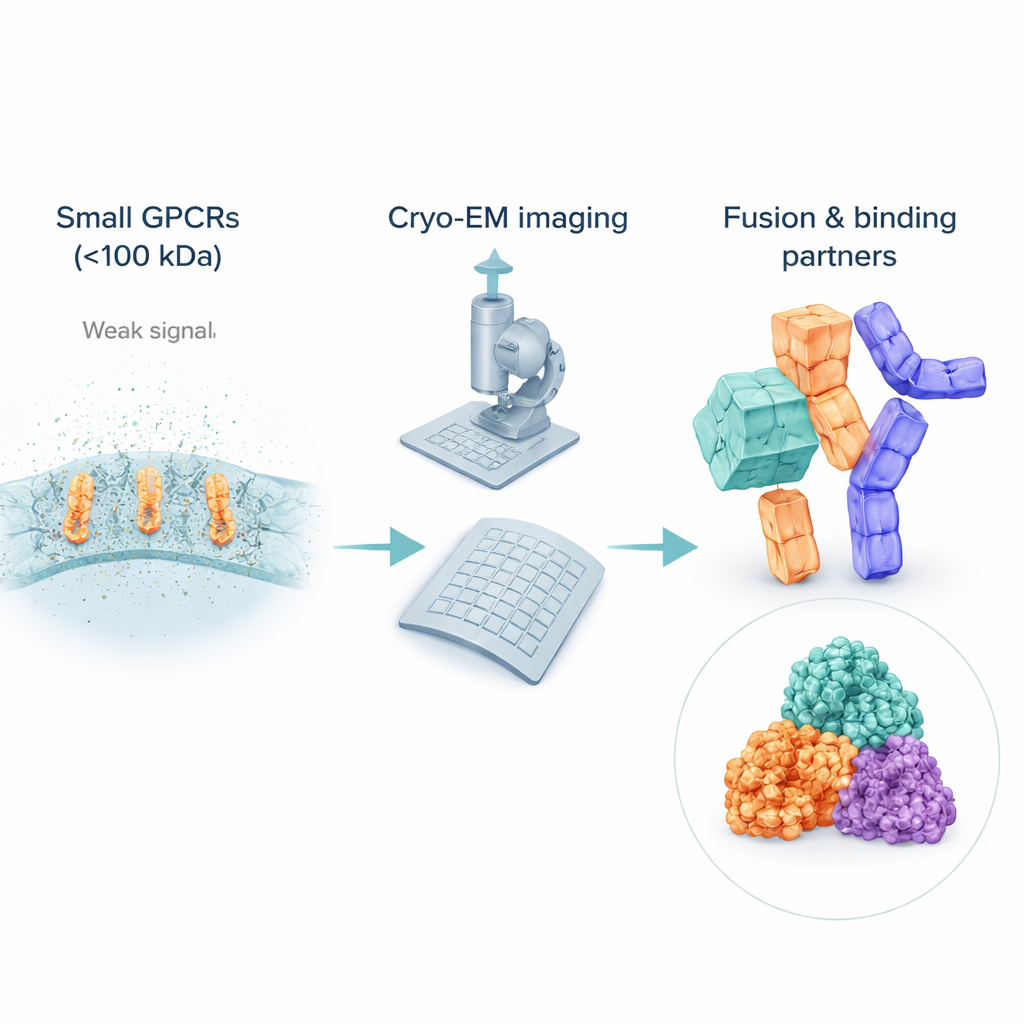
Le défi de voir des récepteurs très petits
Bien que la cryo‑EM ait révolutionné la biologie structurale, elle peine encore avec des molécules petites et flexibles. De nombreux GPCR inactifs pèsent bien moins de 100 kilodaltons, ce qui les rend difficiles à détecter et à aligner dans des images bruitées. Pour rester solubles, les scientifiques enveloppent ces récepteurs dans des bulles de détergent ou des mimétiques lipidiques, qui peuvent en réalité apparaître « plus volumineux » au faisceau d’électrons que le récepteur lui‑même, noyant le signal de la protéine d’intérêt. Contrairement aux récepteurs actifs liés à des partenaires massifs comme les protéines G, les GPCR inactifs manquent souvent de caractéristiques externes marquées, ce qui complique la mise en commun informatique de nombreuses images pour obtenir une vue 3D nette. En conséquence, la plupart des structures de GPCR inactifs proviennent encore d’anciennes méthodes par rayons X, laissant un vide dans la couverture cryo‑EM précisément là où agissent de nombreux médicaments.
Alourdir les récepteurs avec des aides intégrées
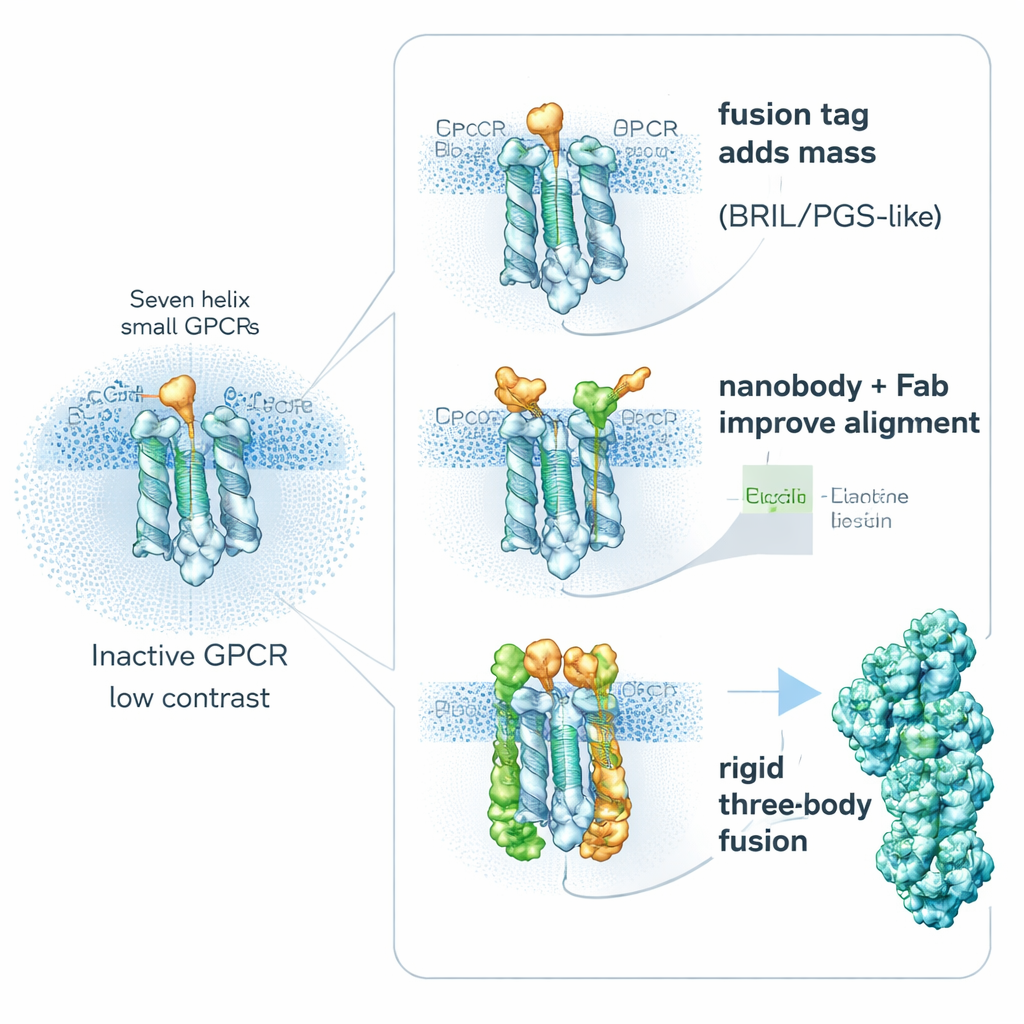
Une stratégie clé est étonnamment simple : rendre volontairement le récepteur « plus lourd ». Les chercheurs fusionnent génétiquement de petites protéines auxiliaires stables sur des parties flexibles des GPCR pour augmenter leur taille et leur rigidité, sans bloquer les régions importantes de liaison aux médicaments. Les aides populaires incluent BRIL (un faisceau à quatre hélices), PGS (un fragment d’enzyme thermostable) et une protéine plus volumineuse en forme de pince appelée calcineurine. Ces partenaires de fusion sont souvent insérés dans une boucle interne mobile qui relie deux hélices. En rigidifiant cette zone, ils réduisent le flou causé par le mouvement moléculaire et fournissent des formes reconnaissables qui aident les algorithmes à aligner les particules. Les études montrent que la position et l’orientation précises de la pièce de fusion peuvent faire ou défaire un projet : pour un récepteur, un tag PGS placé différemment a amélioré la résolution d’un flou de 6 angströms à un 3,7 angströms beaucoup plus net.
Emprunter des anticorps et des liaisons conçues comme poignées
Une seconde voie évite d’intégrer de grosses fusions au récepteur et fixe plutôt des « poignées » à haute affinité depuis l’extérieur. De minuscules fragments d’anticorps appelés nanocorps et des ligands apparentés peuvent être développés pour reconnaître les GPCR inactifs et se lier aux boucles internes flexibles. Un exemple marquant est le Nanobody‑6, initialement créé comme capteur pour un récepteur opioïde puis réutilisé, avec quelques ajustements modestes, pour stabiliser plusieurs autres GPCR sous leur forme inactive. Parce qu’il se fixe de façon décentrée, il fournit à chaque particule un indice d’orientation clair, rendant l’alignement des images plus fiable. Les chercheurs prolongent souvent cette idée en ajoutant une seconde couche — un fragment d’anticorps ordinaire reconnaissant le nanocorps lui‑même — créant un complexe plus volumineux et plus rigide qui apparaît nettement en cryo‑EM. D’autres ligands conçus, tels que les DARPins, peuvent être utilisés comme entretoises modulaires ou comme connecteurs vers des cages protéiques plus grandes, augmentant encore le signal des très petites cibles.
Conception d’échantillons plus intelligente et traitement d’images boosté par l’IA
La fusion d’aides ou l’ajout de ligands ne raconte qu’une partie de l’histoire. La revue souligne que de bonnes structures commencent par des constructions de récepteurs soigneusement conçues : tronquer les régions de queue trop flexibles, introduire des mutations stabilisantes et utiliser des outils modernes de prédiction de structure pour identifier les parties susceptibles de poser problème. Côté imagerie, des astuces anciennes comme les plaques de phase, qui augmentent le contraste pour des particules faibles, sont complétées voire remplacées par des outils d’intelligence artificielle. Des programmes d’apprentissage profond peuvent repérer de minuscules particules cachées dans des micrographies bruitées, et de nouveaux algorithmes peuvent trier les images selon différentes formes lorsque les récepteurs adoptent plusieurs conformations. Avec des aides fiduciales, ces avancées poussent la cryo‑EM vers une résolution fiable des protéines membranaires autrefois jugées trop petites ou trop dynamiques pour être étudiées.
Ce que cela signifie pour les médicaments à venir
L’article conclut qu’il n’existe pas une « aide magique » unique qui fonctionne pour tous les récepteurs, mais qu’une boîte à outils croissante de partenaires de fusion, de ligands de type anticorps et de méthodes pilotées par l’IA ouvre progressivement le paysage inactif des GPCR à la cryo‑EM. Pour les non‑spécialistes, l’essentiel est que, en faisant paraître les petits récepteurs plus gros et plus ordonnés au microscope, les scientifiques peuvent enfin obtenir des instantanés détaillés des formes exactes que de nombreux médicaments préfèrent lier. Ces plans structuraux devraient accélérer la conception de médicaments qui éteignent plus précisément ces interrupteurs cellulaires — ou ajustent finement leur activité — avec moins d’effets secondaires.
Citation: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Mots-clés: Récepteurs couplés aux protéines G, Cryo‑microscopie électronique, découverte de médicaments, biologie structurale, échafaudages de nanocorps