Clear Sky Science · fr
Lier la tension moléculaire et les tractions cellulaires : une approche multiéchelle de la mécanique des adhésions focales
Comment les cellules ressentent et tirent sur leur environnement
Chaque fois qu’une cellule se déplace, se divise ou remodèle un tissu, elle tire discrètement sur son environnement. Ces petites forces mécaniques sont cruciales pour la cicatrisation, la propagation du cancer et le développement des organes, mais elles sont difficiles à observer et encore plus à mesurer. Cette étude présente une nouvelle manière d’examiner ces forces sous deux angles simultanément : combien une cellule entière tire sur un matériau souple, et quelle force portent des « ressorts moléculaires » individuels au sein des sites d’ancrage de la cellule. En reliant ces vues, le travail aide à expliquer comment les cellules perçoivent la rigidité et régulent leur prise sur le monde qui les entoure.
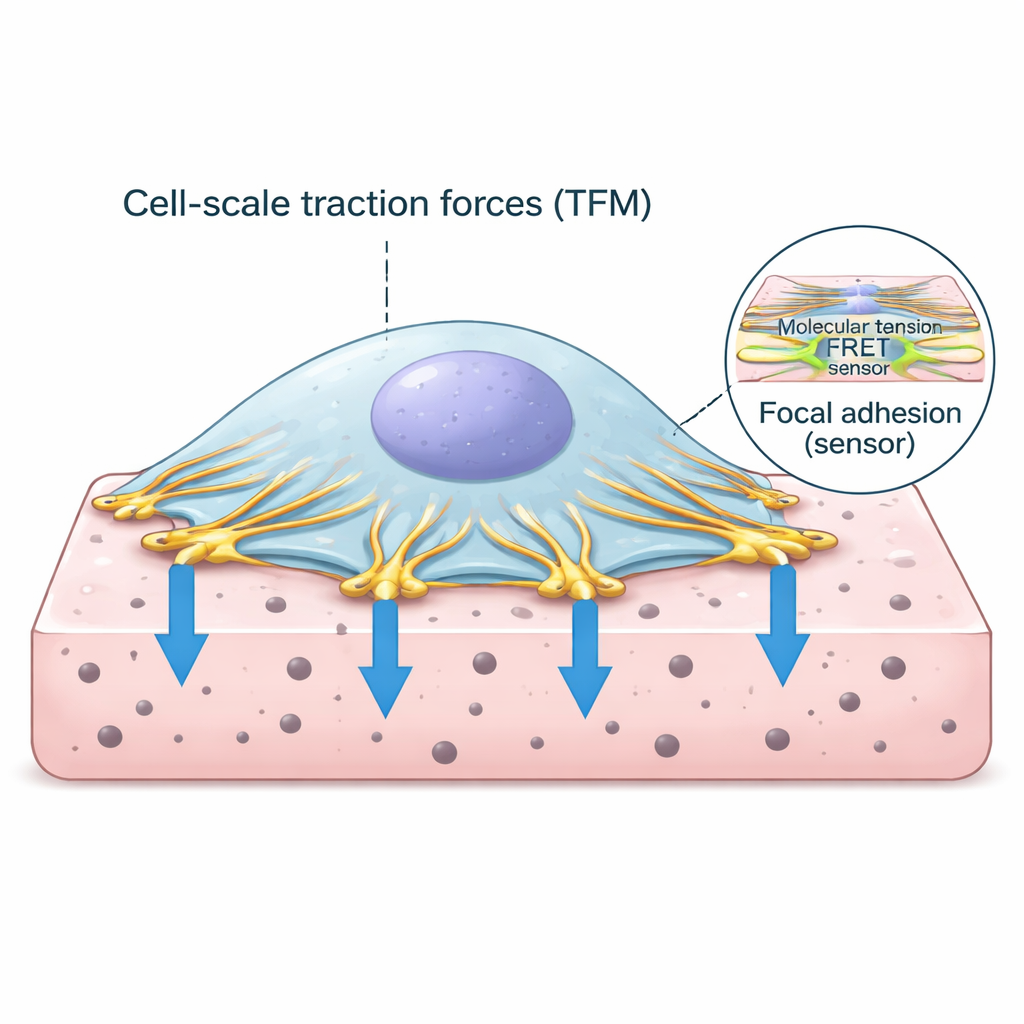
Les points d’appui de la cellule sur le monde extérieur
Les cellules ne flottent pas simplement dans les tissus ; elles s’ancrent via des points de contact spécialisés appelés adhésions focales. À ces endroits, l’échafaudage interne de la cellule constitué de fibres d’actine se connecte à des protéines qui traversent la membrane cellulaire et s’accrochent à la matrice environnante. L’une des protéines clés de ce complexe d’ancrage est la vinculine, qui se comporte comme un lien sensible à la force. Lorsque la machinerie contractile de la cellule tire sur l’actine, la vinculine ressent la charge et contribue à renforcer la connexion. Comprendre quelle force circule à travers ces liens, et comment cela se rapporte à la traction globale de la cellule, est central pour déchiffrer comment les tissus restent sains ou deviennent malades.
Deux fenêtres sur la force cellulaire
Les chercheurs ont combiné deux techniques puissantes dans un seul flux de travail. D’abord, la microscopie des forces de traction mesure dans quelle mesure une cellule déforme un substrat gélifié et souple en suivant le mouvement de minuscules billes fluorescentes dans le gel. À partir de ces déplacements, on peut calculer la distribution des forces de poussée et de traction sous la cellule. Ensuite, une protéine vinculine spécialement conçue porte un capteur de tension fluorescent qui modifie son signal lumineux lorsqu’il est étiré. En utilisant une imagerie avancée par temps de vie de fluorescence, l’équipe a converti ce signal lumineux en une lecture de la tension moléculaire sur la vinculine. Ils ont conçu des hydrogels minces et plats pouvant être imagés à haute résolution et écrit un logiciel personnalisé pour aligner, segmenter et analyser les deux jeux de données jusqu’au niveau des sites d’adhésion individuels.
Comment la rigidité modifie l’effort de la cellule
Quand les cellules ont été cultivées sur des gels mous vs plus raides, leur comportement global a changé de manière nette. Sur des substrats plus rigides, les cellules s’étalaient davantage et exerçaient des forces de traction plus fortes à la surface du gel. En parallèle, la lecture fluorescente du capteur de vinculine indiquait une tension moléculaire plus élevée au sein des adhésions focales. Fait intéressant, les caractéristiques structurelles de base de ces adhésions — comme leur nombre ou leur taille moyenne — ne changeaient pas beaucoup entre gels mous et rigides. En revanche, c’est l’organisation des forces qui différait. Les adhésions larges, orientées radialement et contenant plus de vinculine avaient tendance à supporter des tractions plus élevées, ce qui suggère que tant la géométrie que la composition moléculaire de ces sites contribuent à déterminer la force avec laquelle la cellule tire.
Une relation complexe entre forces locales et moléculaires
Un examen plus fin des adhésions individuelles a révélé que le lien entre la traction locale et la tension de la vinculine n’est pas universel. Dans certaines cellules, les adhésions qui généraient des tractions plus élevées montraient aussi une tension de vinculine plus élevée, ce qui implique que des contacts engagés et porteurs de charge partagent la force plus directement via leurs liens moléculaires. Dans d’autres cellules, le schéma inverse apparaissait : des régions de forte traction étaient associées à une tension de vinculine plus faible, tandis que d’autres adhésions supportaient une charge moléculaire plus importante sans produire de grandes tractions externes. Beaucoup de cellules ne montraient aucun motif clair. Ces comportements distincts reflètent probablement différents états cellulaires — comme l’étalement actif, l’adhésion stable ou la rétraction — et suggèrent que les cellules peuvent redistribuer les forces au sein de leur réseau d’adhésions de multiples façons.
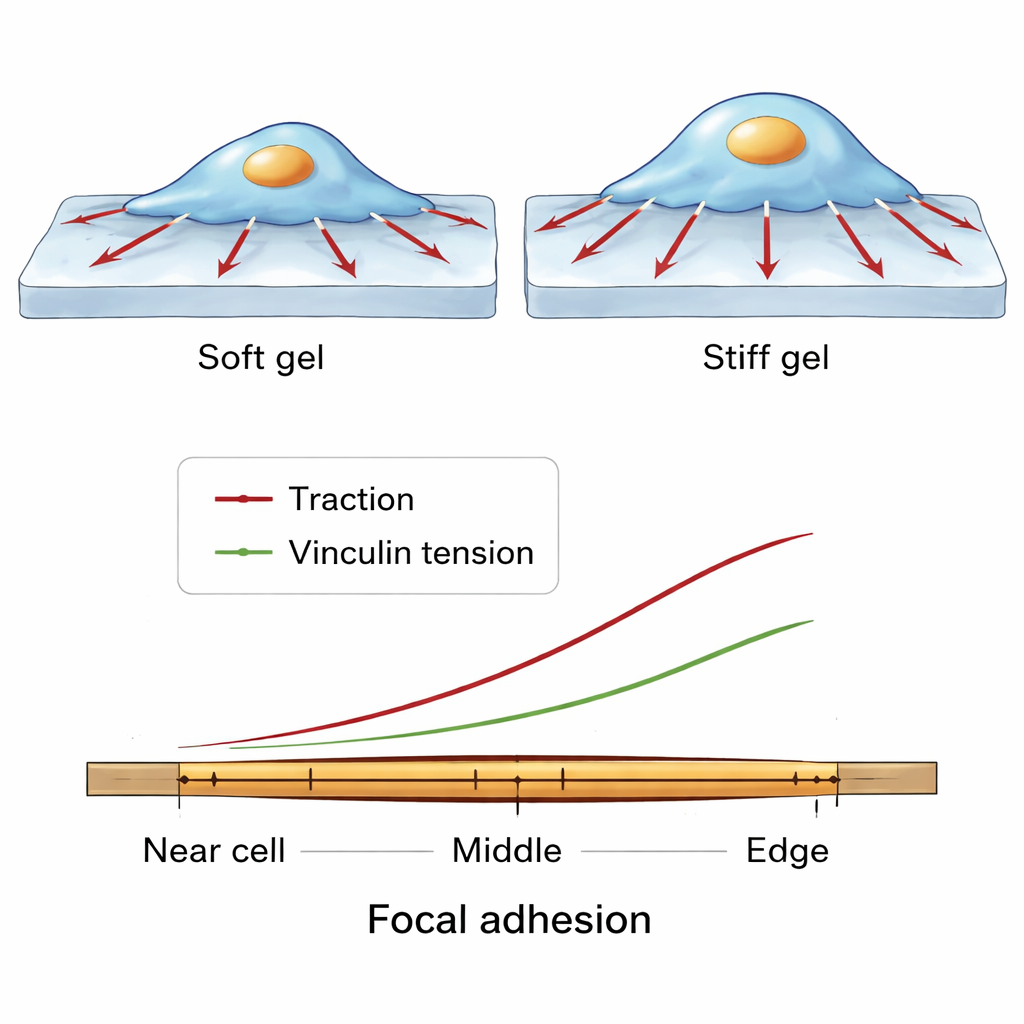
Patrons de force à l’échelle fine le long d’un seul point d’ancrage
L’équipe a ensuite zoomé encore plus, examinant comment les forces varient le long de la longueur d’une seule adhésion focale, du côté proche du centre cellulaire jusqu’au bord près du périmètre. À travers de nombreuses cellules et conditions, un schéma cohérent est apparu. Les molécules de vinculine étaient les plus densément regroupées vers le milieu de l’adhésion. Cependant, tant la traction exercée sur le substrat que la tension moléculaire sur la vinculine augmentaient vers l’extrémité externe, plus périphérique. Cela suggère un jeu d’équilibre : dans les régions centrales, de nombreuses molécules de vinculine peuvent partager la charge, de sorte que chacune ressent moins de tension, alors qu’à l’extrémité extérieure, moins de molécules portent relativement plus de force, soutenant une forte traction locale tout en maintenant l’adhésion intacte.
Ce que cela signifie pour la santé et la maladie
En fusionnant des cartes de traction à l’échelle cellulaire avec des mesures de tension au niveau protéique, cette étude offre une image multiéchelle de la manière dont les cellules gèrent leur prise mécanique. Le travail montre que lorsque l’environnement se rigidifie, les cellules tirent plus fort et sollicitent davantage leurs liens de vinculine, mais que la relation détaillée entre forces externes et tension moléculaire varie d’une adhésion à l’autre et d’une cellule à l’autre. Parallèlement, un motif spatial robuste de distribution des forces au sein des adhésions individuelles semble conservé. Pour un non-spécialiste, le message clé est que les cellules ajustent finement à la fois où et comment elles tirent, redistribuant la force à travers de nombreux « ressorts » moléculaires pour s’adapter à différents environnements mécaniques — un principe qui peut sous-tendre des processus aussi divers que le développement des tissus, la fibrose et l’invasion cancéreuse.
Citation: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Mots-clés: mécanique cellulaire, adhésions focales, vinculine, microscopie des forces de traction, mécanotransduction