Clear Sky Science · fr
Dynamique temporelle de la clivage collatéral de l’ARN par LbuCas13a dans les cellules humaines
Transformer une défense bactérienne en un destructeur cellulaire de précision
Des chercheurs ont découvert comment convertir une protéine immunitaire bactérienne en un interrupteur de « self-destruct » très sélectif pour cellules humaines. En exploitant une enzyme CRISPR nommée LbuCas13a, ils peuvent reconnaître un ARNm choisi à l’intérieur d’une cellule puis déchiqueter presque tous les autres ARN de cette cellule. Pour un lectorat non spécialiste, cela est fascinant parce que les messages ARN contrôlent quelles protéines une cellule produit ; apprendre à les effacer sur commande ouvre des possibilités pour de nouveaux traitements contre le cancer, des stratégies antivirales et des outils puissants pour la recherche.
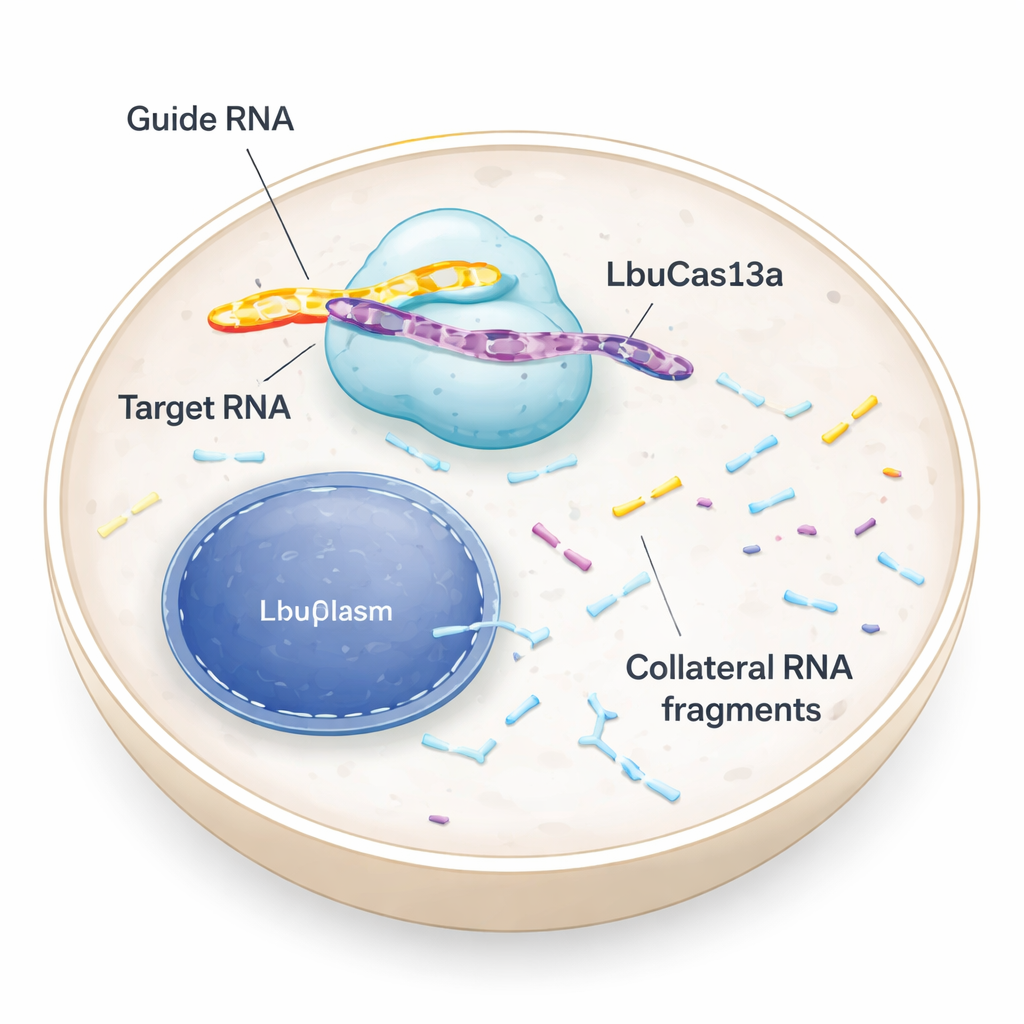
Des ciseaux moléculaires qui ciblent l’ARN, pas l’ADN
La plupart des gens ont entendu parler d’outils CRISPR qui coupent l’ADN et réécrivent le code génétique. LbuCas13a est différent : il reconnaît et coupe l’ARN, ces messages temporaires qui transmettent les instructions de l’ADN aux usines à protéines de la cellule. Chez les bactéries, les enzymes Cas13 font partie d’une défense antivirale. Une fois qu’elles repèrent un ARN viral, elles ne se contentent pas de trancher cet envahisseur, elles commencent aussi à couper de nombreux autres ARN à proximité. Cette activité « collatérale » peut pousser les cellules infectées en dormance ou à la mort, contribuant à protéger la communauté bactérienne. Les premiers tests dans des cellules animales et humaines suggéraient que le clivage collatéral de Cas13 était faible ou absent, si bien que l’enzyme était principalement utilisée comme un interrupteur précis pour l’ARN. La nouvelle étude revisite cette hypothèse et montre que, dans les bonnes conditions, l’activité collatérale dans les cellules humaines peut être à la fois forte et utile.
Déchaîner le clivage collatéral dans les cellules humaines
L’équipe a comparé plusieurs variantes de Cas13 et a constaté que LbuCas13a était particulièrement puissante. Ils ont livré la protéine LbuCas13a purifiée, préchargée avec un court ARN guide, directement dans des cellules humaines, une forme d’« injection » moléculaire appelée livraison de ribonucléoprotéine (RNP). Lorsque le guide correspondait à un ARN cible — comme un gène marqueur fluorescent ou des messages naturels abondants tels que GAPDH et l’ARNr 18S — l’enzyme a d’abord coupé cette cible, puis a commencé à mâcher de nombreux autres ARN. Environ 50 minutes plus tard, le profil global des ARN de la cellule avait changé de façon spectaculaire, avec l’apparition de fragments de clivage caractéristiques. Cet effet collatéral a été observé avec différentes méthodes de livraison et dans une gamme de types cellulaires, montrant qu’il ne s’agissait pas d’un artefact d’une seule lignée cellulaire ou d’une cible artificielle.
Du déchiquetage de l’ARN à la mort cellulaire et à la sélection
Que devient une cellule dont les messages ARN disparaissent soudainement ? Grâce à l’imagerie cellulaire en direct, les chercheurs ont observé que les cellules exprimant l’ARN cible entraient progressivement en apoptose, une forme ordonnée de mort cellulaire programmée marquée par des signaux « d’alerte » caractéristiques avant que la cellule ne se fragmente. De manière importante, les cellules voisines qui n’exprimaient pas l’ARN cible restaient majoritairement indemnes, démontrant que l’autodestruction est spécifique. Le groupe a ensuite exploité cette propriété comme outil de sélection. Lorsqu’ils ont mélangé des cellules porteuses de la cible avec des cellules normales et activé LbuCas13a, les cellules porteuses de la cible ont été éliminées de manière sélective sur plusieurs jours. En répétant le traitement plusieurs fois, leur fraction a encore diminué. Ils ont montré que cela pouvait enrichir pour des cellules correctement éditées et pouvait aussi être ajusté pour attaquer des cellules cancéreuses qui surproduisent un oncogène — ici CDK4 — tout en épargnant des cellules apparentées qui produisent beaucoup moins cet ARN.
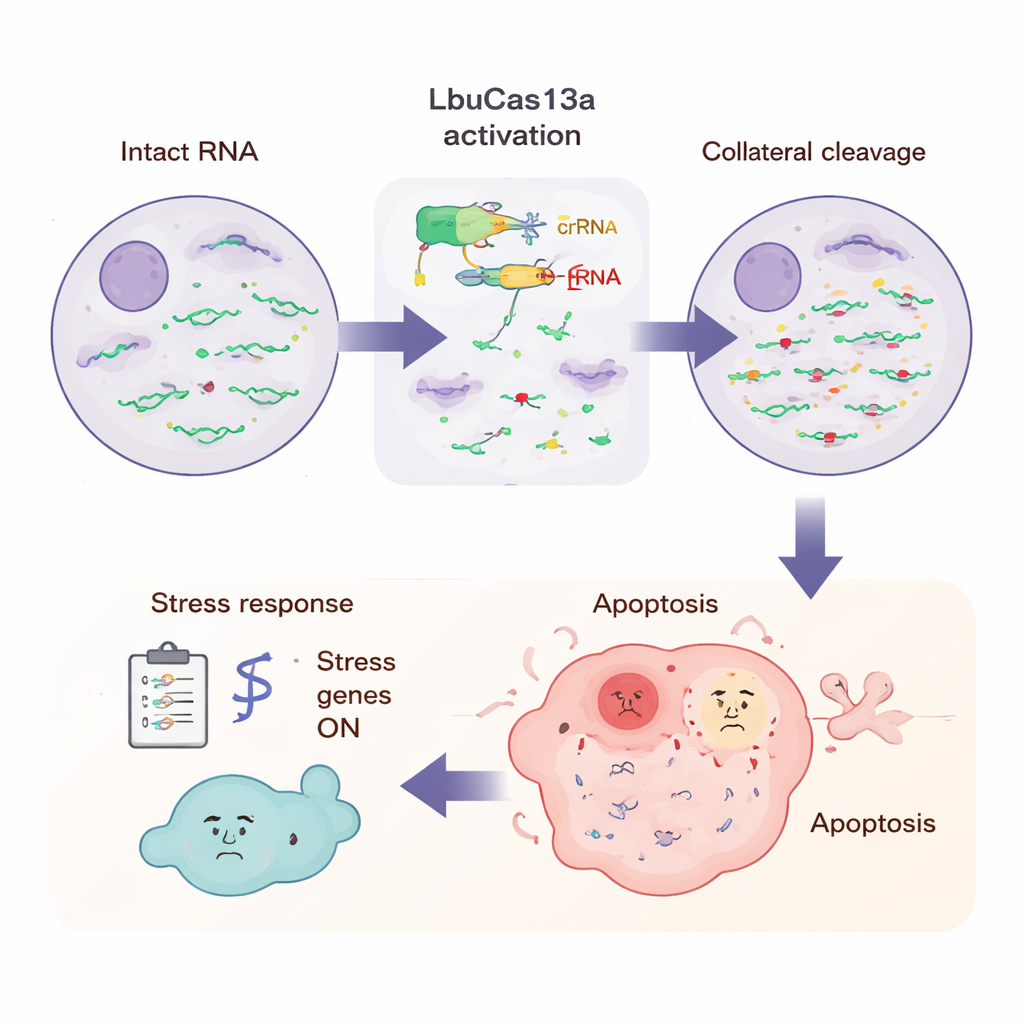
Ce que la cellule ressent pendant l’attaque
Pour mieux comprendre l’ensemble des événements, les scientifiques ont mesuré tous les ARN de la cellule à plusieurs moments après l’activation de LbuCas13a. En ajoutant des standards ARN connus, ils ont pu constater que la plupart des ARN codant des protéines dans le cytoplasme chutaient de plus de moitié en quelques heures, tandis que certains ARN — tels que les messages mitochondriaux et certains ARN non codants nucléaires — étaient largement épargnés. Le séquençage longue lecture a révélé que le clivage se produisait à des positions nucléotidiques répétées et spécifiques, souvent dans des régions en boucle flexibles de l’ARN riches en base uracile, correspondant à des motifs observés dans des expériences in vitro. À des temps plus tardifs, de nombreux gènes de stress et d’immunité innée s’activaient, y compris ceux liés aux signaux inflammatoires et aux défenses antivirales. Ce schéma suggère que la cellule perçoit l’afflux soudain d’extrémités d’ARN brisées un peu comme une infection virale, déclenchant un programme d’alarme qui aboutit à l’apoptose.
Pourquoi cela importe et quelles perspectives
En termes simples, l’étude montre que LbuCas13a peut être transformée en un « interrupteur de mort » guidé par l’ARN : si une cellule produit trop d’un ARN particulier, activer LbuCas13a contre cet ARN provoque une perte quasi globale d’ARN, un signal d’alarme de type immunitaire, puis une mort cellulaire contrôlée. Comme le processus dépend fortement de l’abondance de l’ARN cible, il pourrait être utilisé pour éliminer des cellules qui surexpriment des gènes nocifs — comme certaines cellules cancéreuses — ou pour nettoyer des cellules indésirables dans des cultures mixtes lors d’expériences ou de productions de thérapies cellulaires. En même temps, ce travail est un avertissement : les outils CRISPR visant l’ARN peuvent avoir des effets secondaires puissants qu’il faut contrôler soigneusement. Comprendre quand et comment le clivage collatéral de l’ARN se produit est essentiel pour utiliser en toute sécurité les technologies Cas13 en médecine et en biotechnologie.
Citation: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Mots-clés: CRISPR-Cas13, Clivage de l’ARN, Mort cellulaire, Ciblage du cancer, Outils d’édition génique