Clear Sky Science · fr
Modulation des récepteurs GPCR de classe B1 humains par les lipides de la membrane plasmique
Des graisses qui affinent les récepteurs de messages de nos cellules
Nos cellules s’appuient sur de minuscules antennes protéiques, appelées récepteurs, pour détecter des hormones et des neurotransmetteurs. De nombreux médicaments phares agissent en ciblant ces récepteurs. Cette étude révèle que les lipides courants de la couche externe de nos cellules font bien plus que constituer un décor passif : ils se lient directement à toute une famille de récepteurs essentiels et en modulent la forme, orientant subtilement l’activation ou l’inhibition des signaux. Comprendre cette couche de contrôle cachée pourrait aider à concevoir des médicaments plus intelligents avec moins d’effets secondaires.
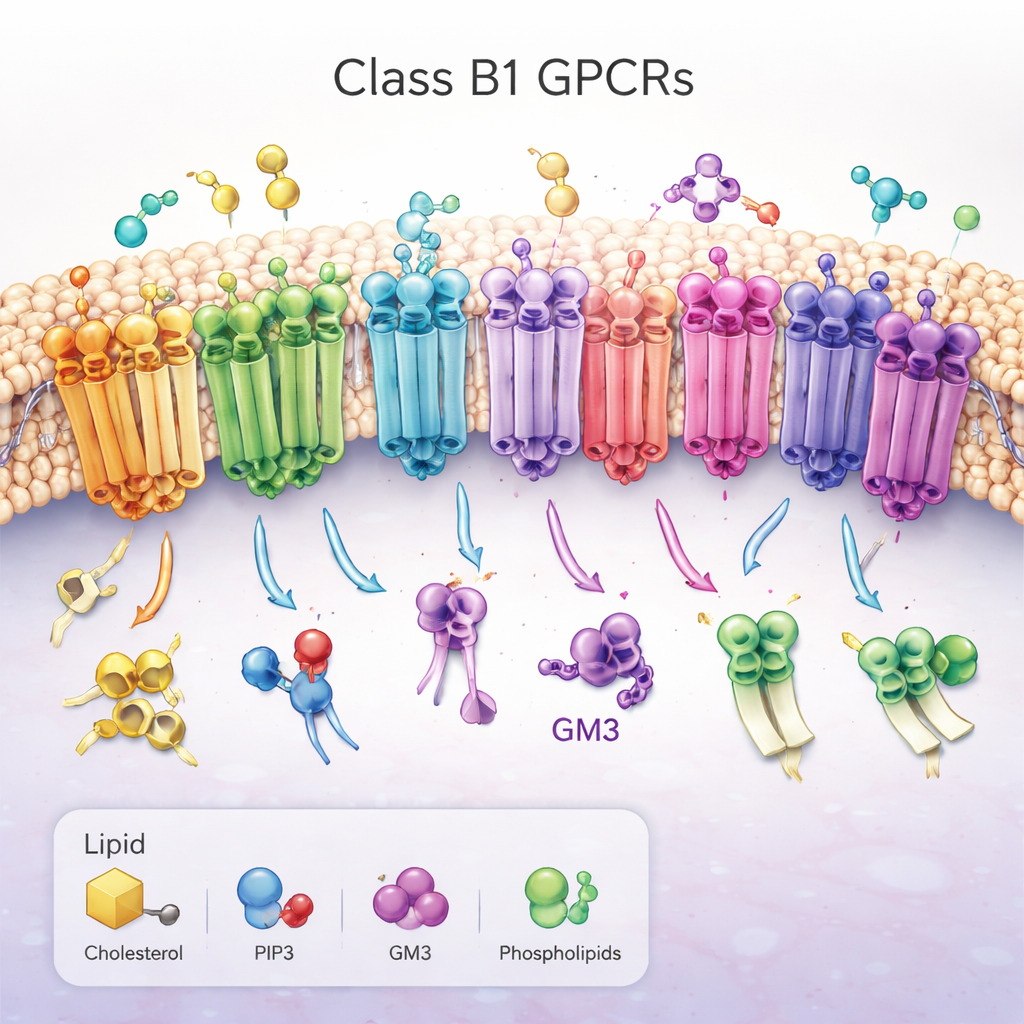
Une famille d’antennes moléculaires importantes
Les travaux portent sur les récepteurs couplés aux protéines G de la classe B1 (GPCRs), un ensemble de 15 récepteurs étroitement apparentés qui aident à réguler la glycémie, le métabolisme, la croissance et les réponses au stress. Ils traversent la membrane plasmique, avec une large « tête » extracellulaire qui saisit des molécules de type hormone et un faisceau de sept hélices qui traversent la membrane lipidique. Lorsqu’ils sont activés, ces récepteurs changent de conformation du côté intracellulaire, ouvrant une gouttière qui recrute des protéines partenaires et déclenche des cascades de signalisation. En raison de leur rôle central dans des pathologies comme le diabète et l’obésité, les GPCR de classe B1 sont des cibles médicamenteuses de premier plan, mais la manière dont les lipides environnants les régulent est restée en grande partie mystérieuse.
Simuler les récepteurs dans leur voisinage naturel
Plutôt que d’étudier les récepteurs dans des micelles de détergent artificielles, les chercheurs ont placé les 15 GPCR humains de classe B1 dans des membranes construites par ordinateur reproduisant le mélange complexe de lipides des cellules réelles. En utilisant une technique appelée dynamique moléculaire en représentation coarse-grained, ils ont lancé de multiples simulations longues pour chaque récepteur, dans leurs états actif et inactif, totalisant environ une milliseconde de temps simulé. Ils ont suivi comment trois lipides « régulateurs » — le cholestérol, le lipide de signalisation PIP2 et le lipide glycosylé GM3 — approchaient, se liaient et se détachaient de différentes régions de chaque récepteur. Pour garantir que d’autres puissent reproduire et étendre cet énorme jeu de données, ils ont documenté chaque étape de la configuration et de l’analyse avec un outil de workflow ouvert appelé aiida-gromacs, et ont comparé leurs résultats basés sur la physique avec des prédictions d’un nouveau modèle d’IA (Chai‑1) qui estime comment les protéines lient de petites molécules.
Poches cachées et prise lipidique conservée
Les simulations ont mis au jour des schémas de liaison récurrents à travers toute la famille de récepteurs. Le cholestérol, surtout connu des discussions alimentaires, a été observé loger non seulement dans un site déjà connu sur l’une des hélices, mais aussi dans des « poches profondes » au sein de la membrane entre les hélices, avec sa tête polaire étonnamment enfoncée dans la membrane. Un récepteur, le récepteur à la sécrétine, a montré des liaisons au cholestérol particulièrement durables dans des poches distinctes selon qu’il était actif ou inactif, ce qui suggère que le cholestérol peut fortement biaiser son mode de signalisation. Le PIP2 a affiché un comportement remarquablement conservé : il s’est regroupé du côté intracellulaire des récepteurs, à la jonction de deux hélices et d’un court segment en queue (TM6, TM7 et H8), en particulier quand les récepteurs étaient dans l’état actif. À cet emplacement, des réseaux d’acides aminés chargés positivement saisissaient le groupement tête négativement chargé de PIP2, suggérant un moyen par lequel ce lipide pourrait stabiliser la conformation active ou aider au recrutement des partenaires de signalisation à l’intérieur de la cellule.
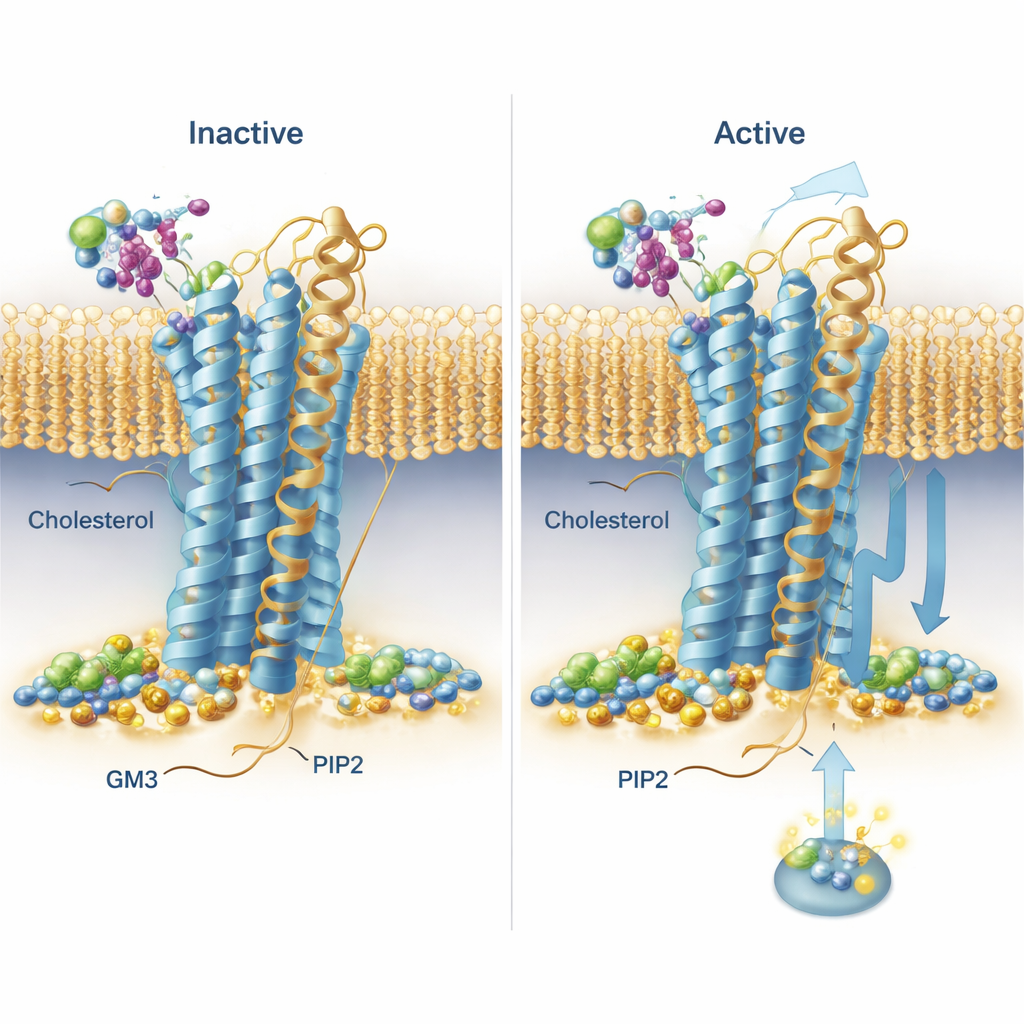
Un lipide sucré qui module le mouvement des récepteurs
Le GM3, un lipide complexe à tête sucrée, interagissait principalement avec les larges domaines extracellulaires des récepteurs. L’équipe a remarqué que les domaines externes de certains récepteurs oscillaient et se pliaient beaucoup par rapport à la membrane, tandis que d’autres étaient plus contraints. Pour deux récepteurs d’intérêt thérapeutique — GLP‑1R et GIPR — ils ont examiné le rôle de GM3 en détail. Dans les simulations avec GM3 présent, le lipide s’installait soit contre la base du domaine externe et la poche de liaison au ligand (GLP‑1R), soit se fixait à l’extrémité distale du domaine externe (GIPR), influençant dans les deux cas la liberté de mouvement de ces domaines. Pour tester ces prédictions dans des cellules vivantes, les chercheurs ont utilisé une technique lumineuse (TR‑FRET) qui renseigne sur la proximité d’une tête de récepteur marquée par rapport à la membrane. Lorsqu’ils ont réduit les niveaux de GM3 avec un inhibiteur de petite molécule, ils ont observé des changements mesurables dans la façon dont les têtes des récepteurs se déplaçaient après stimulation, cohérents avec l’idée que GM3 ajuste la flexibilité des récepteurs de manière dépendante du récepteur et de son état.
Pourquoi ces partenariats lipide–récepteur comptent
Globalement, l’étude brosse le portrait des GPCR de classe B1 non seulement comme des interrupteurs hormonaux mais comme des éléments d’une danse étroitement chorégraphiée avec les lipides environnants. Le cholestérol peut occuper des poches cachées et favoriser subtilement certains résultats de signalisation, le PIP2 forme une « poignée » intracellulaire conservée qui pourrait verrouiller les récepteurs en conformation active et orienter les protéines partenaires, et le GM3 module la mobilité des régions externes des récepteurs et leur rencontre avec les ligands. Pour un public non spécialiste, le message clé est que la membrane est une couche régulatrice active : de petites différences dans la composition lipidique peuvent modifier le comportement d’un même récepteur selon les tissus ou les états pathologiques. En cartographiant ces interactions en détail et en partageant les données de simulation sous-jacentes, ce travail pose les bases pour concevoir des médicaments futurs qui exploitent ou évitent des contacts lipidiques spécifiques, rendant potentiellement les traitements plus sélectifs et plus efficaces.
Citation: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Mots-clés: Récepteurs couplés aux protéines G, lipides membranaires, cholestérol, PIP2, GM3