Clear Sky Science · fr
Perspectives structurelles sur le trafic de métalloclusters dans l’échafaudage d’assemblage de la nitrogénase NifEN
Comment la nature construit un outil chimique puissant
L’azote est partout dans l’air, mais la plupart des organismes ne peuvent pas l’utiliser sous cette forme. Une enzyme spéciale, la nitrogénase, résout ce problème en convertissant l’azote atmosphérique en ammoniac, un ingrédient clé pour la vie et pour les engrais. Au cœur de la nitrogénase se trouve un « cluster » métallique dense qui effectue la chimie difficile, mais la façon dont la cellule assemble cette pièce complexe restait mystérieuse. Cet article examine ce processus de construction, révélant comment une protéine-échafaudage nommée NifEN sert de quai de chargement flexible et de convoyeur pour la cargaison métallique du cluster.
Une usine moléculaire derrière les engrais et les carburants
La nitrogénase est l’équivalent naturel des procédés industriels qui produisent l’ammoniac et les carburants liquides. Plutôt que d’utiliser d’immenses réacteurs, les microbes emploient une machine protéique compacte alimentée par l’énergie cellulaire. Ses performances dépendent d’un centre métallique d’une complexité unique, construit à partir de fer, de soufre, de molybdène, de carbone et d’un groupe latéral organique. L’assemblage de ce noyau est trop délicat pour être laissé au hasard, si bien que la cellule mobilise une chaîne de protéines auxiliaires. L’une des plus importantes est NifEN, qui reçoit un précurseur presque achevé composé uniquement de fer (appelé le L‑cluster), aide à le convertir en forme mature (le M‑cluster), puis le remet à l’enzyme nitrogénase opérationnelle. Comprendre comment NifEN gère ce trafic pourrait éclairer des tentatives d’ingénierie microbienne pour une production d’engrais plus propre ou de nouveaux carburants à base de carbone.
Voir une machine en mouvement par images figées
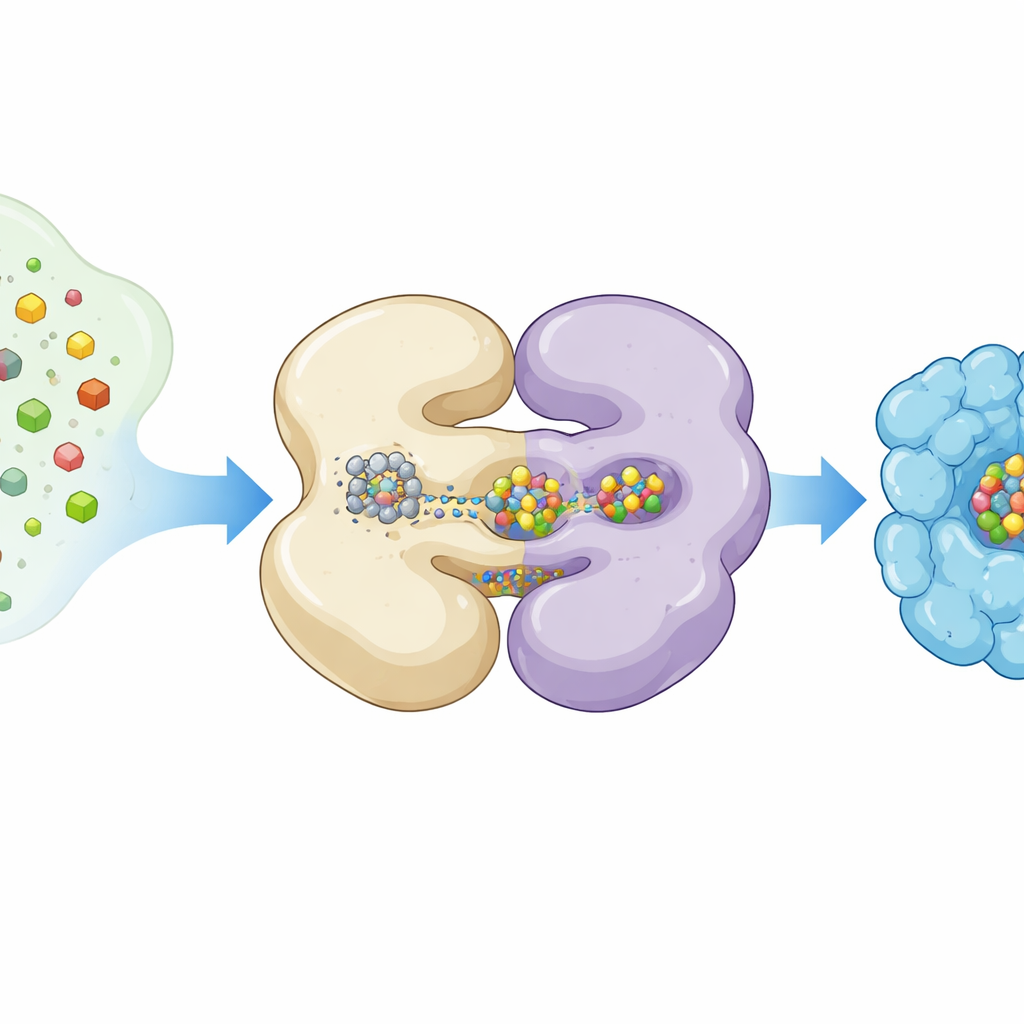
Les auteurs ont utilisé la cryomicroscopie électronique, une technique qui image les protéines à des températures extrêmement basses, pour capturer NifEN dans différentes postures de fonctionnement. Ils ont exprimé NifEN dans des bactéries de laboratoire de manière à ce que certains exemplaires de la protéine portent un L‑cluster et d’autres soient vides. En triant des millions d’images de particules uniques, ils ont reconstruit deux formes principales : une forme « apo » dépourvue du cluster mobile et une forme « holo » avec le cluster lié à un site interne. Les deux formes partagent un cœur composé de quatre sous‑unités arrangées en deux paires, mais lorsque le L‑cluster est présent, une moitié de NifEN devient nettement plus ordonnée et plusieurs hélices se replient vers l’intérieur, serrant la cargaison métallique.
Un tunnel caché pour la cargaison métallique
La comparaison des structures vide et chargée a révélé une caractéristique frappante : un long tunnel traversant le dimère NifEN. À l’état vide, ce passage est large et ouvert ; après la liaison du cluster il se resserre alors que la protéine agrippe son passager. Des structures cristallines antérieures avaient montré une position alternative « extérieure » du L‑cluster près de la surface protéique. En réunissant toutes les vues, les chercheurs ont déduit que le cluster peut occuper au moins deux stations sur NifEN — l’une enfouie à l’intérieur et l’autre exposée — et se déplacer entre elles le long d’un trajet courbe commandé par des déplacements d’un domaine flexible. Ce mouvement semble plus relâché que dans l’enzyme nitrogénase finale, dont le cluster actif est maintenu de manière rigide, ce qui suggère que NifEN est conçu pour le transfert plutôt que pour la catalyse à long terme.
Partenaires d’amarrage et route continue
Pour comprendre comment NifEN se connecte à ses partenaires en amont et en aval, l’équipe a combiné leurs structures expérimentales avec des modèles informatiques d’AlphaFold 3 et des images de microscopie électronique de résolution inférieure de complexes protéiques. Les modèles suggèrent que l’enzyme NifB, qui fabrique le L‑cluster à partir de petites unités fer‑soufre, s’amarre dans une vallée sur une face de NifEN. Là, un tunnel continu peut être tracé depuis les centres métalliques de NifB directement dans le tunnel de NifEN et jusqu’à la station interne du L‑cluster. Sur la face opposée de NifEN, un site d’amarrage différent reçoit NifH, la protéine qui insère le molybdène et un groupe latéral organique pour compléter le cofacteur. Dans cette configuration, le L‑cluster se trouve au site de surface, idéalement positionné pour être modifié. La mutation d’acides aminés clés bordant la voie proposée perturbe le chargement, le déplacement ou la maturation du cluster, apportant un soutien expérimental à ce modèle de tapis roulant.
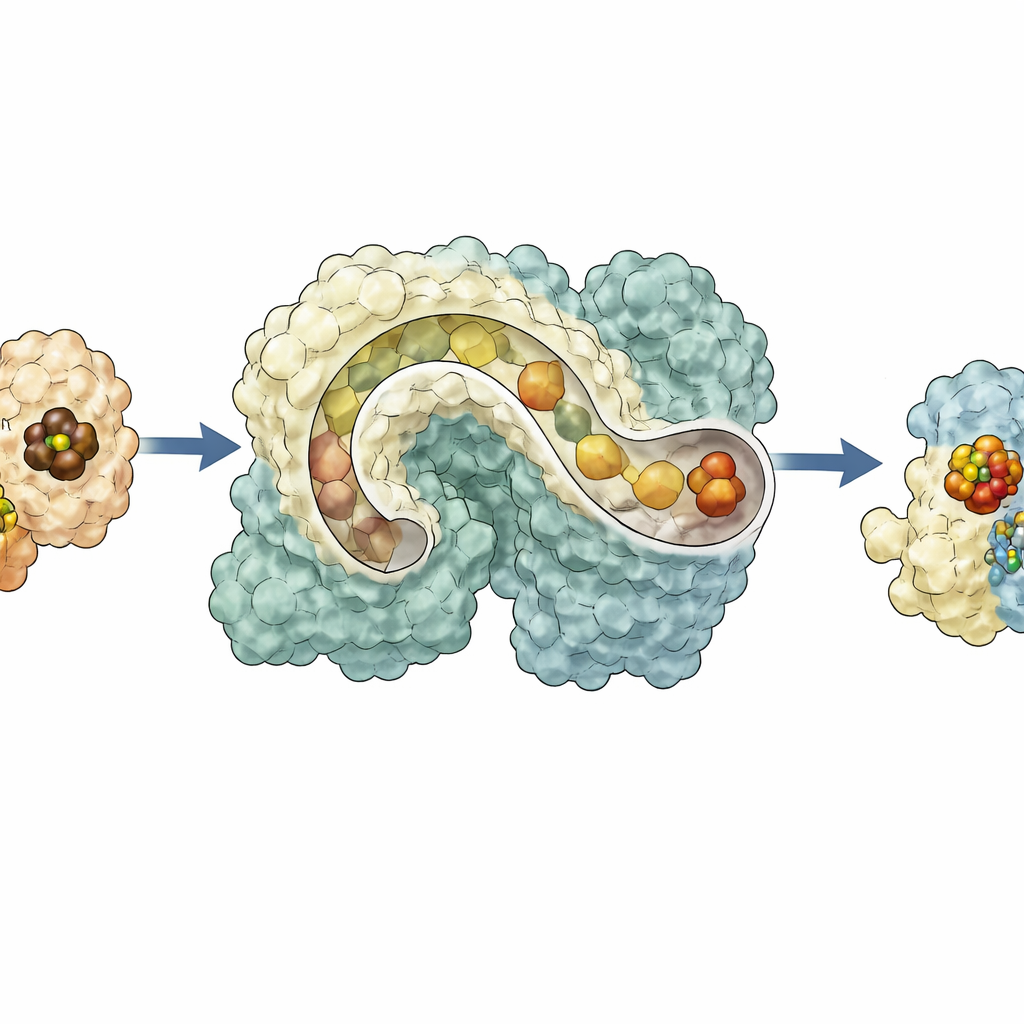
Pourquoi un échafaudage flexible est important
Dans l’ensemble, les résultats décrivent NifEN comme un carrefour dynamique qui reçoit un noyau métallique de NifB d’un côté, le déplace dans une baie intérieure de stockage, puis le présente sur la surface opposée pour finition par NifH avant de guider le cluster mature vers l’intérieur pour la livraison à la nitrogénase. Ce schéma de trafic commandé par conformation explique comment plusieurs étapes délicates peuvent être coordonnées au sein d’un même cadre protéique et suggère comment des enzymes ancestrales ont pu évoluer d’échafaudages plus flexibles vers les catalyseurs hautement spécialisés d’aujourd’hui. Pour un public non spécialiste, ce travail montre que, même à l’échelle nanométrique, la nature s’appuie sur des lignes d’assemblage, des tunnels et des pièces mobiles pour construire les outils moléculaires qui sous-tendent les cycles mondiaux de l’azote, la production alimentaire et, potentiellement, de futures technologies vertes.
Citation: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Mots-clés: nitrogénase, assemblage de métallocluster, échafaudage NifEN, cryomicroscopie électronique, fixation biologique de l’azote