Clear Sky Science · fr
Un modèle d’apprentissage profond intégrant des données structurées et du texte clinique pour prédire la récidive de la fibrillation auriculaire
Pourquoi cela compte pour les personnes avec des battements irréguliers
La fibrillation auriculaire, un trouble fréquent du rythme cardiaque, réapparaît souvent même après qu’un patient ait subi une ablation par cathéter, une procédure invasive visant à rétablir un rythme cardiaque normal. De nombreux patients et leurs médecins se demandent : qui est le plus susceptible de voir le problème revenir, et qui peut être rassuré ? Cette étude montre comment l’intelligence artificielle moderne peut analyser à la fois les données chiffrées et les notes des médecins dans le dossier médical pour prévoir plus précisément la probabilité de récidive de la fibrillation auriculaire, ce qui pourrait orienter le suivi et éviter des procédures répétées.
Un problème rythmique cardiaque difficile qui récidive souvent
L’ablation par cathéter est largement utilisée pour traiter la fibrillation auriculaire en détruisant par chaleur ou froid de petites zones à l’intérieur du cœur qui déclenchent ou entretiennent des rythmes anormaux. Pourtant, 30 à 50 % des patients présentent un retour d’arythmie dans l’année, nécessitant parfois une nouvelle intervention. Les scores de risque existants, basés principalement sur quelques mesures comme la taille des cavités cardiaques et le type de fibrillation auriculaire, ne donnent qu’un tableau partiel. Ils ignorent généralement des détails riches sur le déroulement de la procédure, l’apparence du cœur à l’échographie et les nuances de l’état général du patient qui restent enfouies dans les rapports textuels. En conséquence, les médecins ont encore du mal à identifier qui nécessite vraiment une surveillance rapprochée ou un traitement préventif supplémentaire.
Transformer les données hospitalières routinières en un outil de prédiction plus intelligent
Des chercheurs en Chine ont rassemblé des informations sur 2 508 patients ayant subi une ablation de fibrillation auriculaire dans cinq hôpitaux entre 2015 et 2024. Le patient type avait 65 ans, et environ un sur cinq a eu une récidive d’arythmie au cours d’un suivi médian de près de trois ans. Pour chaque personne, l’équipe a collecté des données structurées — telles que l’âge, la tension artérielle, les résultats biologiques, la taille des cavités cardiaques et les scores de risque existants — ainsi que des éléments textuels non structurés, notamment des synthèses de moniteurs cardiaques de 24 heures, des rapports d’échographie et des notes de procédure détaillées rédigées par des électrophysiologistes. Ils ont ensuite construit un modèle d’apprentissage profond à double branche : une branche traitait les données numériques et catégorielles, tandis que l’autre utilisait de grands modèles de langage pour transformer les rapports en texte libre en caractéristiques quantitatives pouvant être combinées avec les données numériques.
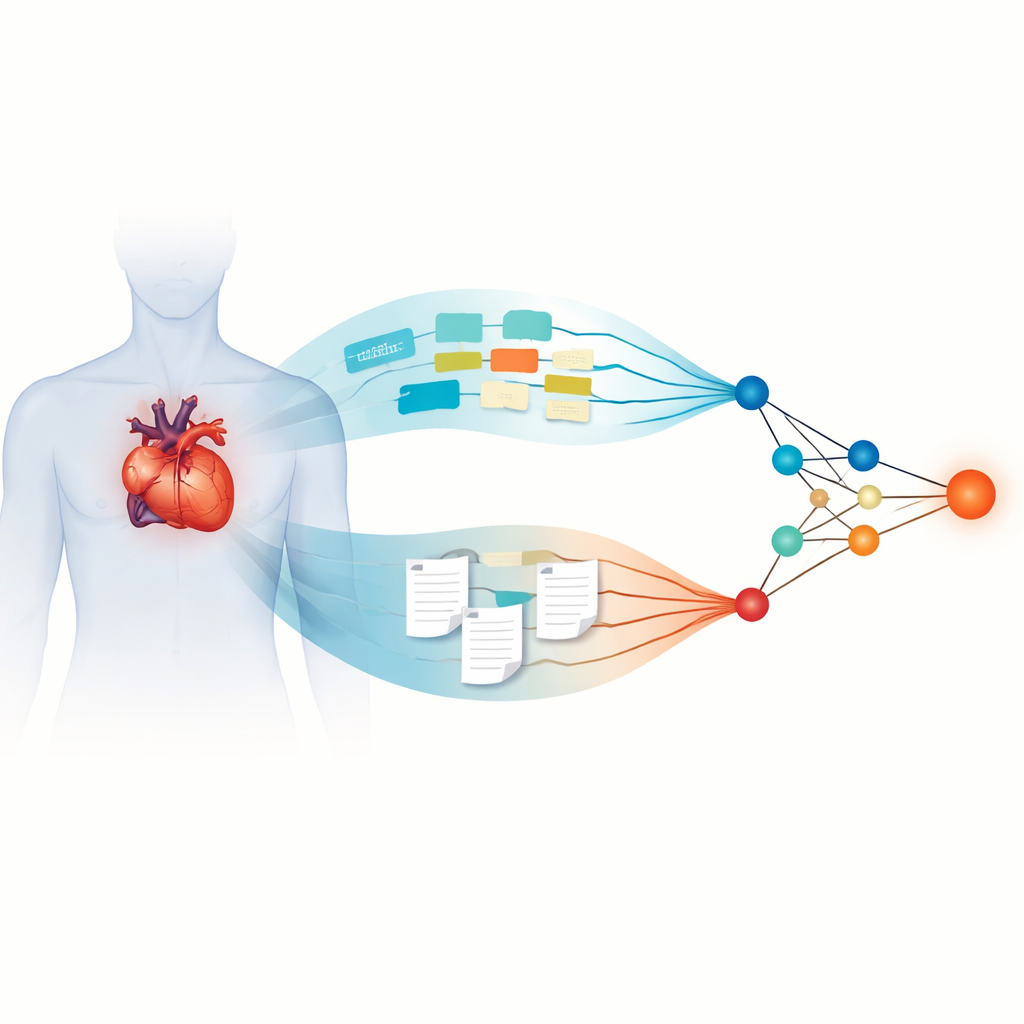
Comment les modèles de langage avancés lisent les notes des médecins
La branche textuelle du système reposait sur quatre grands modèles de langage modernes, entraînés à l’origine sur d’énormes collections de textes, puis adaptés au langage médical. Ces modèles ont été ajustés (fine‑tuning) sur des rapports hospitaliers dépersonnalisés afin de mieux saisir les termes et les motifs spécialisés. L’étude a comparé plusieurs modèles de langage pour déterminer lesquels produisaient des caractéristiques textuelles les plus prédictives de récidive. Le meilleur résultat est revenu à MedGemma, un modèle spécifiquement optimisé pour le contenu médical. Lorsque ses caractéristiques textuelles ont été fusionnées avec la branche de données structurées, le modèle final « MedGemma‑Fusion » a montré une précision remarquable, avec des surfaces sous la courbe ROC supérieures à 0,90 lors de l’entraînement, de la validation et sur des hôpitaux test indépendants. Cela signifiait que le modèle pouvait distinguer de manière fiable les patients qui resteraient exempts d’arythmie de ceux qui ne le seraient pas.
Jeter un coup d’œil à l’intérieur de la boîte noire de l’IA
Pour comprendre ce que le modèle utilisait réellement pour faire ses prédictions, les chercheurs ont appliqué des outils d’interprétabilité qui estiment l’influence de chaque entrée. Dans les données structurées, des facteurs cliniques familiers comme la durée d’évolution de la fibrillation auriculaire, la taille de l’oreillette gauche et le caractère paroxystique ou persistant du rythme avaient le plus de poids. Côté texte, des concepts clés liés aux procédures d’ablation — tels que les descriptions des veines pulmonaires et des potentiels électriques — ont été mis en avant, reflétant des étapes centrales au succès du traitement. Des termes relatifs au mouvement cardiaque dans les rapports d’échographie comptaient aussi, en accord avec l’idée que des altérations du mouvement des oreillettes traduisent des lésions anciennes. En revanche, les résumés des moniteurs cardiaques de 24 heures ont contribué relativement peu, probablement parce que de nombreux patients atteints de fibrillation auriculaire intermittente présentent un rythme normal pendant de courtes fenêtres de surveillance.
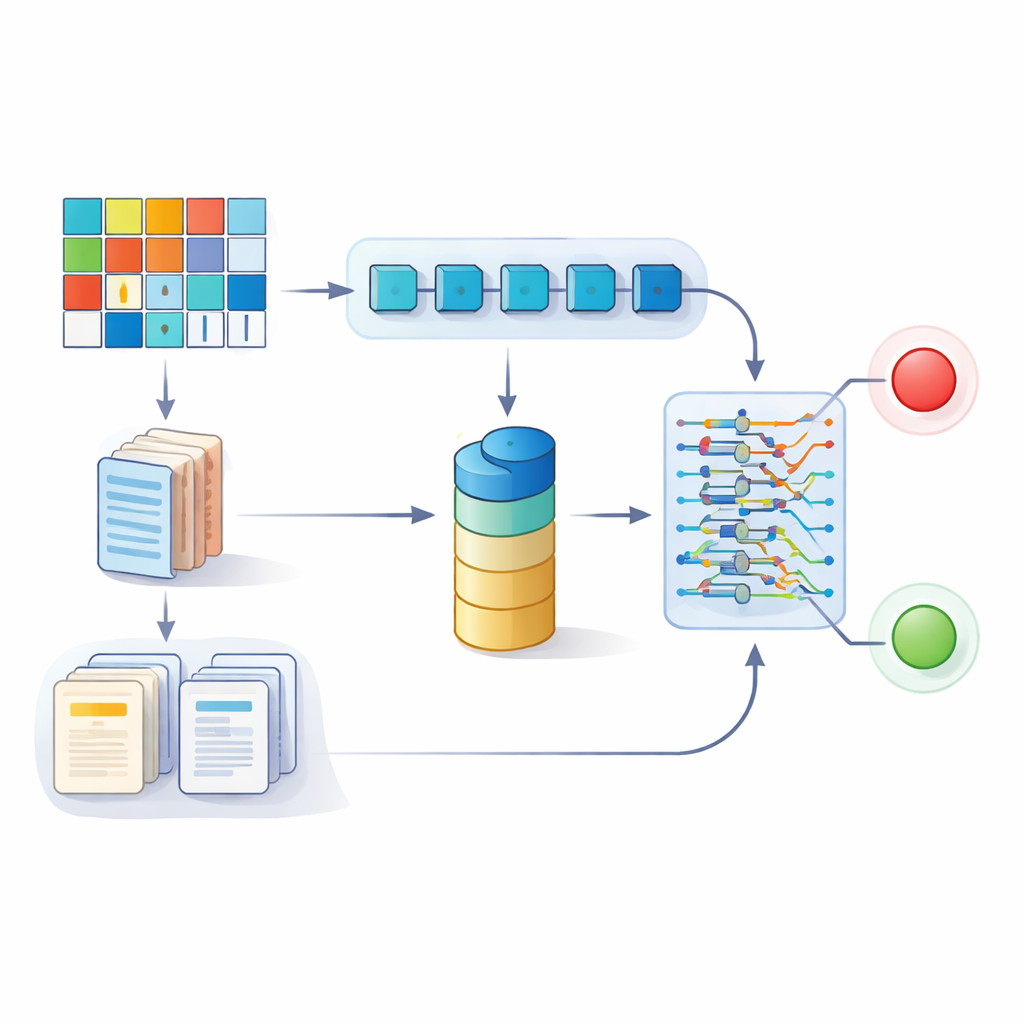
Du modèle de recherche aux décisions au chevet
Au‑delà de la précision brute, l’équipe a évalué comment leur outil séparait les patients en groupes à risque élevé et faible en utilisant des analyses de survie. Les patients identifiés comme à haut risque par MedGemma‑Fusion présentaient des taux de récidive nettement plus élevés au fil du temps. L’analyse des courbes de décision a suggéré que, sur de nombreux seuils raisonnables, l’utilisation du modèle pour guider les soins apporterait un bénéfice net supérieur à celui des scores traditionnels ou des mesures isolées. Néanmoins, les auteurs soulignent plusieurs mises en garde importantes : l’étude est rétrospective, les tailles d’échantillon — bien que grandes pour un projet unique — restent modestes pour l’apprentissage profond, et les styles de compte‑rendu variaient entre les hôpitaux. Des versions futures de grands modèles de langage et des tests plus larges dans d’autres systèmes de santé seront nécessaires avant que de tels outils ne deviennent routiniers. Cela dit, ce travail illustre comment la combinaison des données numériques courantes du dossier et de la nuance cachée dans les rapports narratifs peut affiner les prédictions et finir par aider à adapter le suivi et l’intensité du traitement des personnes vivant avec une fibrillation auriculaire.
Citation: Jia, S., Yin, Y., Guan, Y. et al. A deep learning model integrating structured data and clinical text for predicting atrial fibrillation recurrence. npj Digit. Med. 9, 253 (2026). https://doi.org/10.1038/s41746-026-02436-5
Mots-clés: fibrillation auriculaire, ablation par cathéter, apprentissage profond, exploitation de texte clinique, prédiction du risque