Clear Sky Science · fr
Réseau de neurones graphique contraint par la physique pour la prédiction en temps réel de l’hémodynamique des anévrismes intracrâniens
Pourquoi cela compte pour la santé du cerveau
Des zones affaiblies et bombées des artères cérébrales, appelées anévrismes intracrâniens, peuvent se rompre sans prévenir et provoquer des hémorragies potentiellement mortelles. Les cliniciens savent que la façon dont le sang s’écoule sur ces parois fragiles influence leur stabilité, mais les outils actuels de simulation de cet écoulement sont si lents et spécialisés qu’ils sont rarement utilisés dans la pratique quotidienne. Cette étude présente une méthode d’intelligence artificielle rapide capable d’imiter des simulations détaillées du flux sanguin en quelques secondes plutôt qu’en plusieurs heures, ouvrant la voie à des décisions plus rapides et personnalisées sur qui doit être traité et comment.
Des images statiques au sang en mouvement
À l’heure actuelle, la plupart des décisions concernant les anévrismes se fondent sur ce que révèlent les examens : la taille, la forme et la position de la saillie, ainsi que des facteurs de risque classiques comme l’âge et l’hypertension. Ces clichés ne montrent pas les forces invisibles du sang en mouvement, par exemple la force de cisaillement exercée sur la paroi vasculaire ou la variation de cette force au cours de chaque battement cardiaque. La dynamique des fluides numérique traditionnelle peut calculer ces quantités avec précision, mais nécessite une configuration experte et de longues exécutions sur des ordinateurs puissants. Par conséquent, de nombreux hôpitaux ne peuvent pas raisonnablement les utiliser lorsqu’un médecin a besoin d’une réponse durant une consultation ou une intervention d’urgence.
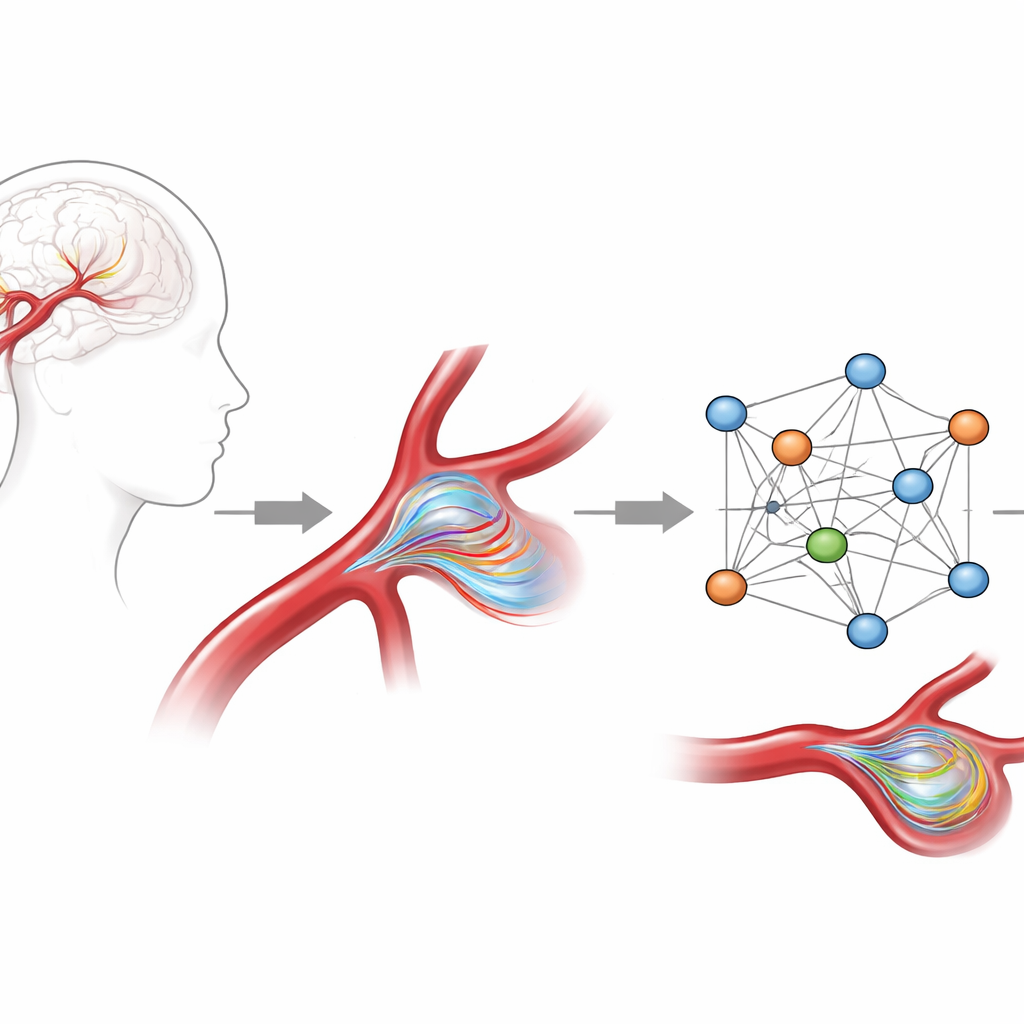
Apprendre à une IA à respecter la physique
Les chercheurs ont construit un modèle d’IA basé sur des réseaux de neurones graphiques, un type d’algorithme adapté aux structures ramifiées comme les maillages vasculaires plutôt qu’aux grilles d’images carrées. Ils l’ont entraîné sur des simulations numériques de haute qualité du flux sanguin dans 105 géométries d’anévrisme dérivées de données patients réelles, en se concentrant sur un emplacement fréquent d’une artère cérébrale clé. Chaque cas comprenait des champs tridimensionnels complets de vitesse et de pression sur un battement cardiaque entier. Pour donner au modèle une compréhension accrue de la physique sous-jacente, ils ont fait plus que lui demander de recopier les vitesses simulées : ils ont ajouté des caractéristiques décrivant la vitesse d’entrée du sang dans l’artère et son accélération, et ils ont pénalisé l’IA chaque fois que ses prédictions violaient des lois fluides de base comme la conservation de la masse.
Voir à l’intérieur d’une saillie dangereuse
Après l’entraînement, l’IA pouvait prendre une image instantanée des conditions d’écoulement et la faire évoluer rapidement dans le temps, recréant les motifs tourbillonnaires et les zones de recirculation à l’intérieur du sac anévrismal. Par rapport aux simulations de référence, ses erreurs à court terme étaient déjà faibles, mais le véritable test était de savoir si ces erreurs s’amplifieraient lorsqu’elle prédisait des dizaines d’instants à venir. La version enrichie et contrainte par la physique a réussi ce test : sur 50 pas de prédiction, ses erreurs étaient plus de six fois plus petites que celles d’un modèle de base plus simple, et elle suivait l’évolution du flux même pendant la phase la plus turbulente du battement. Lorsque l’équipe a converti ces champs de vitesse en mesures cliniquement pertinentes — telles que la contrainte de cisaillement pariétale moyenne sur le dôme de l’anévrisme — l’IA restait à environ 10 % des valeurs de référence et reproduisait les zones de contraintes maximales.
Généraliser au‑delà du jeu d’entraînement
Une question clé pour toute IA médicale est sa capacité à gérer des patients qu’elle n’a jamais vus. L’équipe a mis son modèle au défi avec deux types de situations inconnues, sans entraînement supplémentaire. D’abord, ils ont modifié les formes d’onde d’entrée pour correspondre à des patterns mesurés dans d’autres artères cérébrales. L’IA a suivi la nouvelle synchronisation et l’intensité de chaque impulsion, en maintenant des erreurs modestes et en capturant la recomposition du flux à l’intérieur de la saillie. Ensuite, ils l’ont testée sur quatre géométries d’anévrisme entièrement spécifiques à des patients, avec des tailles, largeurs de collet et trajectoires vasculaires différentes. Bien que les niveaux de vitesse exacts fussent parfois décalés, le modèle a reproduit les structures d’écoulement principales et les zones d’impact, suggérant qu’il avait appris le comportement sous‑jacent plutôt que de mémoriser les formes d’entraînement.
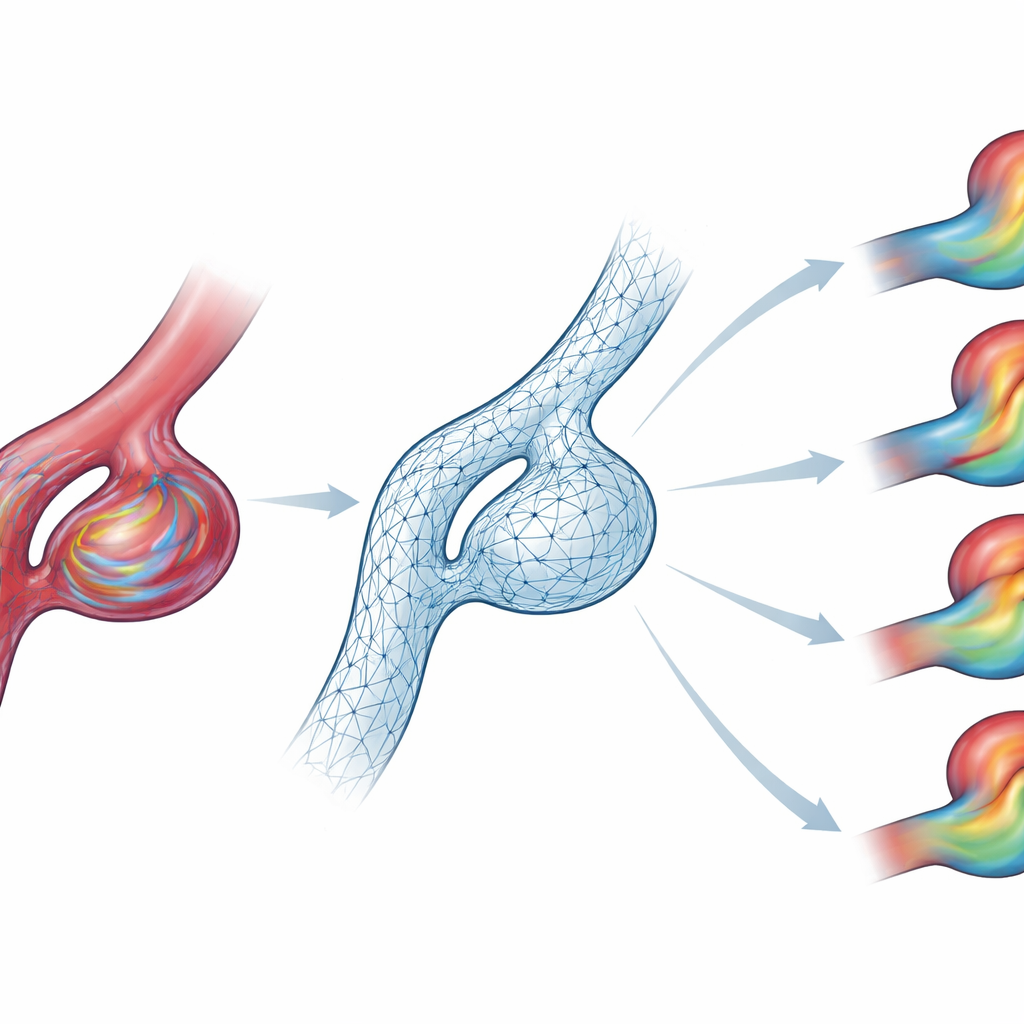
Des réponses plus rapides au chevet
Parce que cette IA s’exécute environ soixante fois plus vite que les simulations traditionnelles dont elle a appris, elle devient plus efficace que les méthodes standard après seulement quelques dizaines de cas et pourrait à terme fournir des prédictions de champ complet du flux sanguin en moins d’une minute. Les auteurs insistent sur le fait que leur outil n’est pas un prédicteur autonome de rupture ; il s’agit plutôt d’un moteur rapide pour générer des cartes d’écoulement et des contraintes pariétales physiquement cohérentes que d’autres modèles de risque peuvent utiliser. Ils publient aussi leur jeu de données de 105 cas comme référence publique afin que d’autres groupes puissent développer et comparer des modèles améliorés. Avec un entraînement supplémentaire sur des formes vasculaires plus réalistes et des données d’entrée spécifiques aux patients, cette approche pourrait aider à transférer l’analyse sophistiquée du flux sanguin hors des laboratoires de supercalculateurs et dans les soins quotidiens des personnes porteuses d’anévrismes cérébraux.
Citation: Lannelongue, V., Garnier, P., Jeken-Rico, P. et al. Physics constrained graph neural network for real time prediction of intracranial aneurysm hemodynamics. npj Digit. Med. 9, 212 (2026). https://doi.org/10.1038/s41746-026-02404-z
Mots-clés: anévrisme cérébral, flux sanguin, réseau de neurones graphique, modélisation numérique, médecine numérique