Clear Sky Science · fr
Décoder l’axe immunorégulateur ERS–CAF via une IA multimodale et sa valeur pronostique et prédictive thérapeutique pan‑cancer
Observer les tumeurs sans scalpel
Les oncologues reconnaissent de plus en plus que ce qui entoure une tumeur peut compter autant que la tumeur elle‑même. Mais prélever à plusieurs reprises ce voisinage caché par biopsies est invasif et souvent peu pratique. Cette étude montre comment l’intelligence artificielle (IA) peut lire des examens médicaux courants et des images au microscope pour déduire des processus immunitaires et cicatriciels difficiles à mesurer à l’intérieur des tumeurs, transformant potentiellement l’imagerie de routine en une sorte de « biopsie numérique » applicable à différents cancers.
Les cellules de soutien cachées qui façonnent le cancer
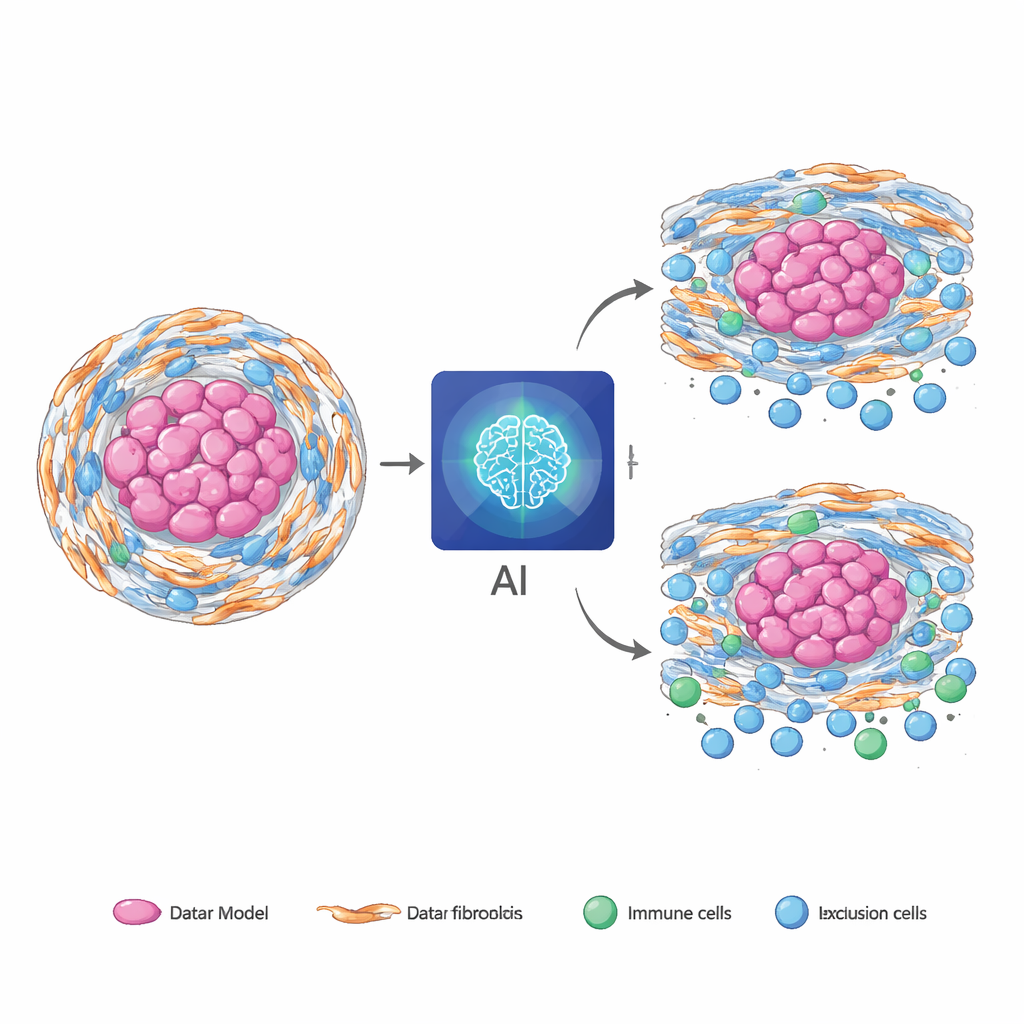
De nombreuses tumeurs solides sont enveloppées d’une coque dure et fibreuse produite par des cellules de soutien spécialisées appelées fibroblastes. Lorsque ces cellules subissent un stress au niveau de l’usine à protéines cellulaire (le réticulum endoplasmique), elles adoptent un état agressif qui favorise le cancer. Dans le chordome, un cancer osseux rare, ces fibroblastes stressés construisent une matrice dense et contribuent à exclure les cellules immunitaires, rendant les traitements moins efficaces. Des environnements fibrosés et pauvres en immunité similaires apparaissent dans d’autres cancers comme les tumeurs pancréatiques et colorectales, ce qui suggère que cette biologie n’est pas propre à une seule maladie. Le problème est que les méthodes actuelles pour mesurer ces fibroblastes stressés et leur comportement bloquant l’immunité reposent sur des échantillons tissulaires et des tests moléculaires complexes, difficiles à répéter et susceptibles de manquer des régions importantes de la tumeur.
Apprendre à l’IA à voir une biologie invisible
Les chercheurs se sont demandé si des IRM préopératoires standard et des lames d’histologie H&E de routine contiennent déjà des indices visuels sur cette barrière fibroblastique sous stress. Ils ont créé trois « scores de référence » numériques à partir du séquençage ARN tumoral : l’un capturant l’activité du programme de stress dans les fibroblastes, l’un résumant la force des signaux que ces cellules paraissent adresser aux cellules immunitaires, et un troisième décrivant la diversité des populations immunitaires et de soutien environnantes. Plutôt que de prédire des milliers de gènes, leur IA a été entraînée à prédire uniquement ces trois scores biologiquement signifiants à partir d’images. Pour cela, l’équipe a combiné deux branches : l’une analyse la texture et la forme sur l’IRM, l’autre balaye des milliers de petites régions dans la lame numérique et utilise un mécanisme d’attention guidé par le langage pour se concentrer sur les zones correspondant aux descriptions expertes de tissu fibrotique et pauvre en cellules immunitaires.
Mêler scans et lames pour des signaux plus forts
Sur 126 patients atteints de chordome avec IRM, lames d’anatomie pathologique, données ARN et suivi appariés, le modèle IA fusionné a surperformé les modèles utilisant uniquement l’IRM ou uniquement les lames. Ses prédictions des trois scores moléculaires concordaient étroitement avec les mesures basées sur l’ARN et sont restées bien calibrées entre différents hôpitaux et appareils d’imagerie. Lorsque des pathologistes ont marqué indépendamment des régions fibreuses et exclues immunitairement, les « points chauds » de l’IA se sont souvent allumés dans ces mêmes zones, suggérant qu’elle suivait une biologie réelle plutôt que la taille de la tumeur. Le modèle a aussi reflété le pronostic : des scores prédits plus élevés pour le stress des fibroblastes et la signalisation étaient associés à une survie plus mauvaise, tandis qu’une diversité micro‑environnementale prédite plus élevée offrait une protection partielle. L’ajout de ces scores dérivés de l’IA aux facteurs cliniques habituels améliorait la capacité à séparer les patients à haut et bas risque au fil du temps.
Du cancer rare aux cancers fréquents
Un test clé était de savoir si un modèle entièrement entraîné sur le chordome pouvait être utilisé « tel quel » dans d’autres cancers plus courants. Appliquée sans réentraînement à des tumeurs pancréatiques, gastriques et colorectales issues de larges jeux de données publiques, la version basée uniquement sur les lames montrait toujours une correspondance significative entre ses prédictions issues d’images et des scores ARN nouvellement calculés. Dans certains de ces cancers, les scores de l’IA amélioraient la prédiction de la survie des patients au‑delà des informations cliniques standard et aidaient à distinguer quels patients étaient plus susceptibles de bénéficier d’une chimiothérapie. Pour faciliter le déploiement là où la pathologie numérique est limitée, l’équipe a distillé le modèle multimodal complet en une version IRM‑seule qui conservait la majeure partie du pouvoir prédictif tout en s’exécutant plus rapidement et en consommant moins de ressources informatiques.
Ce que cela pourrait signifier pour les patients
Pris ensemble, les résultats soutiennent l’idée que les images médicales de routine codent discrètement des informations sur les cellules de soutien stressées, l’exclusion immunitaire et la diversité du microenvironnement — caractéristiques qui nécessitent normalement des tests moléculaires coûteux. Bien que le travail actuel soit rétrospectif et nécessite une validation prospective, il ouvre la voie à un avenir où un scanner et une lame standard peuvent, de façon non invasive, signaler les tumeurs dotées d’une barrière immunitaire fibrotique hostile, orienter les patients vers des tests complémentaires ou des traitements adaptés, et ce, pour plusieurs types de cancer sans charge supplémentaire pour les patients.
Citation: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Mots-clés: microenvironnement tumoral, imagerie du cancer, intelligence artificielle, fibroblastes, immunothérapie