Clear Sky Science · fr
Prise de décision algorithmique des antibiotiques dans les infections urinaires en utilisant la prédiction, informée par le prescripteur, de l’utilité du traitement
Des antibiotiques plus intelligents pour des infections courantes
Les infections urinaires (IU) figurent parmi les raisons les plus fréquentes de prescription d’antibiotiques. Pourtant, choisir le bon médicament est un exercice d’équilibre : il faut éradiquer l’infection, éviter des effets indésirables graves et protéger la collectivité contre l’aggravation de la résistance aux antibiotiques. Cette étude présente un nouvel algorithme d’aide à la décision qui vise à soutenir les cliniciens en combinant de vastes données hospitalières et les priorités réelles des médecins, afin d’aider à sélectionner des antibiotiques à la fois efficaces pour le patient et plus sûrs pour la communauté.
Le problème des médicaments puissants
La médecine moderne dépend des antibiotiques, mais la surutilisation d’agents à large spectre, les « gros calibres », alimente une crise mondiale de résistance aux antimicrobiens. Les Nations unies ont fixé un objectif : d’ici 2030, 70 % de l’utilisation mondiale d’antibiotiques devrait provenir de médicaments de première intention plus étroits, appelés antibiotiques « Access » par l’Organisation mondiale de la Santé. En pratique, de nombreux cliniciens s’orientent vers des médicaments plus larges, classés « Watch » ou « Reserve », parce qu’ils craignent qu’une option plus étroite n’échoue face à des bactéries résistantes, surtout lorsque les patients sont très malades. En conséquence, on sacrifie souvent les risques de résistance à long terme pour une tranquillité d’esprit à court terme, faute d’outils clairs permettant d’évaluer quand un médicament plus sûr et plus ciblé fonctionnerait tout aussi bien.
Apprendre à un algorithme à penser comme un clinicien
Les chercheurs ont développé un algorithme de décision antibiotique centré sur les IU en utilisant des dossiers électroniques détaillés de près de 94 000 patients hospitalisés à Boston. D’abord, ils ont entraîné des modèles prédictifs pour estimer, pour 13 antibiotiques différents, la probabilité que les bactéries responsables des IU soient sensibles, et la probabilité que le traitement provoque des problèmes tels qu’une infection à Clostridioides difficile ou une toxicité médicamenteuse grave. Ensuite, ils ont demandé à 49 cliniciens britanniques de diverses spécialités de réaliser un exercice de classement en ligne, choisissant entre des antibiotiques fictifs différant par des caractéristiques comme le risque d’effets indésirables, l’adéquation pour les IU, le coût, la catégorie Access ou Watch/Reserve, et la forme orale ou intraveineuse. En analysant ces classements, l’équipe a quantifié l’importance que les médecins accordent à chaque caractéristique : par exemple, combien ils préféraient des traitements oraux, axés sur les IU et à faible toxicité plutôt que des options plus risquées ou plus puissantes.
Ajouter un filet de sécurité pour les patients très malades
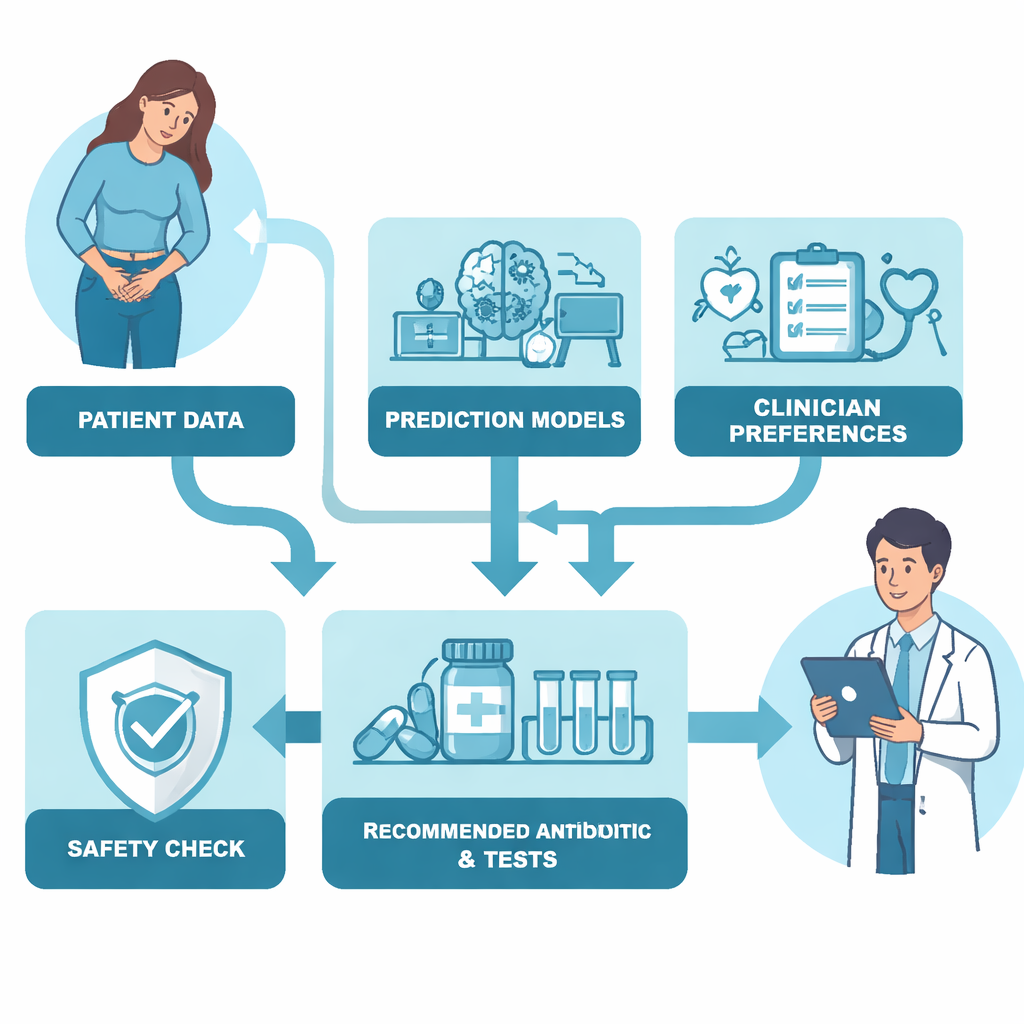
L’algorithme final a combiné ces deux ingrédients : des prédictions basées sur les données et des jugements de valeur des cliniciens. Pour chaque patient, il calculait une « valeur de traitement » pour chaque antibiotique, tenant compte de la probabilité prédite d’efficacité, du risque d’effets indésirables graves, de sa catégorie Access/Watch/Reserve et de sa voie d’administration (orale ou intraveineuse). De manière cruciale, l’algorithme intégrait aussi un mécanisme de sécurité fondé sur la sévérité de l’état du patient à l’arrivée aux urgences. À mesure que la gravité croissait, l’algorithme mettait automatiquement davantage l’accent sur l’intensité du traitement et sur la disponibilité d’une option intraveineuse. Autrement dit, pour les patients peu malades il favorisait les antibiotiques étroits et oraux, mais à mesure que l’état s’aggravait il devenait progressivement plus enclin à utiliser des antibiotiques puissants et intraveineux afin d’éviter un échec thérapeutique.
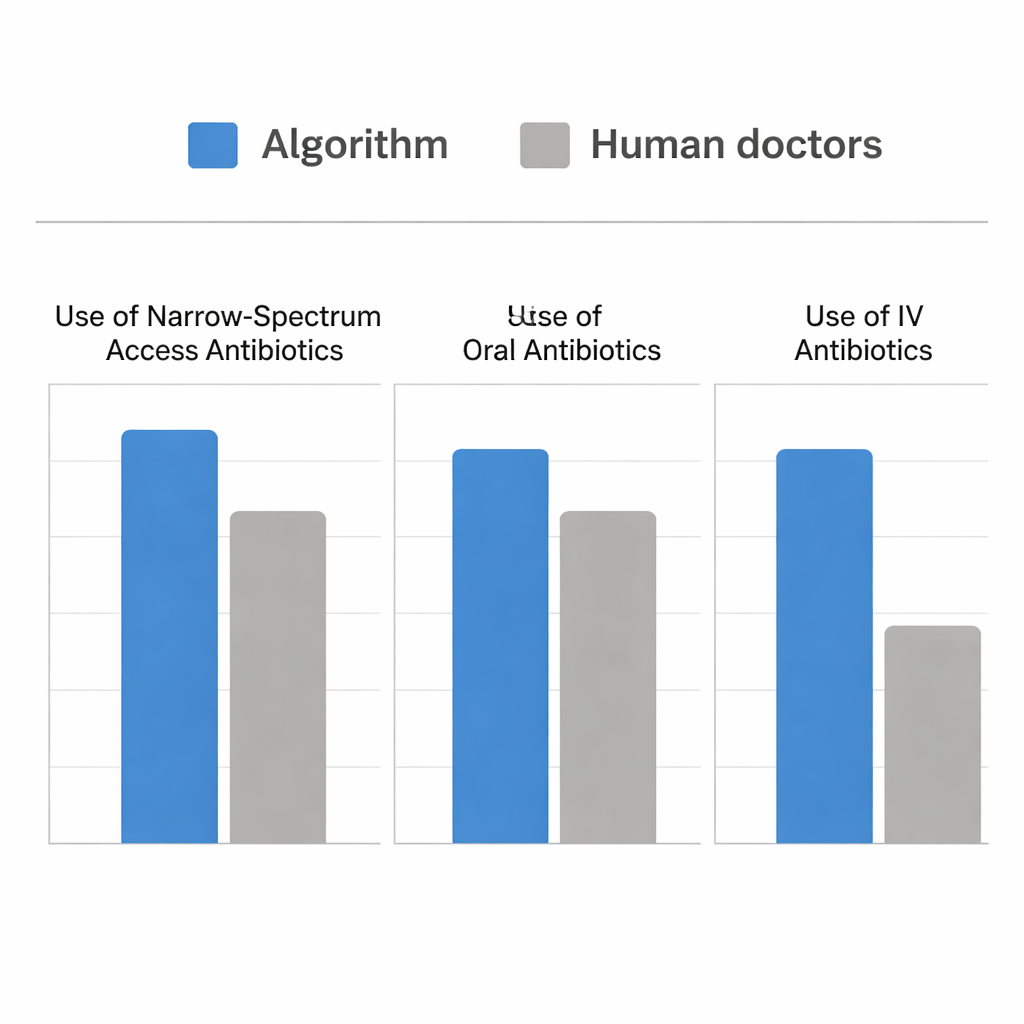
Comment l’algorithme s’est mesuré aux médecins
L’équipe a ensuite réalisé une simulation à partir de cas réels aux urgences où les patients présentaient des IU et des cultures d’urine. Ils ont comparé les antibiotiques réellement prescrits par les cliniciens avec ceux que l’algorithme aurait choisis au moment de l’envoi de la culture. Les deux approches étaient à peu près équivalentes pour sélectionner un antibiotique couvrant la bactérie du patient. Cependant, l’algorithme y parvenait tout en choisissant beaucoup plus d’antibiotiques de la catégorie étroite Access et beaucoup plus de traitements oraux, et en utilisant moins d’antibiotiques intraveineux. Pour les patients plus gravement atteints, l’algorithme se comportait comme les prescripteurs humains, basculant de façon appropriée vers des médicaments intraveineux et plus puissants. Là où il différait, c’était dans sa capacité à repérer des opportunités supplémentaires — notamment chez les patients modérément malades — pour traiter en toute sécurité par voie orale avec des médicaments de catégorie Access comme la nitrofurantoïne ou l’ampicilline-sulbactam, plutôt que d’avoir recours par défaut à des options plus larges.
Ce que cela signifie pour les soins quotidiens
Pour un lecteur non spécialiste, le message essentiel est que ce système ne remplace pas les médecins ; il fonctionne plutôt comme une calculatrice pour des compromis risques–bénéfices complexes que les cliniciens cherchent déjà à évaluer mais ne peuvent pas toujours calculer précisément de tête. En mariant les priorités des cliniciens et les données massives sur la performance des antibiotiques, l’algorithme peut suggérer des traitements tout aussi efficaces pour les patients individuels mais plus respectueux du corps et de la santé publique — privilégiant les comprimés aux perfusions lorsque c’est sûr, et les médicaments plus ciblés plutôt que les derniers recours chaque fois que possible. Si ces outils sont validés dans d’autres contextes, ils pourraient aider les hôpitaux et les systèmes de santé à se rapprocher des objectifs mondiaux d’utilisation responsable des antibiotiques, sans compromettre la sécurité des personnes qui arrivent gravement malades avec une infection.
Citation: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Mots-clés: infection urinaire, stewardship des antibiotiques, aide à la décision clinique, résistance aux antimicrobiens, apprentissage automatique en médecine