Clear Sky Science · fr
Reconstruction 3D et quantification de la microvascularisation rétinienne sans annotations par RADAR
Voir la santé à travers le fond de l’œil
Les minuscules vaisseaux sanguins au fond de nos yeux font bien plus que nourrir la rétine. Parce qu’on peut les observer de manière non invasive, ils servent de carte vivante des petits vaisseaux du corps, offrant des indices précoces sur des affections comme le diabète, les maladies rénales et les problèmes cardiaques. Cette étude présente une nouvelle méthode informatique, appelée RADAR, qui transforme les données d’imagerie oculaire en modèles tridimensionnels détaillés de ces vaisseaux minuscules — sans dépendre d’annotations humaines chronophages ni d’un entraînement d’intelligence artificielle fragile. 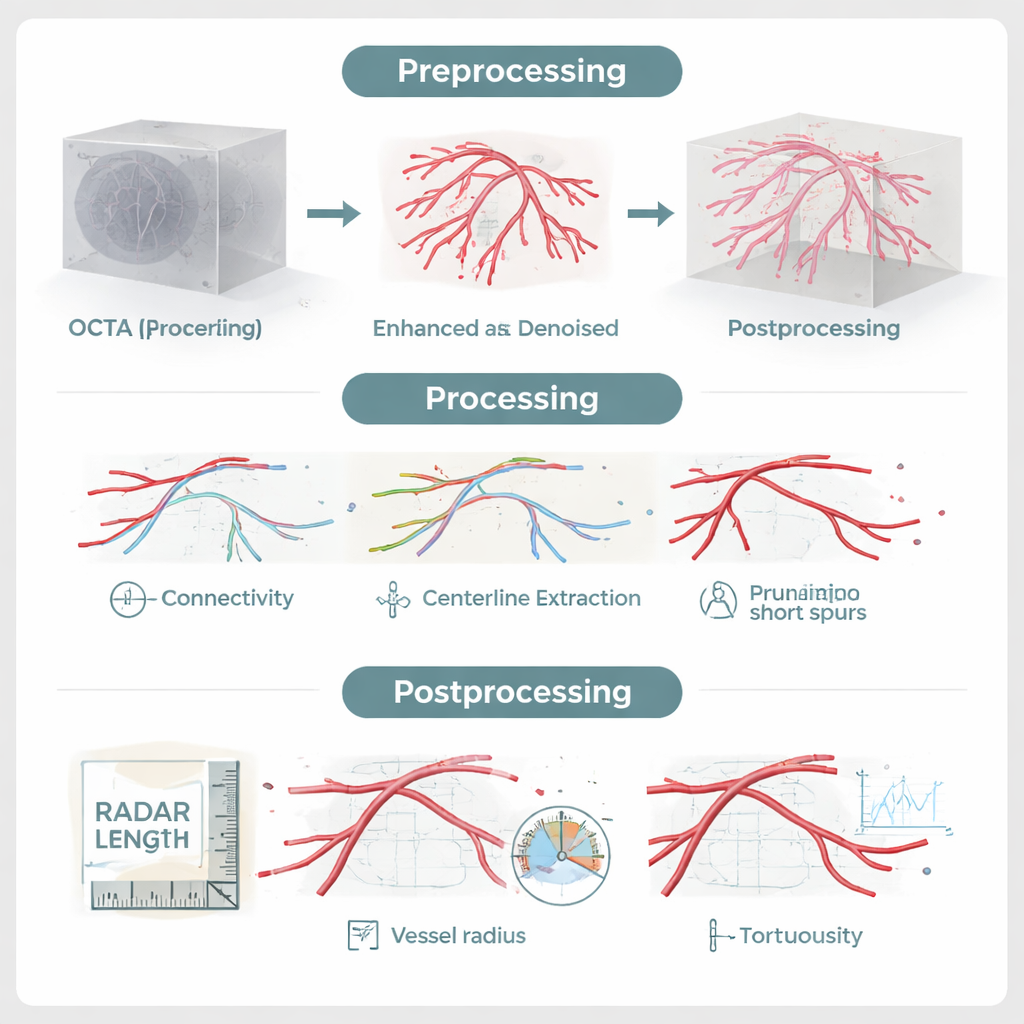
Pourquoi les images plates masquent des indices importants
Les appareils modernes d’angiographie par tomographie par cohérence optique (OCTA) peuvent capturer un volume 3D complet du flux sanguin rétinien. Pourtant, en clinique, ces jeux de données riches sont en général compressés en images planes, vues de dessus. Lorsque toutes les couches de vaisseaux sont aplaties sur un seul plan, des structures situées à différentes profondeurs se superposent, de petits intervalles sont masqués et une perte subtile de capillaires peut disparaître. C’est une limitation sérieuse, car les dommages précoces dus au diabète et à d’autres maladies commencent souvent dans les capillaires les plus fins bien avant que des signes évidents de rétinopathie ou une perte de vision n’apparaissent.
Une carte fondée sur la physique, pas sur des conjectures
Les tentatives récentes pour extraire le réseau vasculaire des scans OCTA ont majoritairement recours à l’apprentissage profond, où des réseaux neuronaux apprennent des motifs à partir de milliers d’exemples préalablement annotés. Ces approches peuvent bien fonctionner mais présentent des inconvénients : elles exigent de larges jeux de données annotés avec soin, peuvent échouer lorsque l’appareil ou le protocole d’imagerie change, et se comportent souvent comme une « boîte noire ». RADAR emprunte une autre voie. C’est une chaîne de traitement basée sur un modèle qui encode la façon dont les vaisseaux doivent apparaître et se comporter en trois dimensions — des tubes continus et courbés qui se ramifient et se reconnectent — plutôt que d’essayer d’apprendre tout à partir des données. Un filtre de débruitage spécialisé renforce les signaux des structures tubulaires tout en préservant leurs courbures, et une étape de connectivité utilise des chemins fondés sur des probabilités pour combler les ruptures causées par le bruit ou le mouvement, guidée par la direction locale des vaisseaux plutôt que par de simples seuils de luminosité.
Des amas de pixels à des réseaux mesurables
Une fois les vaisseaux améliorés et reconnectés, RADAR extrait leur « squelette » central, identifie les points de branchement et les extrémités, et élagage les petites excroissances probablement artéfactuelles. Il en résulte un graphe 3D propre de la circulation rétinienne. À partir de ce modèle, le logiciel peut mesurer directement des caractéristiques d’intérêt clinique : le nombre de segments vasculaires, leur longueur totale et leur surface, la largeur moyenne et leur tortuosité. Surtout, il peut effectuer ces mesures séparément pour les couches superficielles, moyennes et profondes de la rétine, après avoir aligné le réseau vasculaire sur l’anatomie rétinienne de l’individu. La validation par rapport à des tracés 3D manuels minutieux a montré que les segmentations de RADAR sont très précises, et l’ensemble du processus — du scan brut à l’ensemble complet de mesures — demande environ six minutes par œil. 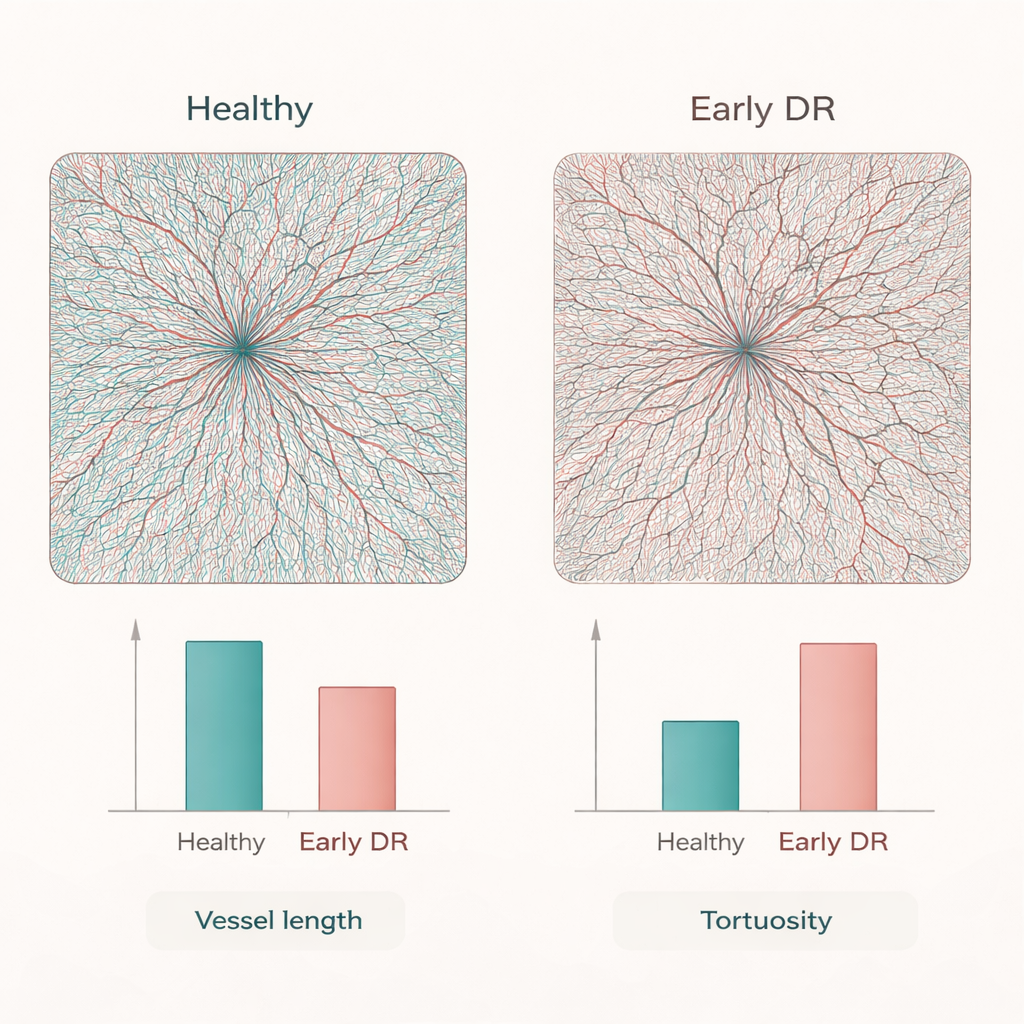
Ce qui change dans les premiers stades des atteintes rétiniennes diabétiques
Pour évaluer sa valeur en conditions réelles, les chercheurs ont appliqué RADAR à des scans OCTA de 50 adultes sains et 50 patients présentant une rétinopathie diabétique précoce. Sur les images planes standard, les deux groupes semblaient similaires. En revanche, les reconstructions 3D ont révélé que les yeux diabétiques présentaient déjà moins de segments vasculaires, des segments plus courts, une surface vasculaire totale réduite et davantage d’extrémités avec moins de points de branchement — signes d’une perte de capillaires et d’un réseau simplifié. Parallèlement, les vaisseaux restants, en particulier les plus petits, étaient plus tortueux. En condensant ces changements en métriques faciles à interpréter, comme le rapport segments/points de branchement ou les patrons de tortuosité selon la taille des vaisseaux, RADAR a mis au jour un remaniement lié à la maladie qui serait probablement manqué par les méthodes 2D actuelles.
Ce que cela pourrait signifier pour les patients
Pour les non‑spécialistes, le message clé est que cette technique transforme les scans oculaires en une carte 3D très détaillée des plus petits vaisseaux, révélant des lésions précoces bien avant que la vision ne soit affectée. Parce qu’elle ne dépend pas d’annotations humaines ni d’un réentraînement pour chaque nouvel appareil, RADAR pourrait être déployée à grande échelle dans les cabinets pour suivre la santé microvasculaire au fil du temps, aider les médecins à détecter plus tôt la maladie oculaire liée au diabète et potentiellement signaler un risque de problèmes cardiovasculaires plus larges. À long terme, ces « empreintes vasculaires » 3D issues de l’œil pourraient devenir des marqueurs de routine guidant la prévention et le traitement bien avant l’apparition de dommages irréversibles.
Citation: Zhang, H., Liu, X., Wu, J. et al. Annotation-free 3D reconstruction and quantification of retinal microvasculature by RADAR. npj Digit. Med. 9, 181 (2026). https://doi.org/10.1038/s41746-026-02366-2
Mots-clés: microvascularisation rétinienne, OCTA, reconstruction 3D, rétinopathie diabétique, biomarqueurs vasculaires