Clear Sky Science · fr
DARE-FUSE : apprentissage guidé par des preuves alignées sur le domaine pour la segmentation et la classification conjointes des tumeurs cérébrales en IRM
Pourquoi des scanners cérébraux plus intelligents comptent
Les tumeurs cérébrales figurent parmi les diagnostics les plus redoutés en médecine, et l'imagerie par résonance magnétique (IRM) est l'outil principal que les médecins utilisent pour voir où commence et où se termine une tumeur. Pourtant, même des radiologues experts peinent parfois à délimiter précisément une tumeur et à juger son évolution au fil du temps, notamment quand ses contours se confondent avec un tissu cérébral enflé. Cet article présente DARE-FUSE, un nouveau système d'intelligence artificielle conçu pour lire les IRM cérébrales de façon plus fiable, tracer des limites tumorales plus nettes et fournir des explications plus claires de ses décisions afin d'aider les chirurgiens, oncologues et patients.
Contours flous et services débordés
Dans les hôpitaux réels, les IRM cérébrales sont imparfaites. Les tumeurs se fondent souvent dans l'œdème environnant, des implants métalliques peuvent déformer l'image, et chaque centre utilise des réglages de scan légèrement différents. Les radiologues doivent faire défiler manuellement des centaines d'images, repérer la tumeur image par image, puis conclure sur son comportement. Ce travail est long, fatigant et sujet à des désaccords entre experts. Les outils d'IA existants peuvent aider à tracer les tumeurs ou à étiqueter les images en « tumeur » ou « pas de tumeur », mais la plupart traitent ces tâches séparément, et beaucoup échouent lorsque les images proviennent de nouveaux centres ou présentent une croissance marginale subtile et irrégulière.
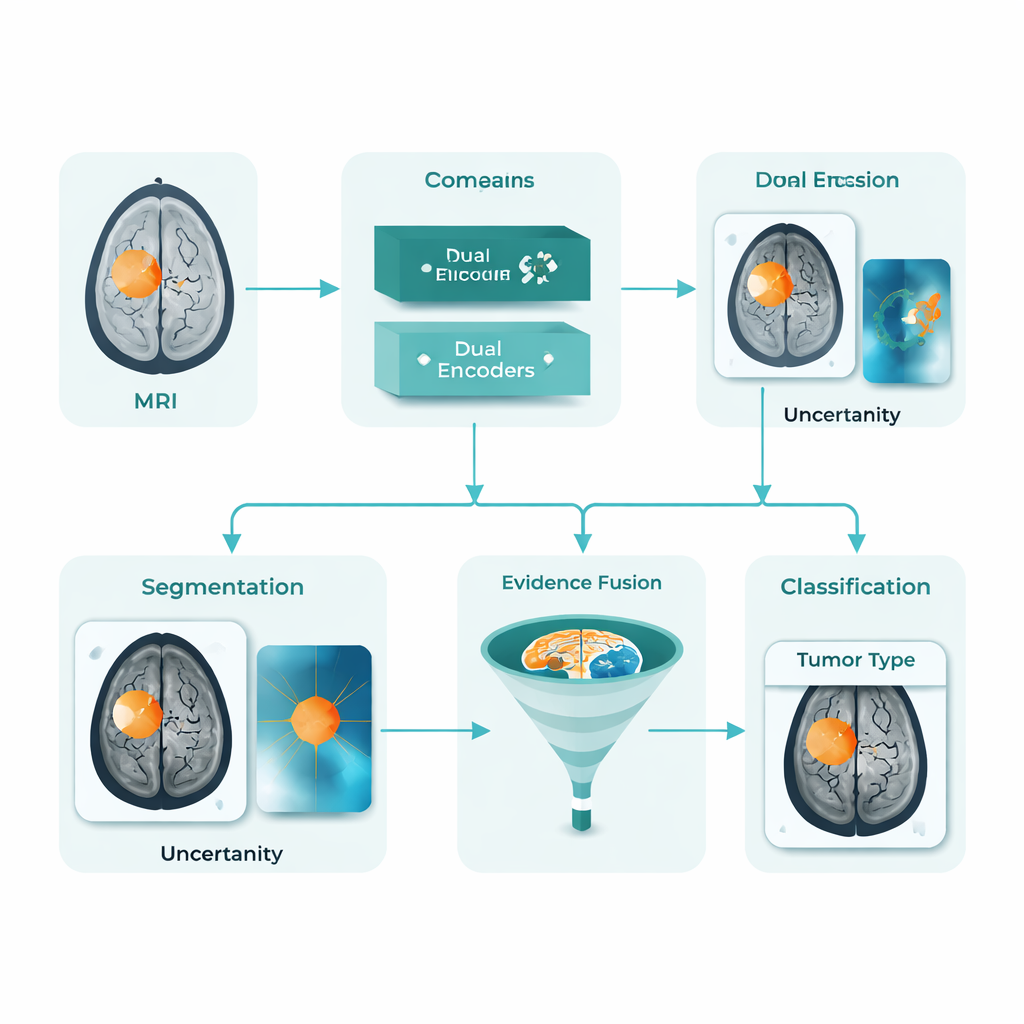
Un assistant IA unifié pour cartes tumorales et étiquettes
DARE-FUSE relève simultanément plusieurs de ces défis. Il est conçu comme une seule chaîne qui trace la tumeur sur chaque coupe IRM (segmentation) et classe les images entières en groupes diagnostiques (classification). Au cœur du système se trouvent deux « vues » coopérantes : un réseau adapté aux formes et aux contours détaillés, et un autre dédié aux motifs globaux qui distinguent les différents types de tumeurs. Un module d'alignement spécifique maintient la cohérence de ces vues entre hôpitaux et appareils, de sorte que les caractéristiques apprises sur un jeu de données ne dégradent pas les performances sur un autre. Le système estime également sa propre incertitude, signalant les zones où il est moins sûr du contour exact de la tumeur—ce qui est essentiel pour un usage clinique sûr.
Utiliser des indices issus de cartes de chaleur et de reconstructions « sans tumeur »
Plutôt que de se fier à un seul signal, DARE-FUSE apprend à partir de plusieurs types de preuves. Une branche produit des cartes de chaleur, montrant quelles parties du cerveau soutiennent le plus fortement la décision de classification de l'IA. Une autre branche utilise un modèle génératif pour imaginer à quoi ressemblerait le même scan si la tumeur avait été retirée, puis compare cette version « sans tumeur » à l'original. Les différences entre les deux mettent en évidence des modifications structurelles et des bords subtils qui pourraient ne pas ressortir fortement sur une carte de chaleur standard. Un module de fusion combine ensuite ces indices en une carte continue de « prior_tumeur » : les régions où plusieurs sources convergent sont traitées comme cœur tumoral, tandis que les régions moins certaines sont ajoutées plus prudemment et atténuées lorsque l'incertitude du modèle est élevée. Ce prior fusionné guide le contour final, aidant à éviter à la fois des poches tumorales manquées et des îlots spurieux dans le tissu sain.
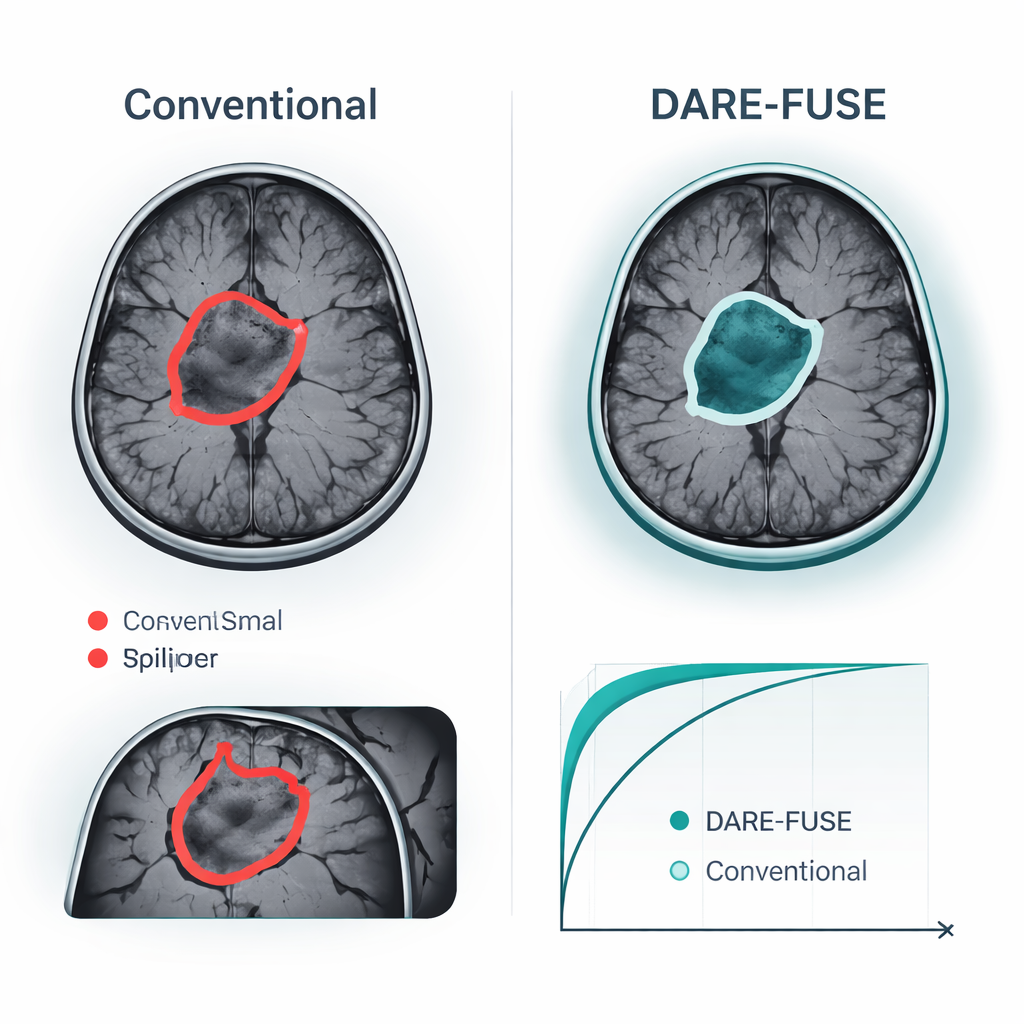
Améliorations prouvées sur des jeux de données publics de tumeurs cérébrales
Les auteurs ont testé DARE-FUSE sur six grands concours multicentriques de tumeurs cérébrales (la série BraTS) et quatre collections publiques d'IRM utilisées pour la classification au niveau de l'image. Sur toutes les éditions de BraTS, le système a égalé ou dépassé les meilleurs modèles récents d'apprentissage profond, obtenant un chevauchement légèrement supérieur entre ses masques tumoraux prédits et les dessins d'experts, et des erreurs systématiquement plus faibles sur la surface tumorale mesurée. Ces gains étaient les plus marqués dans les cas difficiles : petites tumeurs, contours à faible contraste et formes complexes, irrégulières. Dans les tâches de classification—décider, par exemple, si un scan montre un gliome, un méningiome, une tumeur hypophysaire ou l'absence de tumeur—DARE-FUSE a également surpassé des baselines fortes basées sur des transformers et des approches faiblement supervisées en précision et sur une mesure standard de discrimination (AUC). Fait important, lorsque les chercheurs ont artificiellement réduit le nombre d'annotations détaillées, le nouveau système a décliné avec élégance et a conservé un avantage sur les concurrents semi-supervisés et faiblement supervisés.
Ce que cela pourrait signifier pour les patients
Pour les patients et les cliniciens, la principale promesse de DARE-FUSE n'est pas un algorithme spectaculaire, mais un soutien d'imagerie plus fiable et interprétable. En pratique, le système pourrait proposer un contour tumoral, mettre en évidence les régions où il est moins confiant et afficher des cartes de chaleur expliquant quelles zones de l'image motivent sa classification. Les médecins pourraient accepter les régions à faible incertitude comme contour de départ, puis concentrer leur attention sur les zones signalées plutôt que de tout redessiner. Des mesures de volume et de forme tumorale plus précises et cohérentes pourraient améliorer la planification du traitement, le ciblage en radiothérapie et le suivi de la réponse au fil du temps. Si les auteurs soulignent que leur outil est un assistant—et non un remplaçant—du jugement expert, leurs résultats ouvrent la voie à des systèmes d'IA qui voient les tumeurs plus clairement et communiquent leur degré de confiance de manière exploitable par les cliniciens.
Citation: Liu, Y., Sun, C., Niu, Y. et al. DARE-FUSE: domain aligned evidence guided learning for joint brain tumor MRI segmentation and classification. npj Digit. Med. 9, 178 (2026). https://doi.org/10.1038/s41746-026-02365-3
Mots-clés: IRM de tumeur cérébrale, segmentation d'images médicales, apprentissage profond en radiologie, support à la décision clinique, IA consciente de l'incertitude