Clear Sky Science · fr
Cadre collaboratif piloté par des LLM pour l’évaluation et la prise en charge de la douleur cancéreuse enrichies par la connaissance
Pourquoi des soins de la douleur plus intelligents comptent
La douleur liée au cancer n’est pas seulement un effet indésirable désagréable : elle peut dominer les derniers mois ou années d’une personne, rendant le sommeil, le mouvement et même de simples conversations difficiles. Bien que des analgésiques puissants existent, les utiliser en toute sécurité et efficacement est complexe, surtout lorsque le cancer, les comorbidités et les traitements varient d’un patient à l’autre. Cet article décrit OncoPainBot, un nouveau cadre d’intelligence artificielle fondé sur des grands modèles de langage (LLM) qui vise à aider les médecins à trier des dossiers complexes, suivre des recommandations à jour et concevoir des plans analgésiques plus sûrs et personnalisés pour les personnes atteintes de cancer.
Un problème difficile dans les soins oncologiques quotidiens
La douleur chez les personnes atteintes de cancer a de multiples origines : tumeurs comprimant les os ou les nerfs, interventions chirurgicales, chimiothérapie et radiothérapie. Jusqu’à 70 % des personnes atteintes d’un cancer avancé vivent avec une douleur significative, mais le soulagement reste souvent incomplet. Les cliniciens doivent composer avec les opioïdes, les médicaments non opioïdes et les traitements adjuvants tout en surveillant les effets indésirables dangereux, en particulier chez les patients ayant une fonction hépatique ou rénale fragile. Les outils d’évaluation actuels reposent largement sur de courtes échelles et des notes en texte libre, qui varient d’un praticien à l’autre et d’un établissement à l’autre. Par conséquent, les décisions thérapeutiques peuvent être très hétérogènes et des occasions d’améliorer le confort peuvent être manquées.
Transformer le texte médical en information exploitable
Les LLM comme ChatGPT et Claude peuvent lire et résumer des documents longs et désordonnés, ce qui les rend attractifs pour des usages médicaux. Mais les « chatbots » ordinaires sont dangereux pour la prise en charge de la douleur cancéreuse car ils peuvent inventer des détails, omettre des interactions médicamenteuses ou ignorer les recommandations les plus récentes. OncoPainBot traite ces problèmes en combinant des LLM avec une base de connaissances curatée construite à partir des lignes directrices des principales organisations en oncologie, et en répartissant le travail entre quatre « agents » coopérants, chacun reproduisant un rôle clinique réel. Un agent extrait les faits clés sur la douleur d’un patient à partir des dossiers électroniques, un autre raisonne sur le type de douleur présent, un troisième propose un plan de traitement, et un quatrième effectue une vérification de sécurité axée sur les interactions médicamenteuses, la fonction des organes et les besoins de surveillance.
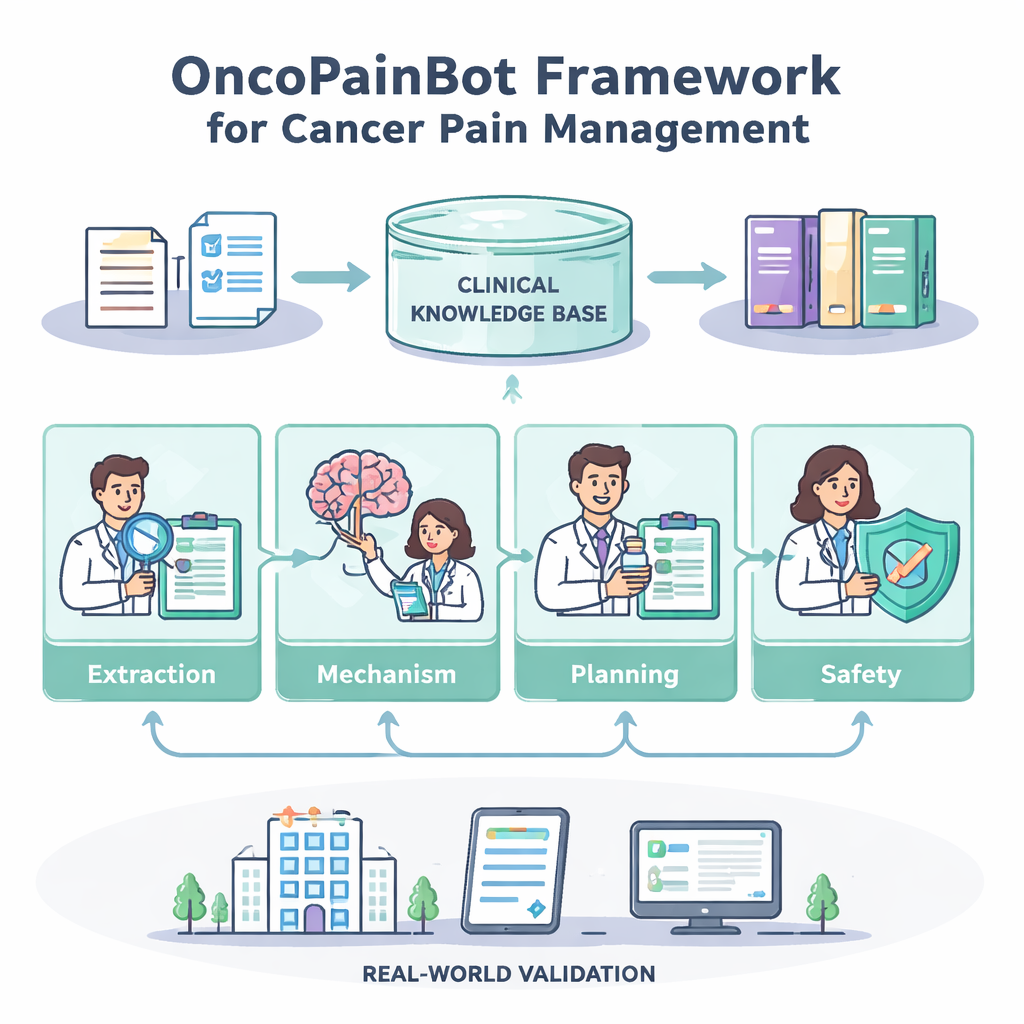
Comment fonctionne l’équipe de quatre agents
L’agent d’extraction de la douleur lit les notes en texte libre et les transforme en un tableau structuré : localisation de la douleur, intensité perçue, facteurs aggravants ou soulageants, et médicaments déjà essayés. L’agent de raisonnement sur le mécanisme de la douleur utilise ensuite ce tableau pour déduire si la douleur provient principalement d’une lésion tissulaire, d’une atteinte nerveuse ou d’un mélange des deux — un indice important pour le choix des médicaments. Ensuite, l’agent de planification du traitement consulte la base de connaissances basée sur les recommandations via une technique appelée génération augmentée par récupération, qui permet au modèle d’intégrer des extraits précis et à jour plutôt que de s’appuyer sur sa mémoire seule. Il propose des plans par étapes — souvent ancrés sur « l’échelle de la douleur » de l’Organisation mondiale de la santé — incluant doses initiales, modalités d’ajustement et doses de secours pour les poussées douloureuses. Enfin, l’agent de vérification de la sécurité agit comme un pharmacien prudent, recherchant des problèmes de dosage, des combinaisons risquées et des analyses manquantes, et signalant les cas où les données sont trop insuffisantes pour étayer une recommandation ferme.
Mettre le système à l’épreuve
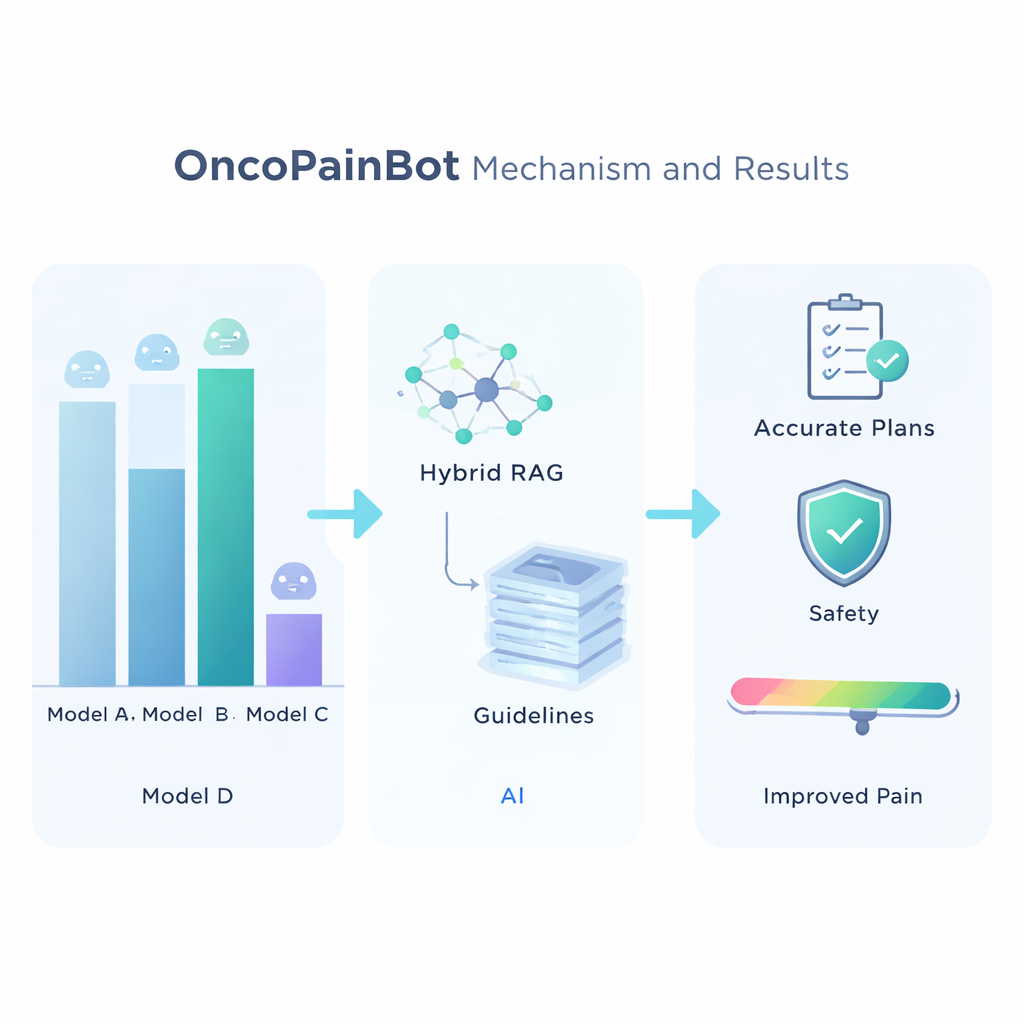
Pour choisir le meilleur modèle de langage sous-jacent, les chercheurs ont comparé sept systèmes de pointe sur plusieurs tests de questions-réponses médicales. Claude 4 s’est avéré le plus précis, bien que pas le plus rapide, et a donc été choisi comme « cerveau » d’OncoPainBot. Ils ont ensuite évalué différentes façons de connecter ce cerveau à la bibliothèque de recommandations et constaté qu’une stratégie de récupération « hybride » — combinant recherche par mots-clés et recherche sémantique plus profonde — fournissait les réponses les plus fiables. Avec cette configuration, l’équipe a exécuté OncoPainBot sur 516 dossiers réels de douleur cancéreuse issus d’un grand hôpital chinois. Les rapports écrits du système correspondaient étroitement aux notes des cliniciens tant sur le plan linguistique que sur le contenu, et ses suggestions de prise en charge de la douleur étaient en accord avec les prescriptions réelles des médecins dans environ 84 % des cas. Fait important, la plupart des discordances provenaient de nuances subtiles spécifiques au patient — comme une tolérance aux opioïdes non documentée ou une insuffisance organique complexe — plutôt que d’erreurs manifestes de choix médicamenteux.
Ce que cela pourrait signifier pour les patients
Pour les personnes vivant avec un cancer, la promesse d’OncoPainBot n’est pas qu’une machine prenne en charge leur traitement, mais qu’elle fournisse à leur équipe soignante un second avis plus précis et plus cohérent. Le cadre est conçu comme un outil « clinicien dans la boucle » : il met en évidence des caractéristiques de la douleur qui pourraient rester cachées dans les notes, suggère des options conformes aux recommandations et signale des problèmes de sécurité, tout en laissant les décisions finales aux médecins. Les auteurs soulignent que leur travail en est encore à un stade précoce et rétrospectif et n’a été testé que dans un seul centre : des essais en temps réel dans plusieurs hôpitaux sont encore nécessaires. Néanmoins, leurs résultats suggèrent qu’une IA soigneusement conçue — fondée sur des preuves solides et un raisonnement transparent — pourrait contribuer à standardiser la prise en charge de la douleur cancéreuse, réduire les erreurs dangereuses de posologie et, surtout, faire en sorte que les patients passent moins de temps à souffrir et davantage à vivre leur vie.
Citation: Liu, H., Hu, Y., Li, D. et al. LLM-driven collaborative framework for knowledge-enhanced cancer pain assessment and management. npj Digit. Med. 9, 180 (2026). https://doi.org/10.1038/s41746-026-02362-6
Mots-clés: prise en charge de la douleur cancéreuse, assistant à la décision clinique, grands modèles de langage, thérapie par opioïdes, génération augmentée par récupération