Clear Sky Science · fr
Application et perspectives de l’intelligence artificielle dans l’imagerie diagnostique du cancer de la prostate
Pourquoi des examens plus intelligents comptent pour la santé des hommes
Le cancer de la prostate est l’un des cancers les plus fréquents chez l’homme, et le détecter tôt peut faire la différence entre un problème de santé mineur et une maladie potentiellement mortelle. Cette revue explique comment l’intelligence artificielle (IA) s’intègre aux examens médicaux modernes pour repérer le cancer de la prostate plus tôt, évaluer sa gravité et suivre l’efficacité des traitements. Pour le lecteur, elle offre une fenêtre sur la façon dont les ordinateurs deviennent des partenaires discrets en salle de lecture, aidant les médecins à prendre des décisions plus rapides et plus cohérentes tout en posant de nouvelles questions sur les données, l’équité et la confiance.
Des ombres floues à des images riches en données
Les médecins s’appuient sur plusieurs outils d’imagerie pour rechercher le cancer de la prostate. L’échographie est rapide et peu coûteuse mais peine à différencier le cancer d’une hypertrophie bénigne ou d’une inflammation. L’imagerie par résonance magnétique (IRM) offre des vues détaillées des tissus mous et est désormais l’examen de référence pour les cancers de la prostate cliniquement significatifs, mais son interprétation prend du temps et même les experts sont souvent en désaccord. Les PET/CT, utilisant des traceurs qui se lient à une protéine appelée PSMA sur les cellules cancéreuses, excellent pour repérer les métastases osseuses et ganglionnaires, mais peuvent manquer de très petites lésions et sont coûteux. L’IA ne remplace pas ces appareils ; elle s’appuie sur les images qu’ils produisent. Les algorithmes nettoient et segmentent d’abord les examens, puis extraient des motifs subtils de luminosité, de texture et de forme. Ces indices invisibles, combinés à des résultats biologiques comme le taux de PSA sanguin, servent à entraîner des modèles capables de signaler des zones suspectes, d’estimer le risque de cancer et de suggérer où faire une biopsie ou comment évaluer la réponse au traitement.
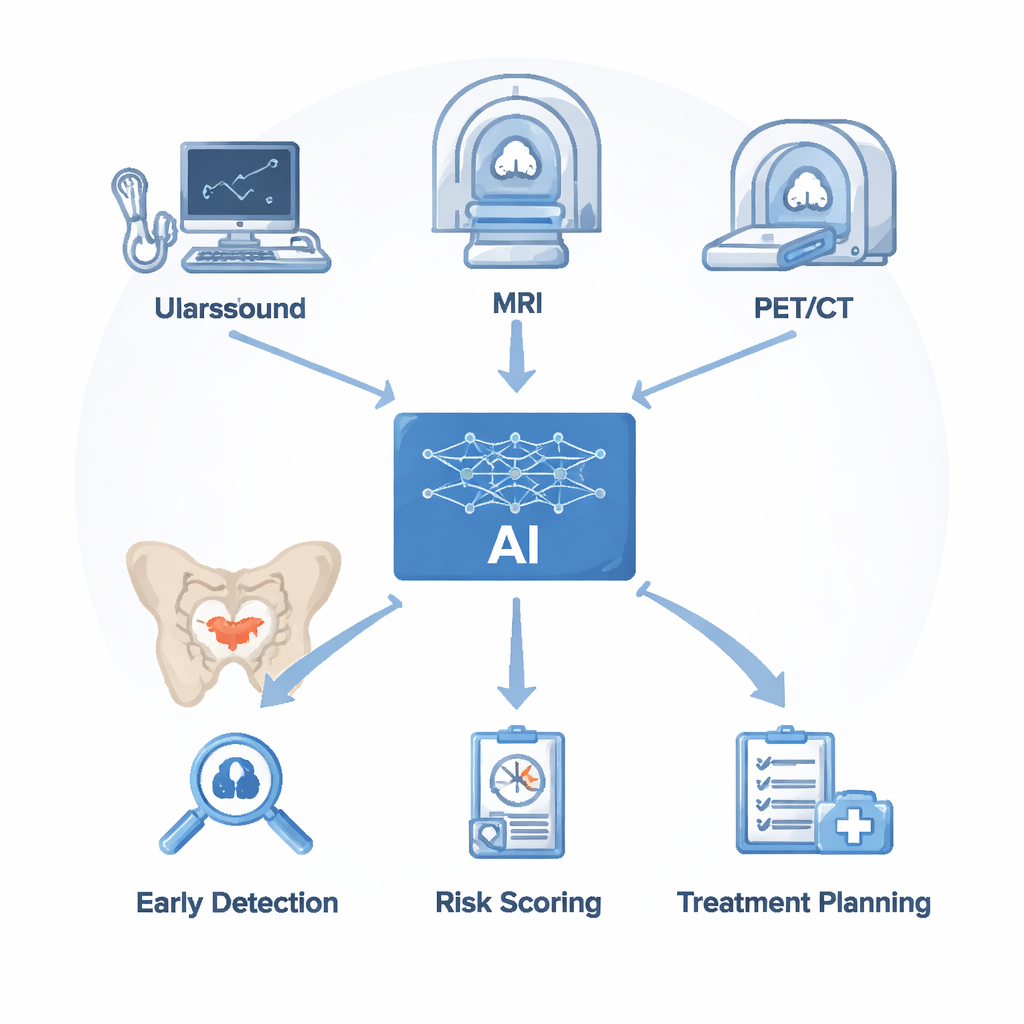
Apprendre aux ordinateurs à voir ce que les radiologues manquent
En échographie, les systèmes d’IA apprennent à partir de centaines d’exemples à repérer des régions cancéreuses qui peuvent se fondre dans le bruit de fond. Les modèles de deep learning peuvent localiser automatiquement la prostate et surligner les tumeurs probables en temps réel, parfois à la hauteur ou au-delà des échographistes expérimentés, tout en conservant la rapidité et en réduisant les petites lésions manquées. Les approches de radiomique vont plus loin en convertissant les images échographiques en grands ensembles de nombres capturant des motifs tissulaires trop complexes pour l’œil humain. Les modèles d’apprentissage machine construits sur ces caractéristiques ont nettement surpassé l’échographie traditionnelle et le seul PSA, en particulier chez les hommes dont le PSA se situe dans la zone grise où les méthodes anciennes classent à tort près de la moitié des cas. Des idées similaires alimentent l’IA sur l’IRM, où des réseaux avancés délimitent automatiquement la prostate et ses zones internes, réduisant le contouring manuel d’environ 20 minutes à un peu plus d’une minute et améliorant significativement la concordance entre lecteurs.
Estimations de risque plus précises et suivi du traitement plus intelligent
L’IA brille surtout lorsqu’elle rassemble des informations issues de multiples séquences d’IRM montrant l’anatomie, le mouvement de l’eau et le flux sanguin. Des modèles basés sur les transformers, adaptés du traitement du langage, fusionnent ces entrées pour produire des cartes de probabilité des tumeurs cliniquement importantes. Testés sur de larges cohortes, ces systèmes ont égalé ou dépassé des radiologues seniors, en particulier pour les petites tumeurs de moins d’un centimètre que l’humain néglige souvent. Sur l’IRM dynamique de contraste, des modèles séries temporelles lisent les courbes de variation de luminosité du produit injecté pour estimer la perméabilité des vaisseaux tumoraux — un indicateur lié à une maladie plus agressive et à un risque de récidive plus élevé. En PSMA PET/CT, des réseaux tridimensionnels entraînés sur des examens corps entier détectent automatiquement les métastases osseuses et ganglionnaires, mesurent la charge tumorale totale et la relient à la durée pendant laquelle les patients restent sans progression. D’autres outils d’IA comparent des examens pris avant et peu après une hormonothérapie ou une chimiothérapie, prédisant des résultats de traitement sur plusieurs mois bien plus tôt que les règles traditionnelles basées sur de simples variations d’intensité.
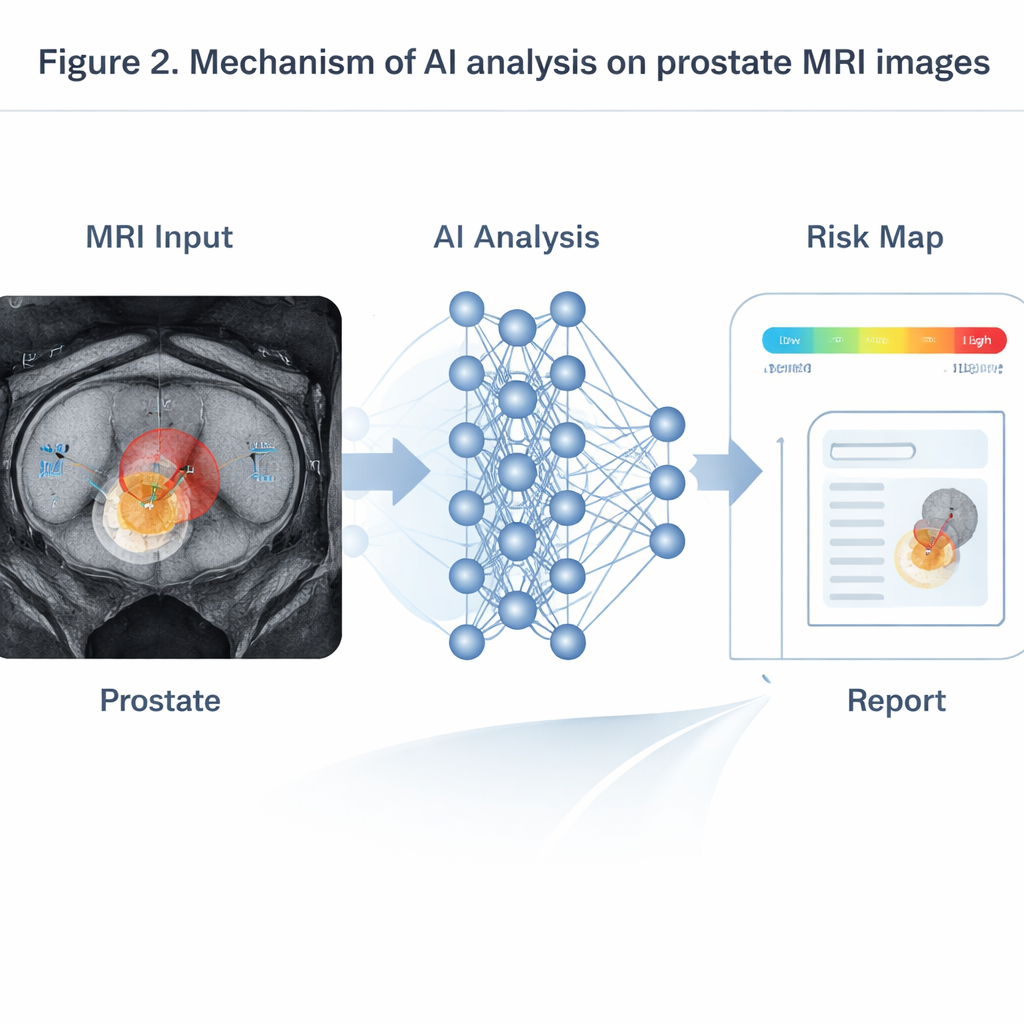
Obstacles : lacunes de données, boîtes noires et usage équitable
Malgré ces progrès, le déploiement en conditions réelles rencontre de sérieux obstacles. Les jeux de données d’imagerie de haute qualité et bien annotés restent limités et biaisés en faveur des grands hôpitaux académiques, tandis que les examens provenant de centres plus petits et de populations diverses sont sous‑représentés. De subtiles différences entre marques d’appareils, réglages et qualité d’image peuvent faire échouer des modèles entraînés dans un contexte donné lorsqu’ils sont appliqués ailleurs. De nombreux systèmes d’IA puissants fonctionnent comme des « boîtes noires », fournissant un score de risque sans explication claire, ce qui mine la confiance des cliniciens — surtout quand l’ordinateur contredit l’expérience. La revue soulève aussi des inquiétudes sur la confidentialité, les restrictions de partage des données et le risque que les modèles performent moins bien pour certains groupes, creusant potentiellement les inégalités de santé si ces biais ne sont pas surveillés et corrigés.
Construire des partenaires de confiance en clinique
À l’avenir, les auteurs envisagent l’IA comme un coéquipier fiable plutôt que comme un oracle mystérieux. Ils décrivent des efforts pour constituer de larges jeux de données partagés entre hôpitaux tout en préservant la vie privée via des techniques comme l’apprentissage fédéré, où seuls des mises à jour de modèle — et non les données brutes des patients — sont échangées. De nouveaux outils d’« IA explicable » visent à montrer quelles régions de l’image ont motivé une décision et à les relier à la pathologie connue, donnant aux médecins des raisons tangibles d’adhérer ou non. Plutôt que des modèles universels, des systèmes adaptés se concentreront sur des tâches précises : dépistage dans des cliniques très actives, guidage des biopsies, suivi des traitements ou surveillance des patients à haut risque. La combinaison de l’imagerie avec des données génétiques et cliniques pourrait affiner encore davantage le pronostic et personnaliser la thérapie. Pour les patients, le bilan est encourageant : si ces défis techniques, éthiques et réglementaires sont bien gérés, l’imagerie augmentée par l’IA pourrait permettre une détection plus précoce, moins de biopsies inutiles, des réponses plus rapides et des plans de traitement mieux adaptés pour le cancer de la prostate.
Citation: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
Mots-clés: imagerie du cancer de la prostate, intelligence artificielle, IRM et échographie, PSMA PET/CT, radiomique