Clear Sky Science · fr
Auto-encodage masqué, préentraînement généralisable et experts intégrés pour améliorer la segmentation des gliomes
Pourquoi des examens plus intelligents comptent pour les tumeurs cérébrales
Les tumeurs cérébrales appelées gliomes figurent parmi les cancers les plus mortels, et pourtant les médecins passent encore beaucoup de temps à tracer manuellement les contours des tumeurs sur les IRM. Ce contourage soigneux oriente la chirurgie et la radiothérapie, mais il peut prendre 15 à 20 minutes par patient et doit être répété au fil du temps. L'étude présente MAGPIE, un système d'intelligence artificielle qui apprend à partir de dizaines de milliers d'IRM cérébrales sans étiquettes humaines, puis n'a besoin que d'une poignée de cas annotés par des experts pour cartographier de manière fiable les gliomes. Pour les patients, cela peut signifier une planification des traitements plus rapide et plus cohérente, même dans des hôpitaux dépourvus de grands jeux de données annotés.
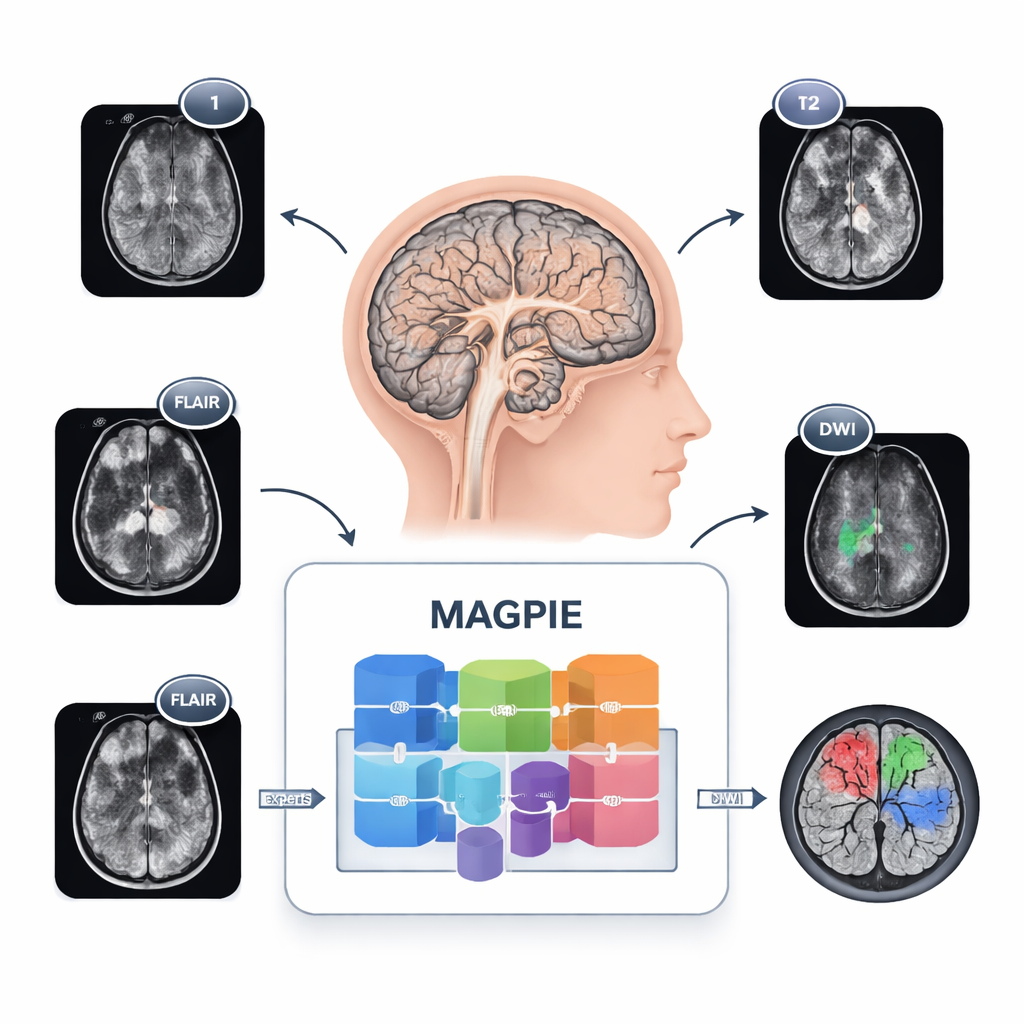
Voir les tumeurs autrement
Les gliomes sont difficiles à cartographier parce qu'ils ne forment pas de masses nettes. Les cellules cancéreuses se propagent le long des fibres cérébrales, créant des marges floues et de petits foyers satellites difficiles à détecter. De plus, les hôpitaux utilisent des réglages d'IRM et des combinaisons de séquences différents, si bien qu'un outil entraîné dans un établissement peut échouer dans un autre. MAGPIE répond à tous ces problèmes à la fois. Il a d'abord été exposé à 43 505 IRM cérébrales non étiquetées issues de nombreuses études et types d'appareils. Pendant cette phase, il a appris des schémas généraux de tissu cérébral sain et malade en essayant de reconstruire des parties manquantes des images et en comparant différentes vues augmentées d'un même cerveau, ce qui l'a forcé à se concentrer sur des caractéristiques stables et significatives plutôt que sur des détails de pixels fragiles.
Laisser plusieurs experts partager le travail
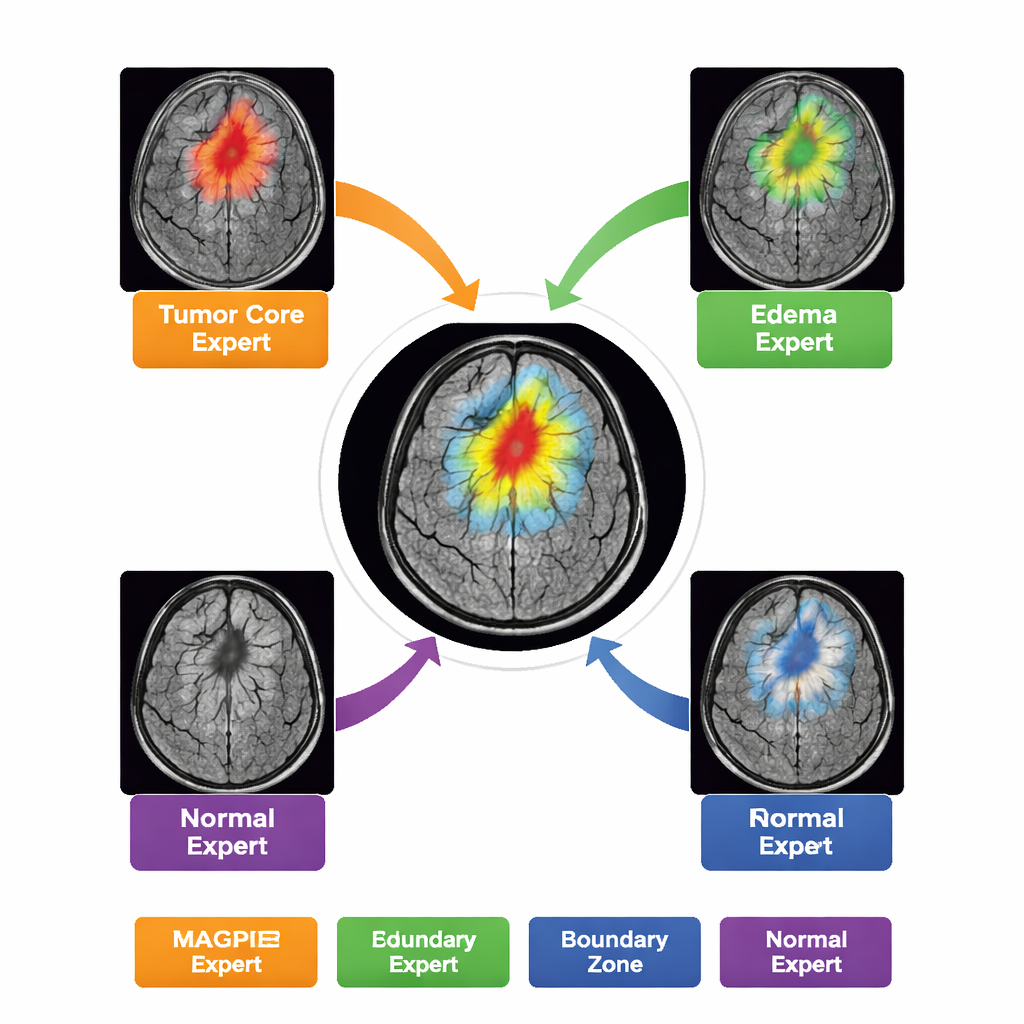
Plutôt que d'agir comme un modèle monolithique unique, MAGPIE contient une « mixture d'experts » interne. Lorsqu'il analyse une nouvelle image, il n'active qu'un petit sous-ensemble de huit sous-réseaux spécialisés pour chaque région de l'image. Au cours de l'entraînement, ces experts se répartissent naturellement la tâche : certains deviennent sensibles à la bordure brillante et en croissance active de la tumeur ; d'autres repèrent le noyau nécrotique ; d'autres encore apprennent l'anneau flou d'œdème autour de la tumeur ; et certains se concentrent principalement sur l'arrière-plan cérébral normal et les limites. Les auteurs le démontrent en mesurant à quel point l'activité de chaque expert chevauche les différentes zones tumorales tracées par les radiologues. Cette division du travail améliore la précision tout en maintenant le coût computationnel raisonnable — seulement environ la moitié des paramètres du modèle sont actifs pour une zone donnée.
Gérer des IRM réelles et désordonnées
Les protocoles cliniques d'IRM sont loin d'être uniformes. Certains patients ont quatre séquences, d'autres moins ; des machines de fabricants différents produisent des images légèrement différentes. La conception de MAGPIE traite chaque séquence d'IRM comme un « jeton » séparé et apprend à estimer le poids de chacune en temps réel, au lieu d'attendre un ensemble fixe d'entrées dans un ordre fixe. Cette approche indépendante des canaux permet au système de s'adapter si, par exemple, une séquence rehaussée au contraste manque mais que la FLAIR est présente. Le modèle utilise également des mécanismes d'attention avancés qui lui permettent à la fois de « voir loin », en capturant la propagation à distance le long des fibres de la matière blanche, et de « voir précisément », en repérant des lésions très petites de quelques millimètres seulement.
Faire plus avec beaucoup moins d'étiquettes
Après le préentraînement, les chercheurs ont ajusté MAGPIE sur seulement 20 cas de gliome entièrement annotés et l'ont comparé à des modèles standard entraînés à partir de zéro dans les mêmes conditions. Sur un important banc d'essai de tumeurs cérébrales (BraTS21), MAGPIE a atteint un score Dice — une mesure courante de recouvrement en imagerie médicale — d'environ 61 %, battant la meilleure version entraînée depuis zéro d'environ 2,6 points de pourcentage et surpassant une méthode auto-supervisée antérieure performante sans montrer de « transfert négatif » nuisible. Sur des données hors distribution difficiles — IRM issues de maladies différentes, de types d'appareils et de réglages d'image variés — il s'est également mieux comporté, atteignant plus de 70 % de Dice sur un jeu de données de lésions de la matière blanche sans réglage supplémentaire. De façon cruciale, ce niveau de performance exige normalement de l'ordre de 400 cas annotés ; MAGPIE l'atteint avec seulement environ 5 % de cet effort.
Ce que cela pourrait signifier pour les patients et les cliniques
Pour les non-spécialistes, le message central est que MAGPIE transforme une montagne d'IRM non étiquetées en un assistant puissant qui nécessite très peu d'apprentissage expert pour devenir cliniquement utile. Il peut délimiter des tumeurs cérébrales complexes avec des limites réalistes, détecter de petits foyers satellites que d'autres systèmes manquent, et continuer à fonctionner de manière fiable lorsque les examens proviennent de machines inconnues ou lorsqu'il manque certaines séquences. Cette combinaison pourrait réduire le temps d'annotation des radiologues d'environ 95 %, abaisser la barrière pour que des hôpitaux de moindre taille déploient une IA d'imagerie avancée, et soutenir une planification chirurgicale et radiothérapeutique plus précise. Bien qu'une validation supplémentaire soit nécessaire sur des types de tumeurs rares et des cas de bas grade, cette étude montre comment un apprentissage auto-supervisé soigneusement conçu peut rapprocher une segmentation robuste et économe en données des pratiques cliniques quotidiennes.
Citation: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Mots-clés: segmentation de gliome, IRM cérébrale, apprentissage auto-supervisé, mélange d'experts, IA en imagerie médicale