Clear Sky Science · fr
Modèles guidés par la clinique ou modèles fondamentaux ? prédire la myélopathie cervicale spondylotique à partir des dossiers de santé électroniques
Pourquoi détecter ce problème de la colonne plus tôt compte
La myélopathie cervicale spondylotique (MCS) est un terme technique, mais pour beaucoup de personnes âgées elle menace discrètement la moelle épinière. Elle peut débuter par de la maladresse, une démarche traînante ou des troubles urinaires et évoluer progressivement vers un handicap sévère voire une paralysie. Les médecins la manquent souvent pendant des années parce que les signes sont subtils et ressemblent à des affections plus courantes comme l’arthrite ou le syndrome du canal carpien. Cette étude pose une question d’actualité : des motifs enfouis dans les dossiers de santé électroniques peuvent-ils aider à repérer des personnes à risque de MCS des années avant un diagnostic formel, et quel type d’intelligence artificielle (IA) est le mieux adapté pour cela ?
Une pathologie cachée dans une population qui vieillit
La MCS survient lorsque l’usure liée à l’âge rétrécit le canal rachidien au niveau du cou et compresse la moelle épinière. La maladie est fréquente chez les personnes âgées ; l’imagerie cervicale montre une compression médullaire chez environ un tiers des personnes de plus de 60 ans, et une part substantielle d’entre elles développera des symptômes. Pourtant, les études suggèrent que les patients attendent souvent deux à six ans entre les premiers signes et un diagnostic correct, perdant un temps précieux durant lequel une chirurgie ou d’autres interventions pourraient prévenir des lésions permanentes. À mesure que les populations vieillissent et que les médecins de soins primaires sont confrontés à des consultations surchargées et à une exposition limitée aux pathologies rachidiennes, le besoin de méthodes évolutives pour détecter précocement la MCS s’accroît.
Transformer les dossiers médicaux en dispositif d’alerte précoce
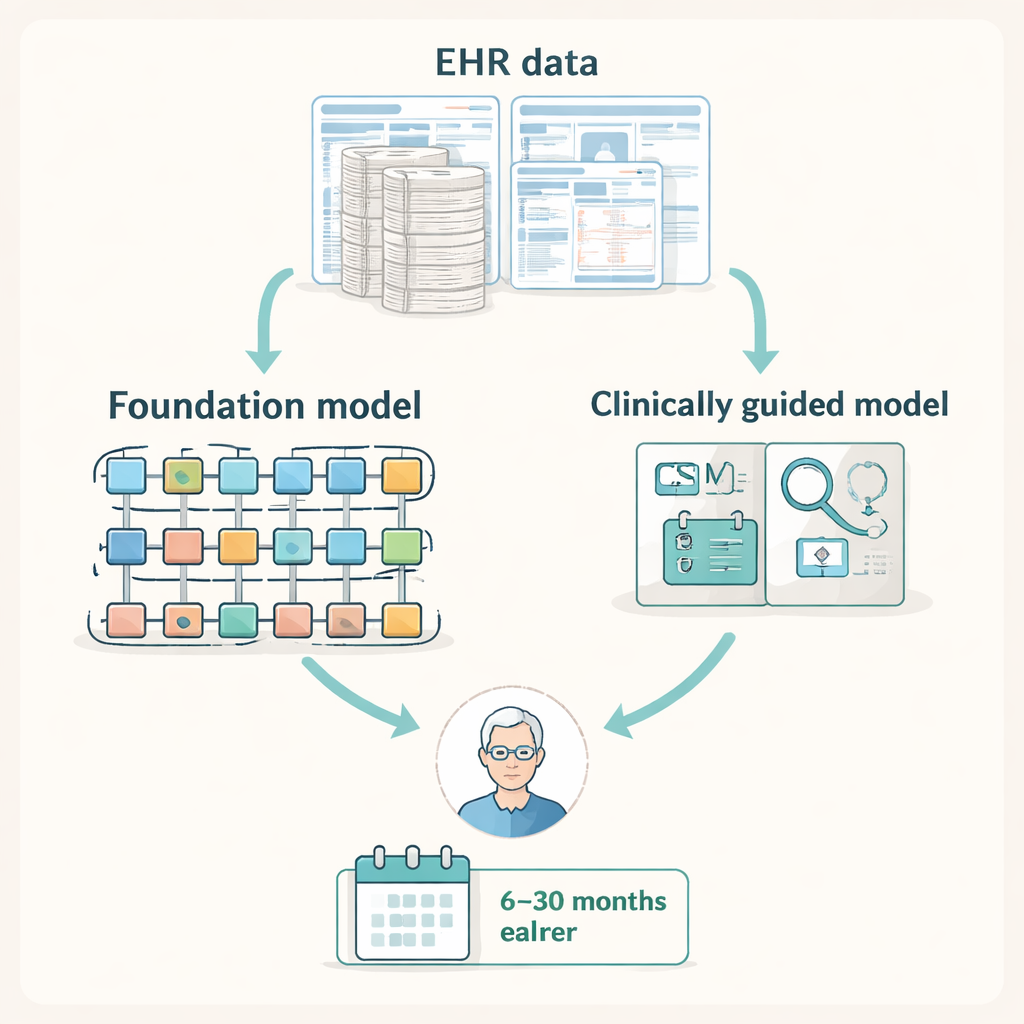
Les dossiers de santé électroniques modernes consignent une trace détaillée de diagnostics, analyses, procédures et consultations. Les chercheurs ont supposé que cette chronologie contenait probablement des indices de MCS précoce — tels que des chutes répétées, des examens nerveux ou des séances de kinésithérapie — bien avant qu’on n’ordonne des imageries spécialisées du rachis. Ils ont rassemblé des données d’environ 2 millions de patients dans deux grandes bases de données américaines : une base nationale de remboursements d’assurance et les dossiers d’un système de santé régional. Dans ces ensembles, ils ont identifié des dizaines de milliers de personnes qui ont finalement reçu un diagnostic de MCS et les ont appariées à des patients similaires qui ne l’ont pas reçu, créant un banc d’essai à grande échelle pour déterminer si l’IA pouvait prédire qui serait diagnostiqué ultérieurement avec la MCS à des horizons de 6 à 30 mois.
IA généraliste puissante contre outils sobres guidés par la clinique
L’équipe a comparé plusieurs types de modèles d’apprentissage automatique traitant des données EHR. D’un côté se trouvaient de grands « modèles fondamentaux » — des systèmes puissants basés sur des transformeurs initialement entraînés sur des millions de dossiers patients pour apprendre des motifs généraux dans les données de santé. De l’autre, des modèles plus petits construits uniquement à partir d’une liste concise de 497 codes de diagnostic, procédure et médicaments sélectionnés à la main par des spécialistes du rachis comme fortement pertinents pour la MCS. Les chercheurs ont mesuré les performances avec des statistiques adaptées aux maladies rares, s’interrogeant sur l’amélioration apportée par chaque modèle par rapport à un classement aléatoire pour identifier des patients qui développeraient ensuite une MCS sur différentes fenêtres de prédiction.
Précision sur place, robustesse sur la route
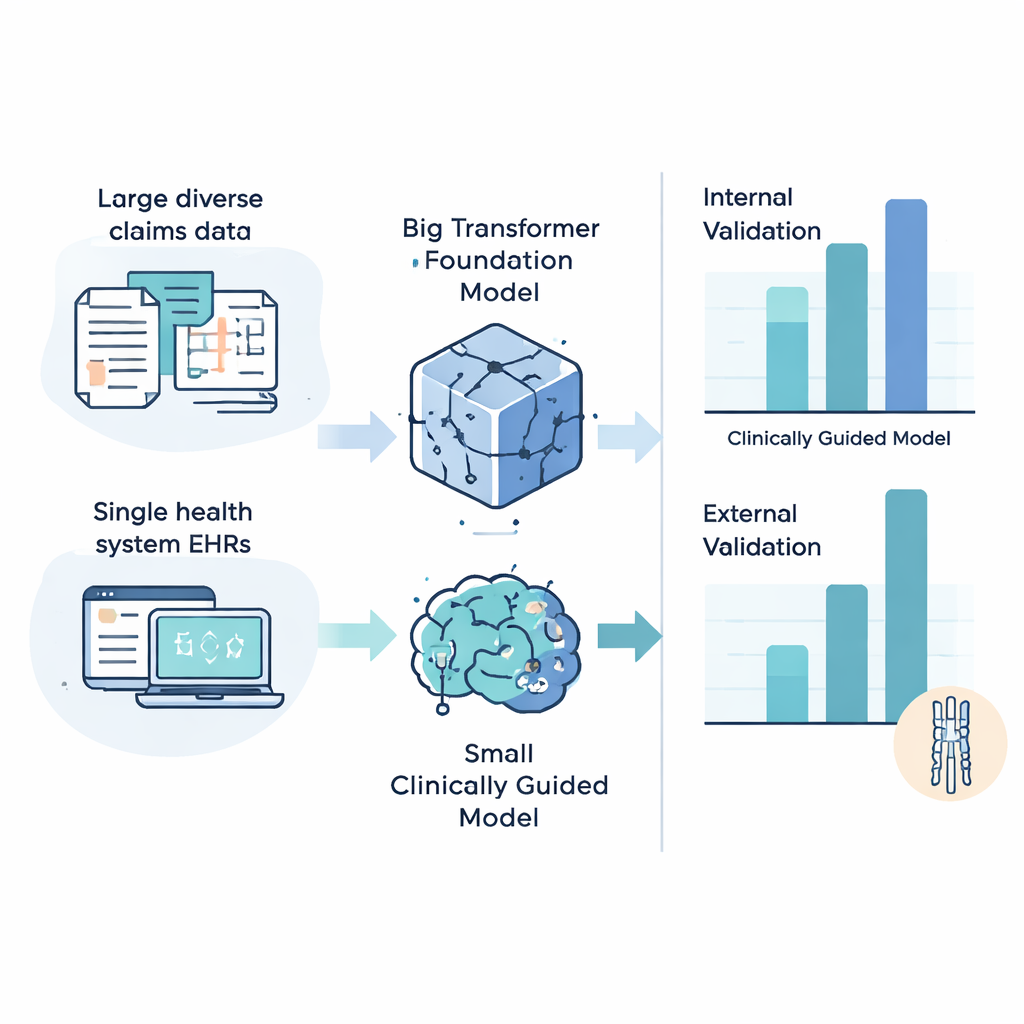
Lorsque les modèles étaient entraînés et testés au sein de la même vaste et diverse base d’assurance, le plus grand modèle fondamental était généralement le plus performant, atteignant jusqu’à environ six à sept fois la précision d’un classificateur non informatif. Cependant, la donne changeait lorsque les modèles étaient évalués sur le système de santé indépendant. Là, les modèles plus simples et guidés cliniquement dépassaient généralement les transformeurs complexes et, dans certains cas, obtenaient jusqu’à 13 fois de meilleure performance que le hasard pour prédire quels patients recevraient bientôt un diagnostic de MCS. Une expérience inverse — entraînement sur le système de santé unique et test sur la base nationale — racontait une histoire similaire : les modèles plus petits et centrés sur la clinique avaient tendance à mieux se transférer entre institutions. Des analyses par sous-groupes ont également révélé que tous les modèles fonctionnaient mieux pour les patients ayant des visites de santé plus fréquentes, soulevant des questions d’équité pour ceux qui consultent moins souvent.
Ce que cela signifie pour les patients et les médecins
Les résultats suggèrent que l’IA pourrait aider à repérer des personnes à haut risque de MCS jusqu’à deux ans et demi avant le diagnostic, orientant potentiellement les cliniciens vers des examens neurologiques plus précoces et des imageries du rachis. Pourtant, l’étude souligne aussi un compromis : tandis que de grands modèles sophistiqués peuvent exceller sur les données sur lesquelles ils sont entraînés, des modèles plus petits, conçus avec soin et ancrés dans l’expertise clinique peuvent être plus fiables lorsqu’on les déplace vers de nouveaux hôpitaux et populations. Pour les patients, le message est porteur d’espoir mais nuancé : l’usage intelligent des données de routine pourrait raccourcir la longue odyssée diagnostique que vivent nombreux des patients atteints de MCS, mais la réussite dépendra non seulement d’algorithmes puissants, mais aussi d’une conception réfléchie des modèles, de tests rigoureux dans des contextes divers et d’une attention à l’équité pour que les bénéfices de la détection précoce soient largement partagés.
Citation: Yakdan, S., Warner, B., Ghogawala, Z. et al. Clinically-guided models or foundation models? predicting cervical spondylotic myelopathy from electronic health records. npj Digit. Med. 9, 153 (2026). https://doi.org/10.1038/s41746-026-02337-7
Mots-clés: myélopathie cervicale spondylotique, dossiers de santé électroniques, apprentissage automatique, modèles fondamentaux, diagnostic précoce