Clear Sky Science · fr
Fusion multimodale de modèles fondamentaux en pathologie et en radiologie pour le sous-typage des gliomes selon l'OMS 2021
Rapprocher deux visions des tumeurs cérébrales
Lorsqu'une personne reçoit un diagnostic de tumeur cérébrale, les médecins doivent savoir non seulement qu'une tumeur est présente, mais quel type exact il s'agit. Les différents types de tumeurs répondent très différemment à la chirurgie, à la radiothérapie et aux médicaments. Aujourd'hui, ce « sous-typage » détaillé nécessite généralement des tests génétiques qui peuvent être lents, coûteux et indisponibles partout. Cette étude examine si un système informatique intelligent qui analyse à la fois des images cérébrales et des images au microscope du tissu tumoral peut inférer de manière fiable ces sous-types, accélérant potentiellement l'accès à des traitements de précision et les rendant plus largement disponibles.
Pourquoi le type de tumeur importe
Les gliomes diffus de l'adulte font partie des cancers cérébraux les plus meurtriers, et pourtant ils peuvent souvent se ressembler sur les examens standard et au microscope. Les directives modernes les regroupent en trois sous-types génétiques qui diffèrent fortement par leur agressivité et par la survie moyenne des patients. La référence actuelle pour distinguer ces sous-types repose sur des tests moléculaires de l'ADN tumoral. Ces tests nécessitent plus de tissu, des laboratoires spécialisés et des délais de quelques jours à quelques semaines. Les auteurs se demandent si des IRM et des lames de pathologie numérisées, collectées de manière routinière, pourraient être combinées pour extraire suffisamment d'informations pour remplacer une partie de ce bilan génétique.
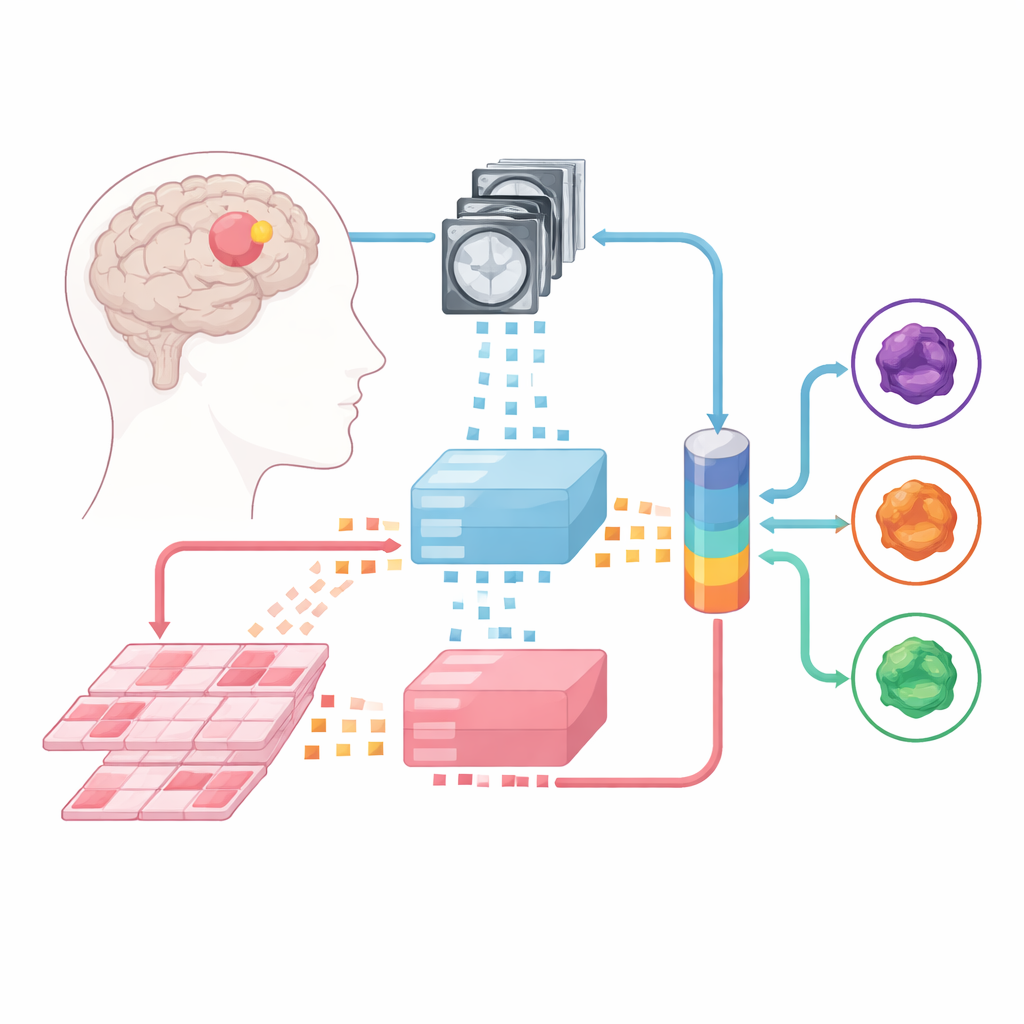
Apprendre aux machines à lire scans et lames
L'équipe s'est appuyée sur de grands « modèles fondamentaux » — de puissants analyseurs d'images préentraînés sur d'énormes corpus d'images médicales. Un de ces modèles traite des IRM multiparamétriques, et un autre gère des lames de pathologie haute résolution issues du tissu tumoral. Chaque cas est découpé en petits patchs d'image, que les modèles fondamentaux transforment en empreintes numériques. Par-dessus ces « experts » fixes, les chercheurs ont entraîné trois types de modèles de fusion apprenant à combiner l'information des deux modalités : une architecture de fusion tardive, une de fusion précoce et une architecture plus souple de mixture d'experts capable de décider dynamiquement de la pondération à accorder à chaque source.
Mélanger les modalités sans appariement patient
Un obstacle pratique pour ces méthodes multimodales est que les hôpitaux disposent rarement de grands jeux de données où chaque patient a à la fois des IRM et des images de pathologie soigneusement appariées. Plutôt que de s'appuyer sur des données parfaitement appariées, les auteurs ont assemblé des collections séparées : des centaines de cas d'IRM provenant de plusieurs centres et des centaines de cas de pathologie issus d'une autre ressource, plus un petit ensemble de 171 patients d'un projet public sur le cancer ayant les deux. Pendant l'entraînement, ils ont souvent associé une IRM d'une personne avec une lame de pathologie d'une autre, du moment que les tumeurs appartenaient au même sous-type. De manière surprenante, les modèles entraînés sur ces données « non appariées » ont obtenu des performances équivalentes à celles entraînées sur de vrais couples patients, et nettement supérieures au simple moyennage de deux modèles mono-modaux distincts.
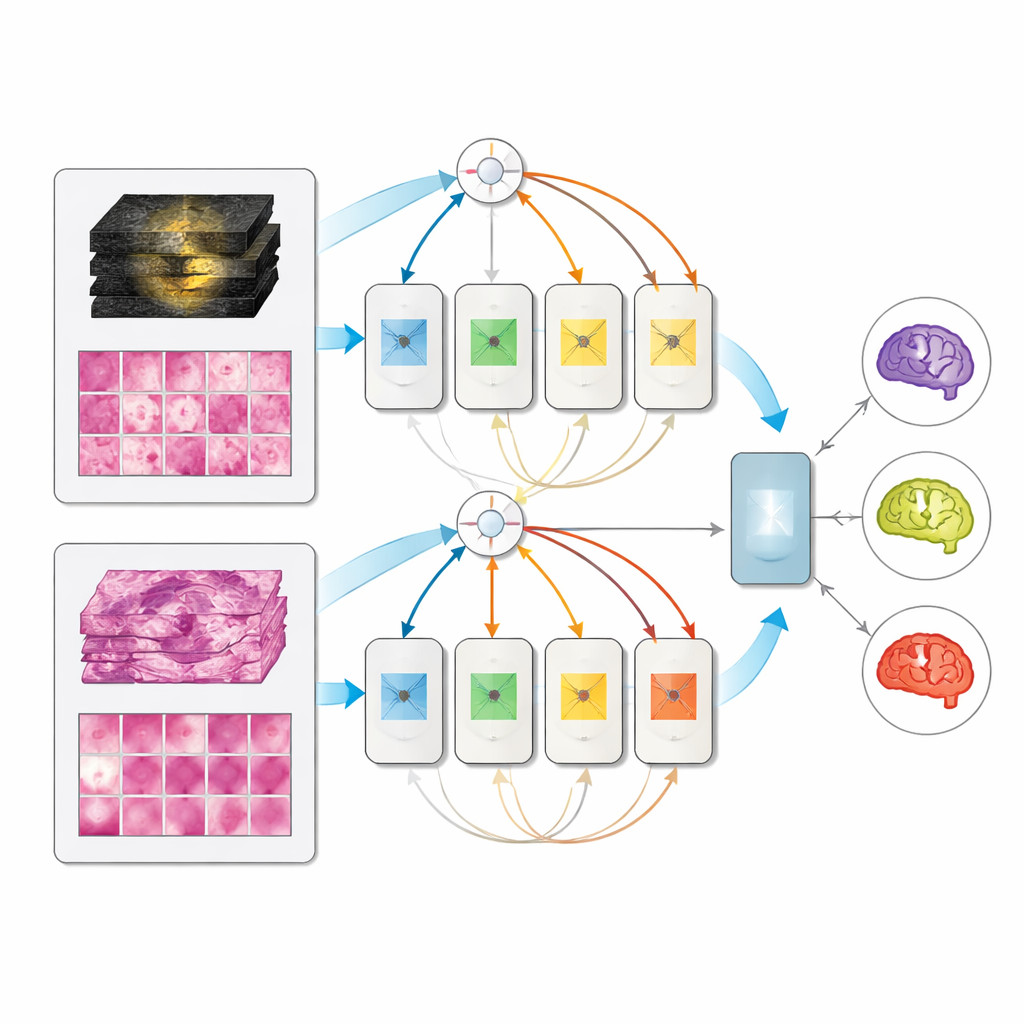
Un modèle unique qui s'adapte à ce qui est disponible
Sur l'ensemble indépendant de 171 patients entièrement caractérisés, tous les modèles multimodaux ont surpassé leurs équivalents à entrée unique, et l'architecture mixture d'experts a obtenu les meilleurs résultats, atteignant des scores très élevés pour distinguer les trois sous-types. Fait notable, lorsque seule l'IRM ou seule la pathologie était fournie au moment du test, le modèle multimodal ne s'effondrait pas ; il obtenait des performances à peu près équivalentes à celles des modèles dédiés à une seule modalité. Cela signifie qu'une clinique pourrait déployer un système unifié utilisant les informations disponibles — seules les images préopératoires, seules les lames post-chirurgicales, ou les deux — plutôt que de maintenir des outils séparés pour chaque situation.
Voir ce que le modèle voit
Pour instaurer la confiance dans les décisions du système, les chercheurs ont examiné où le modèle « regarde » et quelles caractéristiques d'image sont les plus importantes. Les cartes d'attention ont montré que le modèle joint répartit son focus de manière plus large sur la tumeur et ses alentours, tant sur l'IRM que sur les lames de tissu, et que cette attention plus diffuse coïncidait souvent avec des prédictions correctes. Une analyse approfondie des caractéristiques apprises a révélé des motifs correspondant à des indices médicaux connus : par exemple, des caractéristiques IRM mettant en évidence des cœurs tumoraux se rehaussant au contraste et des espaces liquidien déformés aident à séparer les tumeurs plus agressives, tandis que des caractéristiques tissulaires capturant des formes cellulaires et des textures classiques aident à reconnaître des sous-types spécifiques de gliome. Des lacunes intéressantes ont aussi émergé : le modèle n'encodait pas fortement certains signes classiques des tumeurs les plus agressives, ce qui soutient l'idée qu'il traite souvent ce groupe comme une « valeur par défaut » en l'absence de preuves solides en faveur d'un sous-type plus favorable.
Ce que cela pourrait signifier pour les patients
En termes simples, ce travail montre qu'un système d'IA combinant images cérébrales et images au microscope peut classer les tumeurs cérébrales plus précisément que des systèmes n'utilisant qu'un seul type d'image, et qu'il peut être entraîné même lorsque les deux types d'images ne proviennent pas des mêmes patients. Si ces outils sont validés davantage sur des cohortes plus vastes et plus diverses, ils pourraient aider les médecins à estimer le sous-type tumoral plus tôt et de manière plus répandue, en particulier dans les contextes où les tests génétiques sont limités. Bien qu'ils ne remplacent pas les analyses moléculaires, ils peuvent servir de guides rapides et peu coûteux orientant les chirurgiens et oncologues vers le diagnostic le plus probable et la stratégie thérapeutique la plus appropriée.
Citation: Saueressig, C., Scholz, D., Raffler, P. et al. Multimodal fusion of pathology and radiology foundation models for WHO 2021 glioma subtyping. npj Precis. Onc. 10, 118 (2026). https://doi.org/10.1038/s41698-026-01366-5
Mots-clés: sous-typage des gliomes, imagerie multimodale, intelligence artificielle, IRM et pathologie, diagnostic du cancer du cerveau