Clear Sky Science · fr
Profilage quantitatif du HER2 dans les tissus et le plasma prédit l’activité du trastuzumab deruxtecan pour le cancer du sein
Pourquoi cette recherche importe pour les patients
Pour les personnes vivant avec un cancer du sein métastatique, de nouveaux médicaments peuvent apporter de l’espoir — mais ils ne sont pas également efficaces pour tout le monde. Cette étude pose une question pratique : peut-on mieux prédire qui bénéficiera le plus, et le plus longtemps, d’un médicament ciblé largement utilisé appelé trastuzumab deruxtecan (souvent abrégé en T‑DXd) ? En examinant de plus près et de manière plus précise les échantillons tumoraux et le sang, les chercheurs montrent qu’une mesure fine d’une molécule appelée HER2 — et de certains marqueurs d’ADN et de protéines — peut révéler quels cancers sont les plus susceptibles de répondre à ce traitement.
Un médicament ciblé aux résultats inégaux
Le T‑DXd est un « conjugué anticorps–médicament », une sorte de missile guidé qui cible les cellules exprimant la protéine HER2 et délivre à l’intérieur d’elles une charge utile de type chimiothérapie. À l’origine utilisé pour des tumeurs présentant des niveaux très élevés de HER2, il est désormais approuvé pour près de neuf patients sur dix atteints de cancer du sein métastatique, y compris pour ceux ayant un faible niveau ou même une absence de HER2 selon les tests standards. Pourtant, dans la pratique quotidienne, certains patients bénéficient d’une longue période de contrôle de la maladie sous T‑DXd, tandis que d’autres voient leur cancer progresser au bout de seulement quelques mois. Les méthodes de laboratoire traditionnelles, qui classent les tumeurs en HER2‑positif, HER2‑faible ou HER2‑zéro, n’ont pas su expliquer correctement ces différences.
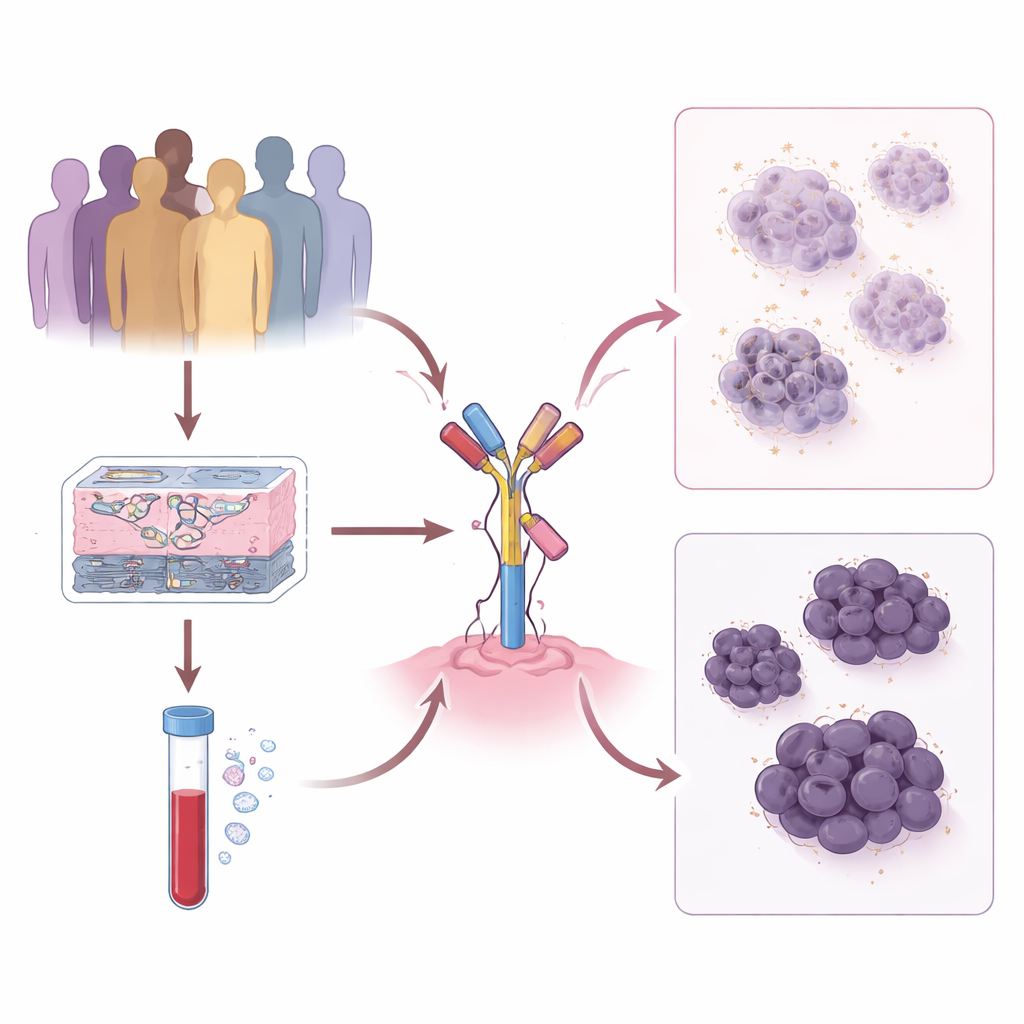
Suivre l’évolution de la tumeur dans le temps
L’équipe a examiné 191 patients traités par T‑DXd dans deux grands centres cancérologiques américains, en analysant le comportement de leurs cancers et l’évolution des niveaux de HER2 depuis la tumeur initiale jusqu’aux métastases ultérieures. Ils ont constaté qu’un étiquetage unique d’une tumeur comme HER2‑faible ou HER2‑zéro manquait des dynamiques importantes. Les patients dont les cancers restaient clairement HER2‑positifs ont vécu le plus longtemps sous T‑DXd, suivis par ceux dont les tumeurs présentaient de manière constante des niveaux faibles — mais stables — de HER2. En revanche, lorsque le statut HER2 oscillait entre faible et zéro au fil du temps, le bénéfice du T‑DXd était sensiblement plus court. Ces schémas suggèrent que plus une tumeur dépend de façon stable du HER2, mieux ce médicament peut fonctionner.
Mesurer le HER2 avec une règle plus fine
Pour dépasser les catégories grossières, les chercheurs ont appliqué un ensemble de tests modernes aux tissus tumoraux. L’un utilisait l’immunofluorescence quantitative pour compter précisément la protéine HER2 ; un autre reposait sur une puce protéique haut débit ; un troisième lisait des profils d’activité génique liés à la région HER2 du génome. Dans les trois approches, le message était cohérent : des niveaux quantitatifs plus élevés de HER2 — qu’ils soient mesurés comme protéine à la surface cellulaire, formes activées (phosphorylées) ou ARN messager — étaient associés à un délai plus long avant le prochain traitement et à une meilleure survie globale sous T‑DXd. Chez les mêmes patients, la lecture pathologique habituelle (HER2‑positif, faible ou zéro) distinguait à peine les résultats, soulignant que « combien » de HER2 est présent importe davantage que la case cochée.
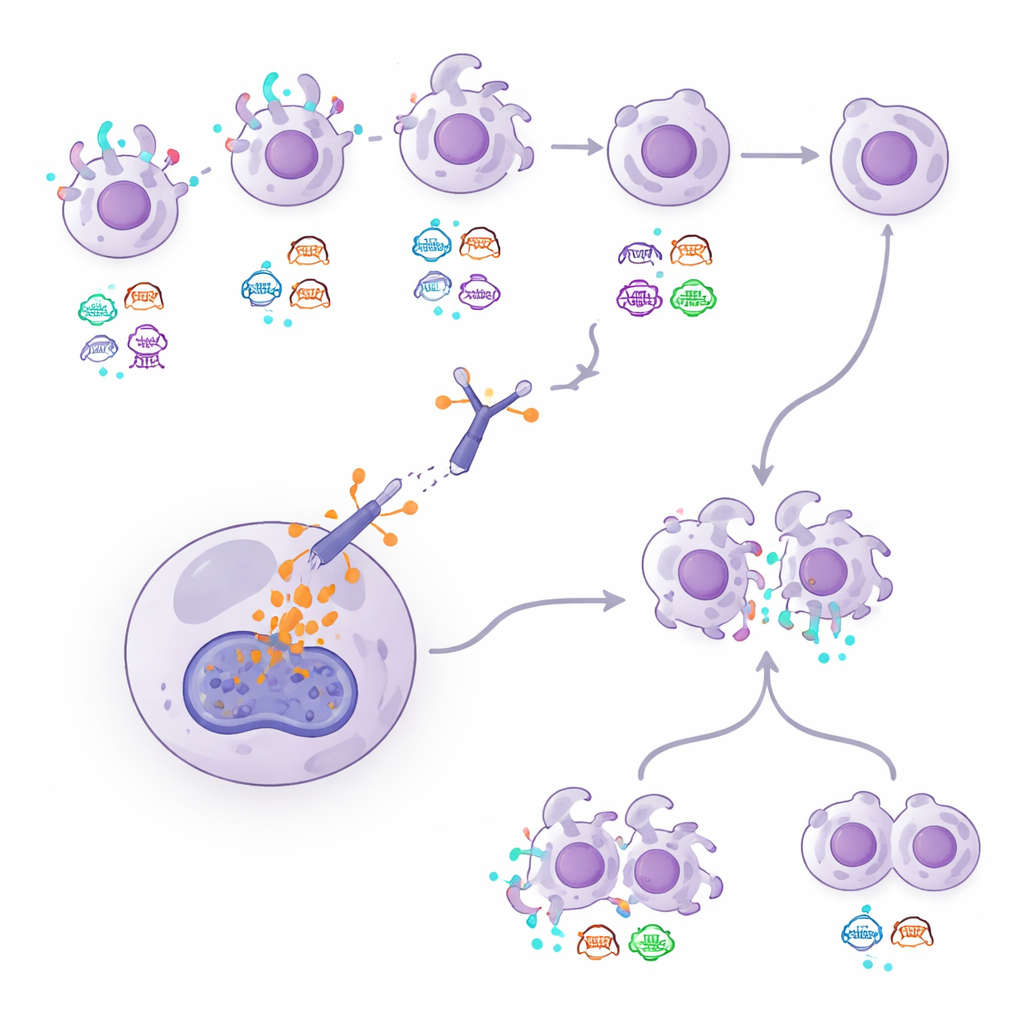
Indices issus des tests sanguins et d’autres marqueurs tumoraux
Parce que les biopsies répétées peuvent être invasives, l’étude a aussi évalué une approche sanguine qui analyse des fragments d’ADN tumoral circulant dans le flux sanguin. En utilisant une méthode appelée DNADX, les investigateurs ont regroupé les échantillons sanguins des patients en grappes biologiques et calculé un signature ADN liée au HER2. Les patients dont le sang montrait des signaux HER2 plus forts avaient tendance à rester plus longtemps sous T‑DXd, tandis que ceux présentant des profils d’ADN associés à une maladie plus agressive et à croissance rapide avaient de moins bons résultats. Les chercheurs ont également noté que, dans des cancers étiquetés HER2‑négatifs, des niveaux élevés d’une protéine appelée topoisomérase 1 à l’intérieur des cellules tumorales étaient liés à des résultats plus défavorables, laissant entendre que la façon dont la charge du médicament est traitée par la cellule peut influencer le succès. Certaines pertes ou mutations génétiques, comme des altérations des gènes ERBB2 et TP53 et un enrichissement en mutations ARID1B après traitement, sont apparues comme des marqueurs possibles de résistance.
Ce que cela signifie pour les patients et les cliniciens
Globalement, l’étude montre que le T‑DXd est un traitement efficace en pratique réelle, en particulier pour les patients dont les tumeurs sont fortement et régulièrement drivées par le HER2. Mais elle montre aussi que le test HER2 traditionnel est un instrument trop grossier pour guider l’utilisation de ce médicament puissant. En recourant à des mesures plus sensibles sur le tissu et le sang, les médecins pourraient éventuellement identifier avec précision les patients les plus susceptibles de bénéficier du T‑DXd, épargner aux autres un traitement inefficace et mieux planifier l’ordre d’utilisation des différents conjugués anticorps–médicament. Bien que ces tests avancés ne soient pas encore routiniers et nécessitent une validation sur des cohortes plus larges, ils ouvrent la voie à un avenir où les choix thérapeutiques pour le cancer du sein métastatique seront adaptés à des portraits moléculaires détaillés, et non à de simples étiquettes générales.
Citation: Tarantino, P., Kim, SE., Hughes, M.E. et al. Quantitative HER2 tissue and plasma profiling predicts the activity of trastuzumab deruxtecan for breast cancer. npj Precis. Onc. 10, 141 (2026). https://doi.org/10.1038/s41698-026-01365-6
Mots-clés: Test du HER2, trastuzumab deruxtecan, cancer du sein métastatique, biopsie liquide, conjugués anticorps–médicament