Clear Sky Science · fr
La réponse au midostaurin dans la LMA est dictée par un état cellulaire de type progéniteur ciblé sélectivement par des mimétiques de SMAC
Pourquoi certains médicaments contre la leucémie cessent de fonctionner
Pour de nombreuses personnes atteintes d’un type de cancer du sang appelé leucémie myéloïde aiguë (LMA), les nouveaux médicaments ciblés ont apporté de l’espoir — mais tout le monde n’en bénéficie pas, et les réponses s’estompent souvent. Cette étude pose une question simple mais cruciale : pourquoi certaines cellules leucémiques ignorent‑elles un médicament largement utilisé, le midostaurin, et peut‑on trouver une combinaison intelligente qui contraigne ces cellules récalcitrantes à mourir ?
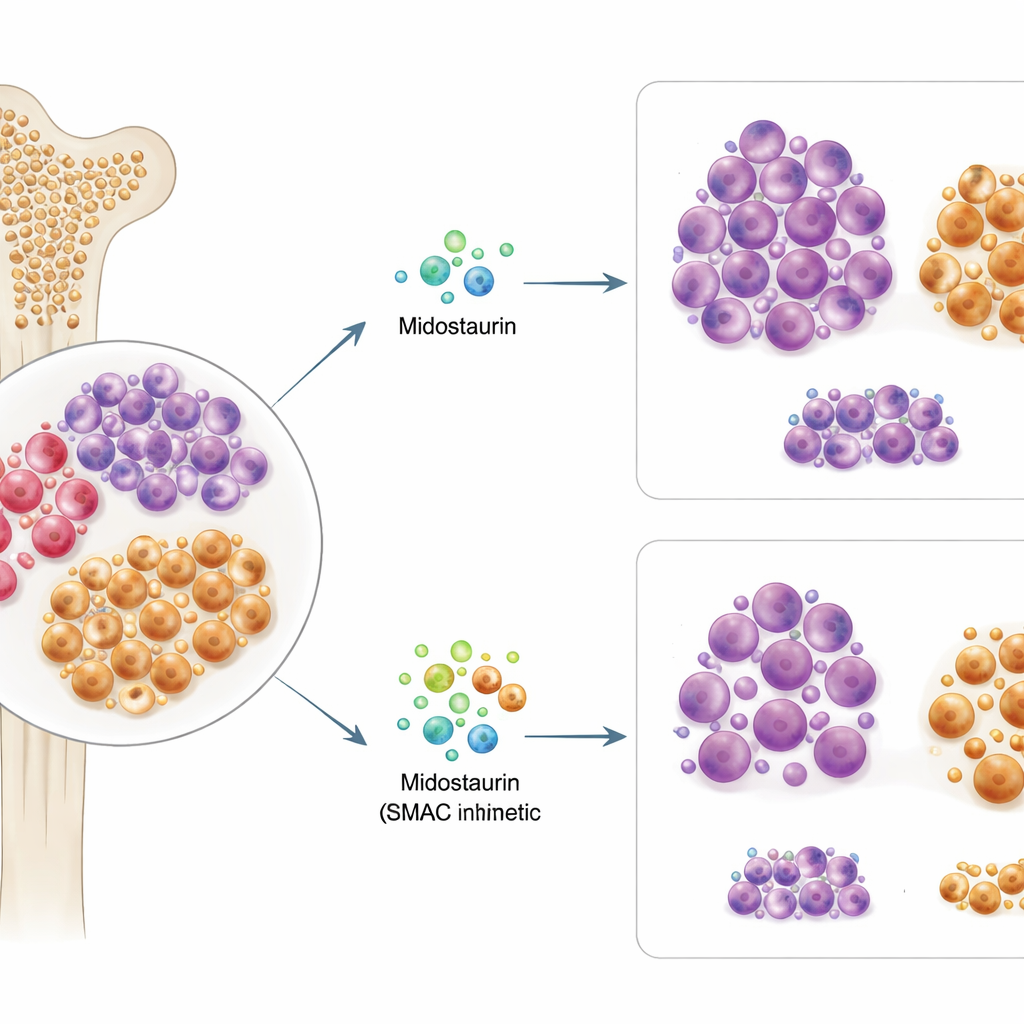
Au‑delà de la mutation principale
Environ un patient sur trois atteint de LMA porte une altération d’un gène appelé FLT3, qui stimule la croissance leucémique et motive la prescription de midostaurin. Les chercheurs ont testé des échantillons de moelle osseuse et de sang de 63 patients atteints de LMA avec mutation FLT3, en exposant les cellules au midostaurin et à plus de 500 autres drogues anticancéreuses en laboratoire. Ils ont constaté que la sensibilité des cellules d’un patient au midostaurin ex vivo correspondait étroitement à la réponse clinique ultérieure de ce patient. De manière surprenante, le type exact de mutation FLT3 ou son abondance ne prédisaient pas de façon fiable le succès du midostaurin, ce qui suggère que la génétique seule n’explique pas qui en bénéficie.
Un réservoir caché de cellules « graines » résistantes
En approfondissant, l’équipe a comparé les profils protéiques et d’expression génique globaux entre les cellules sensibles au midostaurin et celles qui ne l’étaient pas. Les échantillons non répondeurs étaient enrichis en caractéristiques de cellules progénitrices immatures, de type souche — des cellules proches de la racine de la formation du sang et considérées comme des « graines » capables de relancer la leucémie. En revanche, les échantillons répondeurs ressemblaient davantage à des cellules myéloïdes et immunitaires partiellement matures. À l’aide de méthodes avancées en cellule unique, les scientifiques ont identifié une population spécifique de cellules leucémiques marquée par les protéines de surface CD38 et CD45RA qui se comportait comme ces graines de type progéniteur. Ces cellules présentaient une organisation inhabituelle de leur membrane externe, suggérant que des molécules de signalisation clés y étaient arrangées d’une manière favorisant la survie.
« Câblage » de survie : un basculement des voies de signalisation
Le midostaurin est conçu pour bloquer la signalisation FLT3, qui alimente normalement une chaîne de signaux incluant une molécule appelée STAT5 et pouvant entraîner la prolifération cellulaire. Lorsque l’équipe a examiné la signalisation dans des lignées cellulaires et des échantillons de patients après traitement par midostaurin, deux schémas distincts sont apparus. Dans les cellules sensibles au midostaurin, l’activité de STAT5 chutait rapidement, cohérente avec une inhibition efficace de FLT3. Dans les cellules résistantes, cependant, une autre voie dominait : PI3K/AKT, une voie de survie classique qui aide les cellules à résister à la mort. Ces cellules résistantes maintenaient voire augmentaient l’activité d’AKT après traitement et présentaient des niveaux plus élevés de protéines bloquant l’apoptose (mort cellulaire programmée). Autrement dit, le câblage intracellulaire de ces cellules de type progéniteur semblait réorienté pour favoriser la survie même lorsque FLT3 était inhibé.
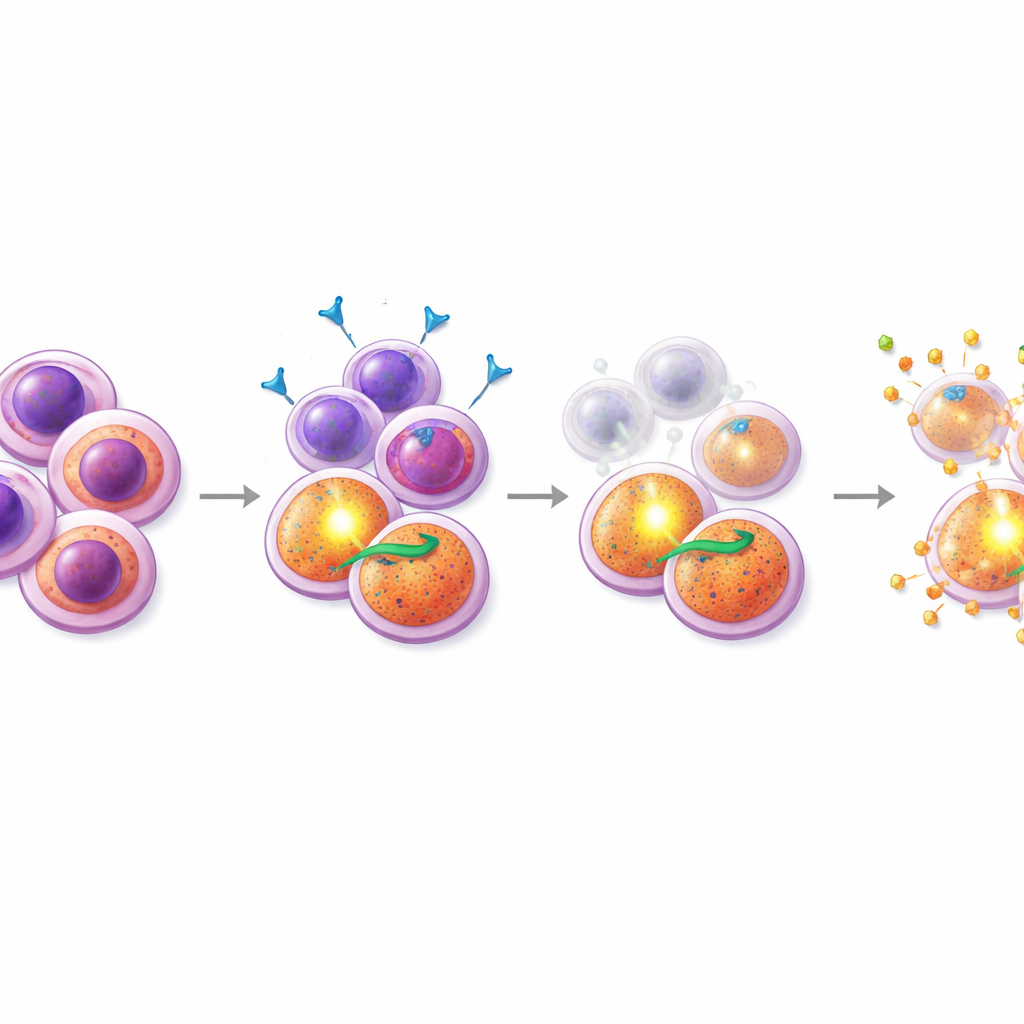
Trouver un médicament partenaire qui frappe au point faible
Avec cette connaissance, les chercheurs ont dépisté des combinaisons de midostaurin avec des centaines d’autres composés, en se concentrant sur des médicaments qui influencent la mort cellulaire. Un groupe s’est démarqué : les mimétiques de SMAC, des médicaments qui neutralisent les protéines « inhibitrices de l’apoptose » dont dépendent les cellules pilotées par PI3K/AKT. Dans des échantillons de patients résistants et dans une lignée cellulaire mutée FLT3 résistante, l’ajout de mimétiques de SMAC tels que le birinapant au midostaurin a produit une forte synergie : ensemble, les médicaments ont tué bien plus de cellules que chacun pris séparément. De manière cruciale, des expériences détaillées de cytométrie en flux ont montré que la combinaison midostaurin–mimétique de SMAC appauvrissait sélectivement la population progénitrice CD38+CD45RA+ et réduisait les niveaux caractéristiques de ses marqueurs de surface, suggérant que cette thérapie cible spécifiquement ces graines difficiles à éliminer. En revanche, les combinaisons avec l’inhibiteur approuvé de BCL‑2, le venetoclax, étaient plus efficaces contre un autre sous‑groupe à forte expression de CD34 et n’affichaient pas le même effet ciblé sur les cellules résistantes.
Ce que cela signifie pour les patients
Ce travail suggère que la résistance au midostaurin ne se résume pas à la mutation FLT3 elle‑même, mais concerne aussi « l’état » des cellules leucémiques — leur niveau de maturité, l’organisation de leur membrane et les voies de survie privilégiées. Un sous‑groupe de type progéniteur CD38+CD45RA+ semble constituer un réservoir clé de résistance, déplaçant sa signalisation de la voie STAT5 habituelle vers un programme de survie PI3K/AKT. En associant midostaurin et mimétiques de SMAC, les chercheurs ont pu resensibiliser ces cellules et les conduire à la mort en laboratoire. Bien que des études cliniques plus larges soient encore nécessaires, les résultats ouvrent la voie à un avenir où les cliniciens pourraient utiliser des tests fonctionnels et le profilage de l’état cellulaire, et pas seulement le séquençage de l’ADN, pour choisir des combinaisons ciblant FLT3 capables d’éliminer à la fois la masse leucémique et ses graines les plus résistantes.
Citation: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Mots-clés: leucémie myéloïde aiguë, inhibiteurs de FLT3, résistance aux médicaments, cellules souches leucémiques, mimétiques de SMAC