Clear Sky Science · fr
Les fibroblastes associés au cancer à haute expression de COL3A1 orchestrent les microenvironnements métabolique et immunitaire pour conférer une chimiorésistance dans le cancer du sein
Pourquoi certains tumeurs du sein résistent à la chimiothérapie
La chimiothérapie peut sauver des vies dans le cancer du sein, mais de nombreux patients constatent que leurs tumeurs cessent de répondre ou ne répondent pas bien dès le départ. Cette étude dépasse les seules cellules cancéreuses pour examiner le voisinage dans lequel elles vivent et poser la question : quelles cellules voisines aident les tumeurs à survivre au traitement, et comment s’y prennent-elles ? La réponse se concentre sur un groupe particulier de cellules de soutien qui réorientent à la fois la nutrition tumorale et l’immunité locale pour protéger les cellules cancéreuses de la chimiothérapie.
Les aides cachées autour de la tumeur
Les tumeurs du sein ne sont pas seulement des cellules cancéreuses ; ce sont des communautés mixtes qui incluent des vaisseaux sanguins, des cellules immunitaires et des cellules du tissu conjonctif appelées fibroblastes. Lorsque les fibroblastes résident dans une tumeur, on les appelle fibroblastes associés au cancer, ou FAC, et ils peuvent soit freiner soit favoriser le cancer. En combinant plusieurs méthodes puissantes de profilage génétique sur des échantillons de patients — analyses en cellule unique, spatiales et en vrac — ainsi que des expériences en laboratoire et sur animaux, les chercheurs ont identifié un sous-groupe de FAC qui produit de fortes quantités d’une molécule appelée COL3A1, un composant de l’échafaudage tissulaire. Les patients dont les tumeurs contenaient plus de ces FAC à haute expression de COL3A1 avaient plus de risques de mal répondre à la chimiothérapie et de survie réduite.
Un bouclier à deux volets : carburant et protection
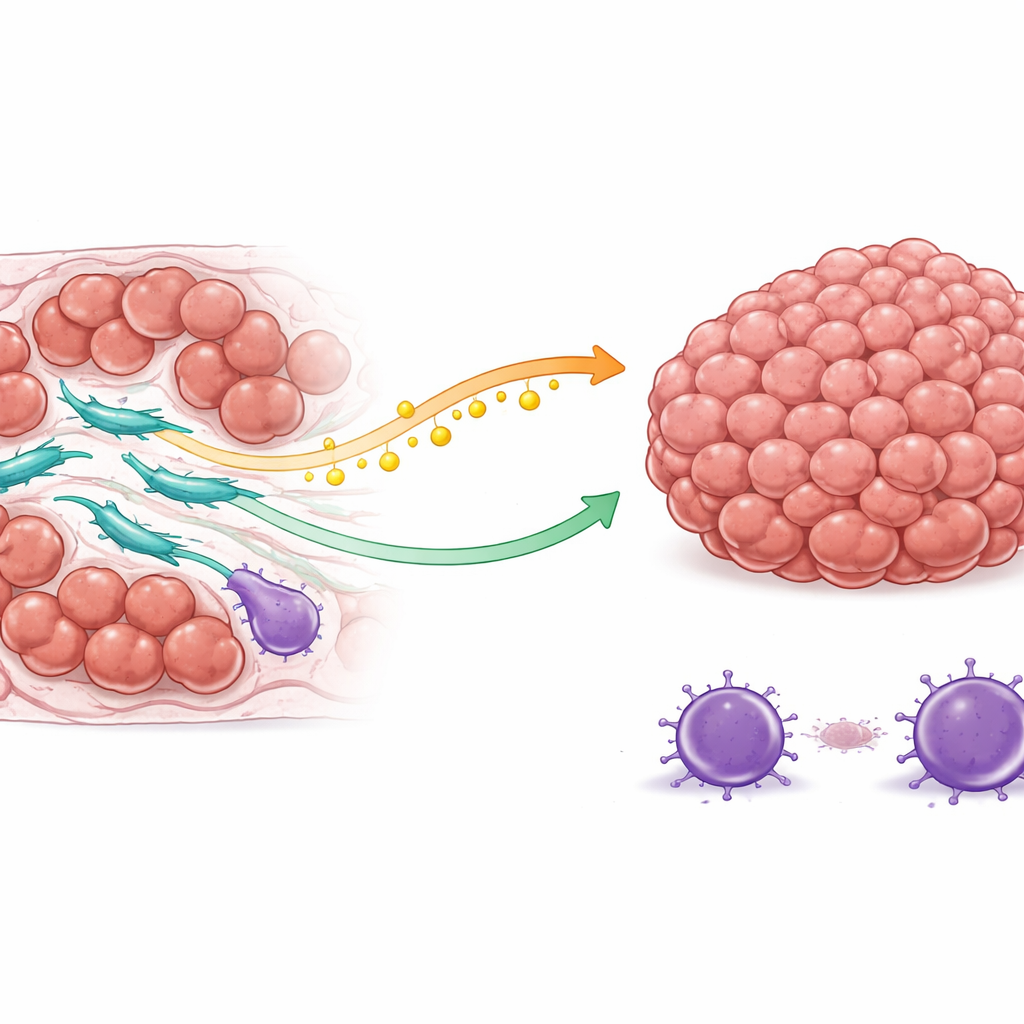
L’équipe a découvert que les FAC à haute expression de COL3A1 protègent les cellules cancéreuses de deux manières principales. D’abord, elles modifient leur gestion des lipides. Ces fibroblastes augmentent l’activité d’une enzyme qui fabrique de l’acide oléique, un type de lipide. Plutôt que de conserver ce carburant, elles le libèrent dans le microenvironnement tumoral. Les cellules cancéreuses captent cet acide oléique via une protéine de surface et, en réponse, activent une voie de survie interne connue pour aider les cellules à résister aux signaux d’apoptose. Ainsi, quand la chimiothérapie tente de déclencher des programmes d’autodestruction dans les cellules cancéreuses, celles-ci sont mieux équipées pour résister et continuer à se diviser.
Façonner un voisinage immunitaire peu accueillant
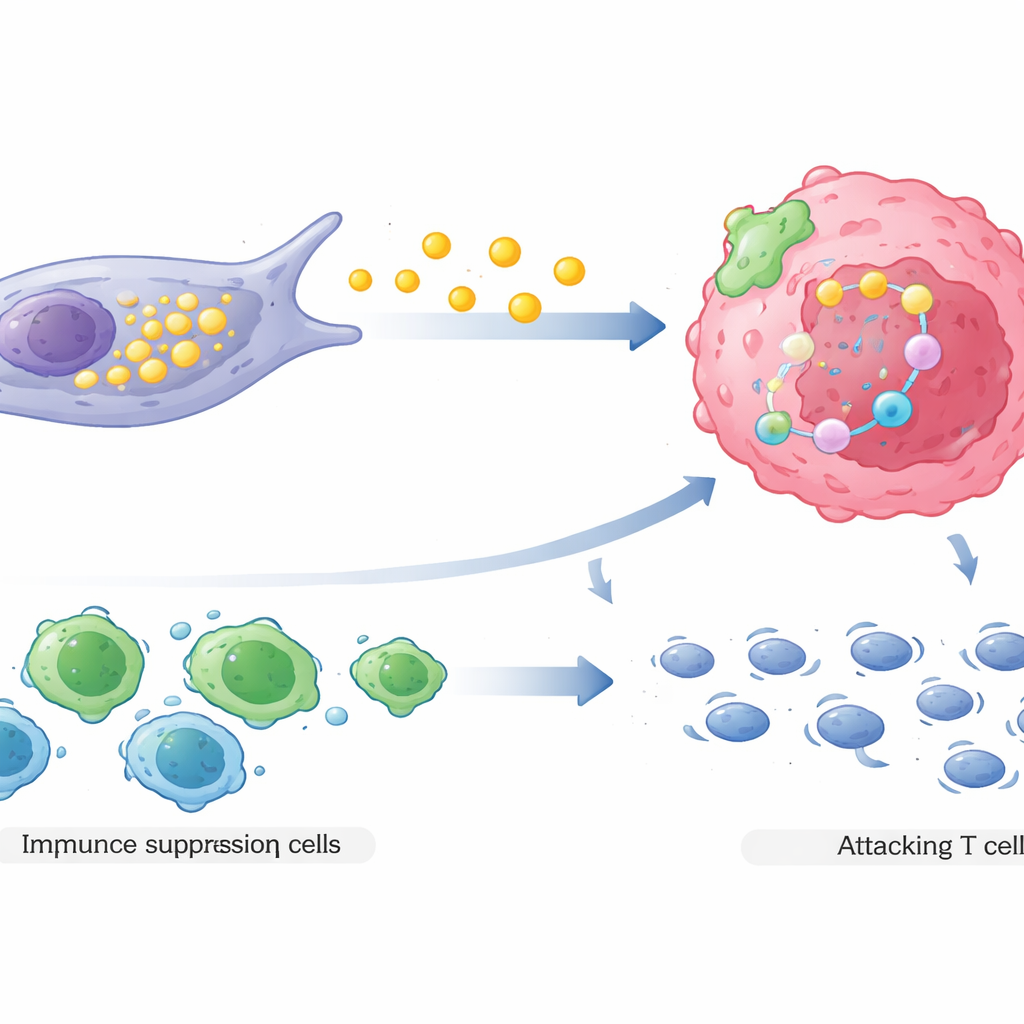
Ensuite, les FAC à haute expression de COL3A1 remodelent le paysage immunitaire local en faveur de la tumeur. Par des interactions complexes de signalisation, elles attirent des cellules T régulatrices, un type de cellules immunitaires qui atténue les attaques immunitaires, tout en décourageant ou affaiblissant les cellules T cytotoxiques qui attaqueraient normalement le cancer. La cartographie spatiale de tumeurs de patients réels a montré que ces fibroblastes ont tendance à se situer près des cellules cancéreuses résistantes aux médicaments et des cellules immunitaires suppressives, tandis que les cellules T tueuses efficaces sont repoussées plus loin. Cet agencement crée une zone abritée où les cellules cancéreuses font face à moins de menaces immunitaires au moment même où elles deviennent plus difficiles à éliminer par les médicaments.
Preuves issues de cellules, de souris et de patients
Pour tester la causalité, les chercheurs ont réduit l’expression de COL3A1 dans des FAC cultivés en laboratoire. Lorsque des cellules de cancer du sein ont été cultivées aux côtés de ces fibroblastes modifiés, elles ont formé moins de structures invasives, ont été plus facilement tuées par le médicament chimiothérapeutique paclitaxel et ont montré davantage de signes d’apoptose programmée. Chez des souris implantées avec des mélanges de cellules cancéreuses et de FAC, bloquer COL3A1 dans les fibroblastes a ralenti la croissance tumorale sous chimiothérapie et diminué les niveaux de l’enzyme de synthèse lipidique ainsi que du récepteur des cellules cancéreuses lié à l’acide oléique. Dans un groupe de 72 patients traités par chimiothérapie avant chirurgie, des niveaux plus élevés de COL3A1 et de ses partenaires du métabolisme lipidique correspondaient fortement à de moins bonnes réponses au traitement et à un délai avant récidive plus court.
Ce que cela signifie pour les traitements futurs
En résumé, l’étude montre qu’un ensemble particulier de cellules de soutien dans les tumeurs mammaires agit comme une unité de garde du corps : elles nourrissent les cellules cancéreuses avec un régime protecteur à base de lipides et attirent des alliés immunitaires qui estompent les défenses de l’organisme. Ensemble, ces actions rendent la chimiothérapie moins efficace. Mesurer l’abondance des fibroblastes à haute expression de COL3A1 améliore la capacité des médecins à prédire qui répondra ou non au traitement, et les voies qu’ils utilisent — production de lipides, signalisation de survie intracellulaire et affaiblissement immunitaire — offrent de nouvelles cibles thérapeutiques. À l’avenir, des thérapies visant à désarmer ou reprogrammer ces fibroblastes pourraient être associées à la chimiothérapie standard pour empêcher les tumeurs de développer une résistance.
Citation: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Mots-clés: cancer du sein, chimiorésistance, microenvironnement tumoral, fibroblastes associés au cancer, métabolisme des lipides