Clear Sky Science · fr
Validation clinique d'un test d'enrichissement du méthylome génome-entier, indépendant du tissu, pour surveiller la réponse au pembrolizumab
Surveiller le traitement du cancer par une simple prise de sang
Les patients atteints de cancers avancés et leurs médecins attendent souvent des semaines ou des mois pour savoir si un médicament d'immunothérapie fonctionne réellement. Les scanners peuvent être difficiles à interpréter, et les biopsies tissulaires répétées sont invasives voire impossibles. Cette étude explore un nouveau type de test sanguin qui lit de minuscules marques chimiques sur l'ADN tumoral circulant dans le sang, offrant un moyen plus rapide et moins invasif de savoir si le pembrolizumab est efficace.
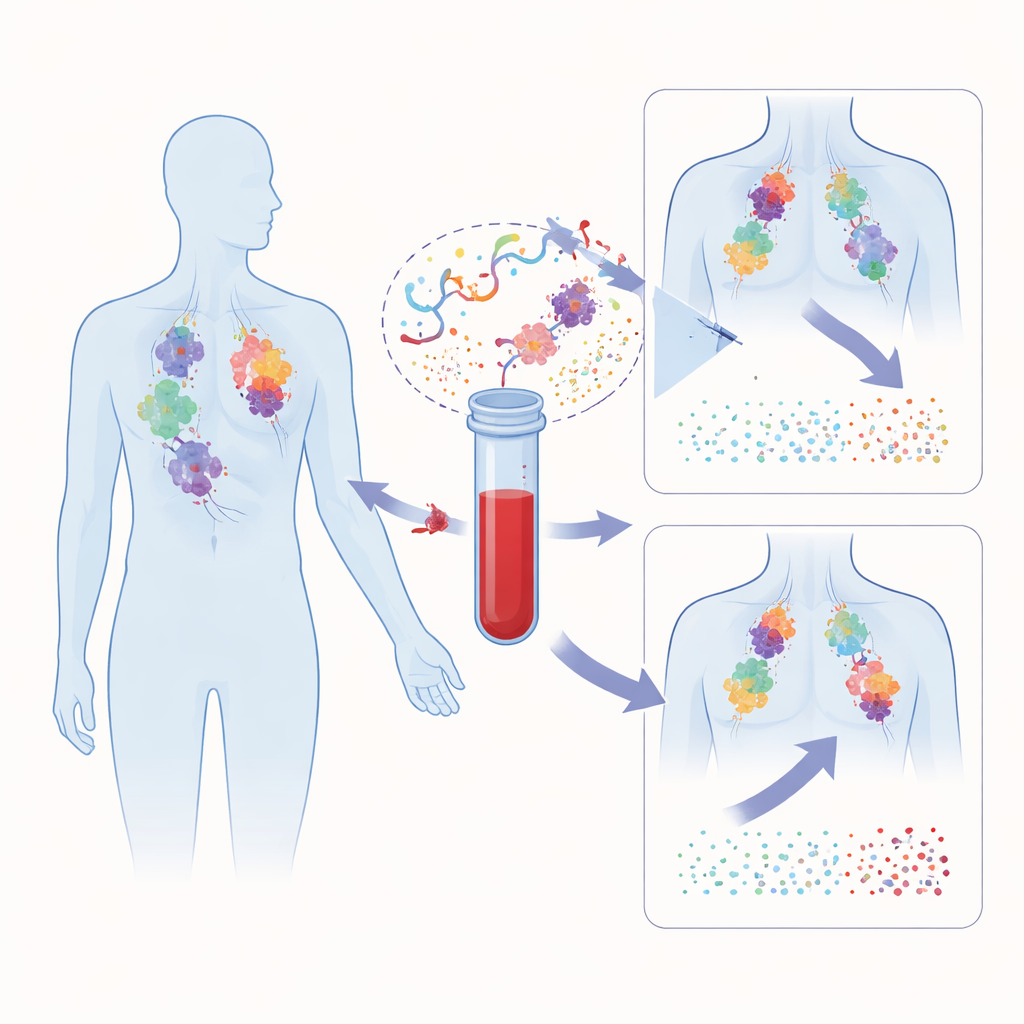
Pourquoi les contrôles actuels ne suffisent pas
Les médicaments d'immunothérapie comme le pembrolizumab peuvent produire des réponses remarquables et durables, mais seulement chez une fraction des patients. Aujourd'hui, les cliniciens s'appuient sur des caractéristiques tumorales comme les niveaux de PD-L1 ou le nombre de mutations mesurés à partir de biopsies tissulaires, ainsi que sur des examens d'imagerie périodiques. Ces approches présentent des inconvénients importants : les échantillons de biopsie ne sont pas toujours disponibles, peuvent ne pas refléter l'intégralité de la tumeur et sont généralement mesurés une seule fois avant le début du traitement. L'imagerie peut être trompeuse parce que l'afflux de cellules immunitaires dans la tumeur peut temporairement l'agrandir, un phénomène connu sous le nom de pseudoprogression. Ensemble, ces limites font que des patients peuvent poursuivre des thérapies inefficaces pendant des mois avant qu'il soit clair qu'elles ne fonctionnent pas.
Un test sanguin universel au lieu de biopsies tumorales
Les chercheurs ont testé un dosage sanguin « indépendant du tissu » qui ne nécessite pas d'échantillon tumoral préalable. Il se concentre plutôt sur la méthylation de l'ADN — des marqueurs chimiques stables qui ornent l'ADN et diffèrent entre cellules saines et cellules cancéreuses. Les tumeurs libèrent en permanence des fragments d'ADN dans la circulation sanguine, créant de l'ADN tumoral circulant (ctDNA). À l'aide d'une technique appelée cfMeDIP-seq, l'équipe enrichit et séquence uniquement les fragments méthylés provenant du plasma, puis applique un classifieur entraîné sur de larges jeux de données cancéreuses et non cancéreuses. Cela produit un score numérique de ctDNA reflétant la quantité d'ADN d'origine tumorale présente dans le sang, indépendamment du site d'origine du cancer dans l'organisme.
Suivre la réponse au pembrolizumab dans de nombreux cancers
Pour évaluer si ce test pouvait suivre la réponse à l'immunothérapie, les scientifiques ont analysé 241 échantillons sanguins de 69 personnes atteintes de divers tumeurs solides avancées incluses dans l'essai INSPIRE. Les participants, n'ayant pas reçu d'immunothérapie auparavant, ont été traités par pembrolizumab seul et ont eu des prélèvements sanguins avant le traitement puis tous les trois cycles, en commençant autour du troisième traitement. La question principale était simple : le score de ctDNA augmente-t-il ou diminue-t-il entre le début du traitement et le troisième cycle ? Les patients ont été regroupés en conséquence et suivis pour la réponse tumorale, le temps sans progression de la maladie et la survie globale.
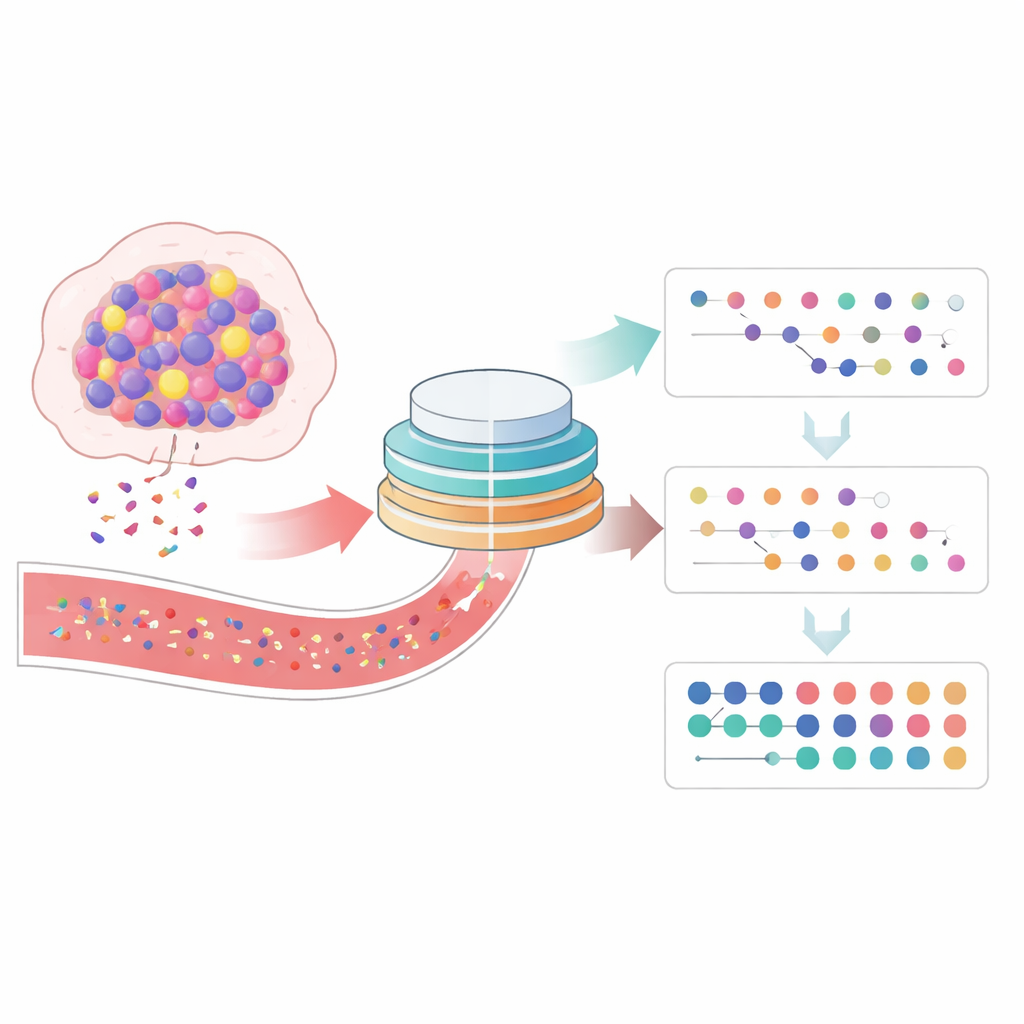
Ce que les changements dans l'ADN tumoral ont révélé
La moitié des patients ont montré une baisse du score de ctDNA au troisième cycle, et l'autre moitié une augmentation. Le schéma précoce était frappant : aucun des patients dont le ctDNA avait augmenté n'a présenté une réduction tumorale significative, et presque tous n'ont tiré aucun bénéfice de la thérapie. En revanche, presque tous les patients ayant répondu cliniquement avaient une diminution du ctDNA. Une chute du score était fortement associée à de meilleures chances de réduction tumorale, à des périodes plus longues avant la progression de la maladie et, dans des analyses plus simples, à une survie globale plus longue. Lorsque l'équipe a regardé au-delà de ce point temporel unique, elle a constaté que les patients dont les niveaux de ctDNA sont restés en dessous de leur valeur initiale tout au long du traitement avaient tendance à vivre plus longtemps et à rester plus longtemps sans progression que ceux dont le ctDNA a dépassé la valeur de base à un moment donné.
Comparaison de ce test avec d'autres signaux
L'équipe a également comparé les variations de ctDNA à des marqueurs plus familiers tels que l'expression de PD-L1 et la charge mutationnelle tumorale mesurées à partir du tissu. Alors que des niveaux plus élevés de PD-L1 montraient une certaine relation avec le bénéfice dans des analyses de base, ces marqueurs tissulaires perdaient leur signification une fois que la dynamique du ctDNA était incluse dans des modèles plus complexes. En revanche, les variations précoces du ctDNA restaient un indicateur fort et indépendant du pronostic des patients, en particulier pour la survie sans progression. Fait important, cette performance égalait celle obtenue précédemment avec des tests de ctDNA personnalisés et informés par la tumeur, qui requièrent un séquençage préalable de la tumeur de chaque patient — alors que le nouvel essai fonctionne uniquement à partir du sang et peut être appliqué à de nombreux types de cancer.
Ce que cela pourrait signifier pour les patients
Concrètement, cette étude suggère qu'un test sanguin spécialisé peut indiquer, en quelques cycles de traitement, si le pembrolizumab aide probablement le patient. Une baisse soutenue de l'ADN tumoral dans le sang signale une meilleure probabilité de bénéfice, tandis que des niveaux en hausse avertissent que la maladie peut résister à la thérapie. Parce que la méthode ne dépend pas de la disponibilité d'un tissu tumoral et peut être répétée dans le temps, elle pourrait permettre aux médecins de prendre des décisions plus tôt et mieux informées concernant la poursuite, le changement ou l'intensification du traitement. Des essais prospectifs de plus grande envergure seront nécessaires, mais ce travail fournit des preuves solides que la lecture des profils de méthylation de l'ADN tumoral circulant pourrait devenir un outil puissant et largement utilisable pour guider l'immunothérapie.
Citation: Stutheit-Zhao, E.Y., Zhong, Y., Melton, C.A. et al. Clinical validation of a tissue-agnostic genome-wide methylome enrichment assay to monitor response to pembrolizumab. npj Precis. Onc. 10, 129 (2026). https://doi.org/10.1038/s41698-026-01327-y
Mots-clés: ADN tumoral circulant, suivi de l'immunothérapie, biopsie liquide, méthylation de l'ADN, pembrolizumab