Clear Sky Science · fr
L’acide valproïque renverse la résistance au témozolomide médiée par les macrophages dans les gliomes riches en macrophages
Retourner les auxiliaires du corps contre les tumeurs cérébrales
Les tumeurs cérébrales appelées gliomes sont notoirement difficiles à traiter, en partie parce qu’elles cessent souvent de répondre au principal chimiothérapeutique, le témozolomide. Cette étude explore un allié inattendu dans la lutte : un médicament anti‑épileptique utilisé de longue date, l’acide valproïque. En poussant certains globules blancs présents dans et autour de la tumeur à changer de camp, l’acide valproïque pourrait aider la chimiothérapie à mieux fonctionner chez les patients dont les tumeurs sont chargées de ces cellules.
Pourquoi le traitement standard échoue souvent
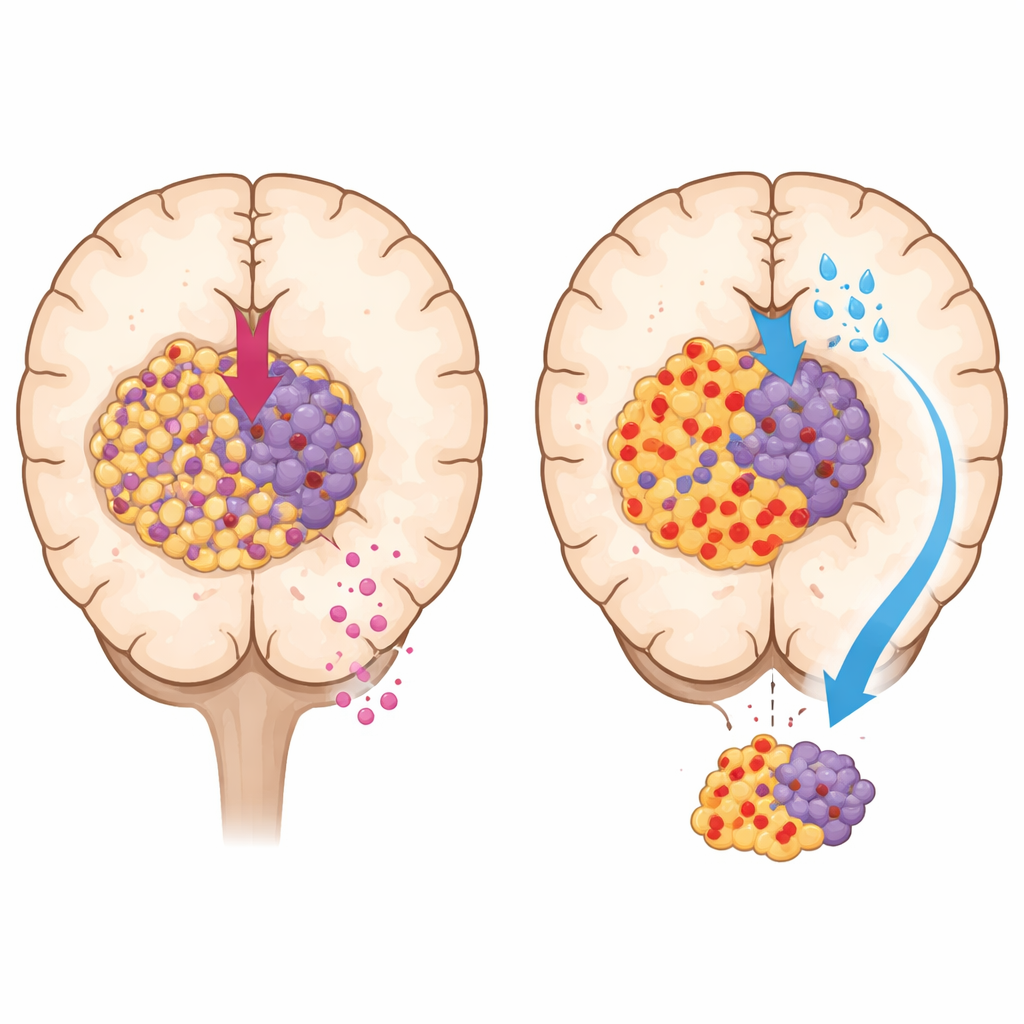
Pour les gliomes agressifs, en particulier le glioblastome, la chirurgie et la radiothérapie sont généralement suivies par du témozolomide. Pourtant, de nombreuses tumeurs résistent au médicament dès le départ ou deviennent résistantes avec le temps. Les travaux antérieurs avaient largement imputé cela à des changements à l’intérieur des cellules cancéreuses elles‑mêmes, par exemple dans leurs mécanismes de réparation de l’ADN. Mais les tumeurs des patients ne se réduisent pas aux seules cellules cancéreuses : elles évoluent dans un quartier complexe d’éléments immunitaires et de soutien. Parmi les plus abondants figurent les macrophages, un type de globule blanc qui peut soit attaquer les tumeurs soit, dans de mauvaises conditions, favoriser discrètement leur croissance.
Quand le voisinage tumoral bloque la thérapie
Les chercheurs ont comparé la réponse de plusieurs lignées de cellules de gliome au témozolomide en culture et chez la souris. Certaines lignées apparemment très sensibles en laboratoire devenaient obstinément résistantes une fois développées en tumeurs. La différence clé n’était pas la génétique des cellules cancéreuses, mais l’environnement entourant la tumeur. Les tumeurs résistantes chez l’animal étaient fortement infiltrées par des macrophages, en particulier une forme « réparatrice » qui tend à apaiser l’inflammation et à protéger la tumeur plutôt qu’à la détruire. Les analyses des données de patients et des échantillons tissulaires ont montré que les gliomes riches en ces macrophages avaient plus de risques de récidive après le traitement et étaient associés à une survie plus courte.
Deux anti‑épileptiques, deux effets immunitaires très différents
De nombreuses personnes atteintes de gliomes reçoivent des anti‑épileptiques tels que le lévétiracétam ou l’acide valproïque. Les deux ont été proposés comme compléments au témozolomide, mais leur impact sur le microenvironnement immunitaire de la tumeur n’avait pas été pleinement évalué. Dans cette étude, l’équipe a exposé des macrophages d’origine humaine à des signaux provenant de cellules de gliome, puis les a traités soit par lévétiracétam soit par acide valproïque. L’acide valproïque a systématiquement orienté les macrophages vers un état plus agressif, combattant la tumeur, caractérisé par une production accrue de molécules messagères pro‑attaque. Le lévétiracétam tendait au contraire à les pousser vers un état plus protecteur, soutenant la tumeur.
Reprogrammer les macrophages pour restaurer la sensibilité au médicament
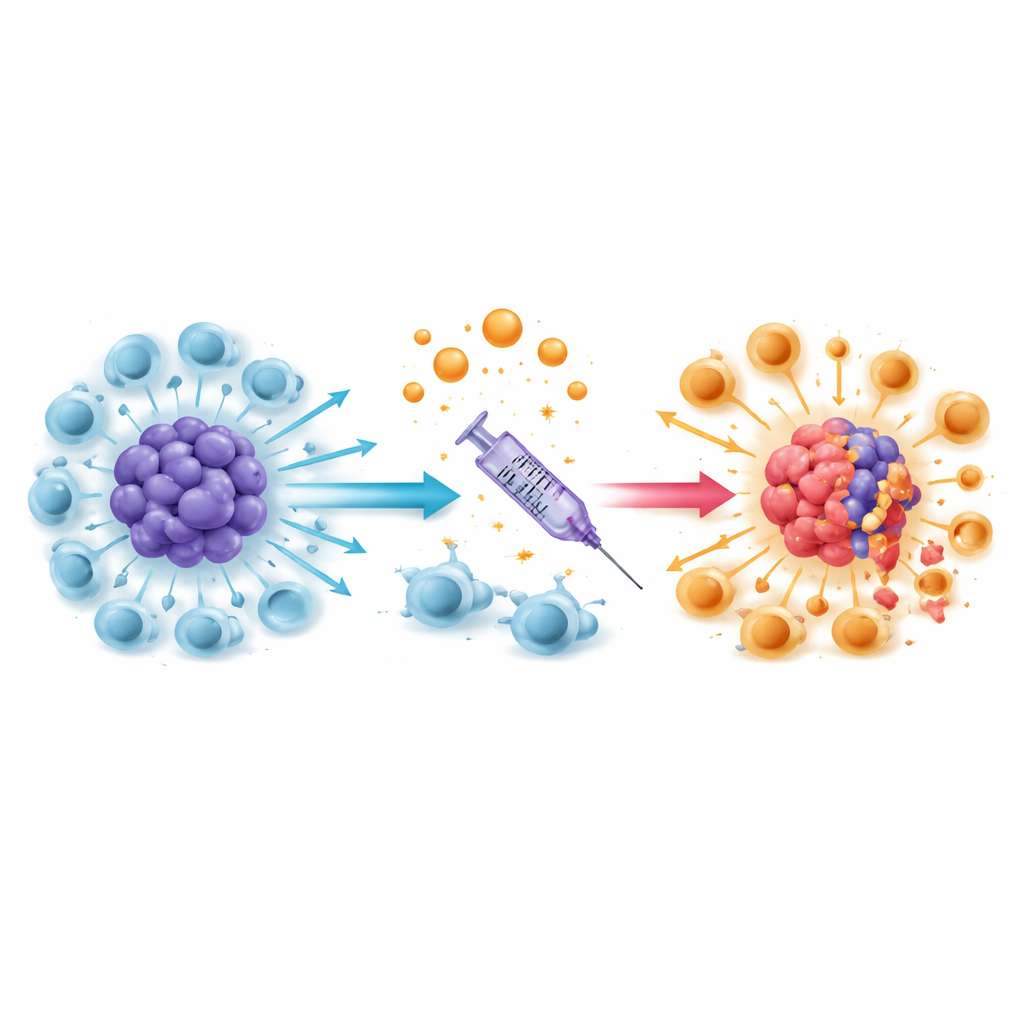
Les scientifiques se sont ensuite demandé si ces basculements immunitaires modifiaient réellement la réponse des tumeurs à la chimiothérapie. Lorsque les cellules de gliome étaient cultivées avec des macrophages ou avec le fluide provenant de macrophages, le témozolomide devenait moins efficace, reproduisant la résistance observée chez l’animal et chez les patients. Mais si les macrophages avaient été prétraités par l’acide valproïque, l’effet inverse se produisait : leurs sécrétions rendaient désormais les cellules de gliome plus vulnérables au témozolomide et réduisaient la production de plusieurs facteurs liés à la résistance. Dans des modèles murins de gliomes riches en macrophages, l’association acide valproïque plus témozolomide a ralenti la croissance tumorale et prolongé la survie davantage que le témozolomide seul ou le témozolomide associé au lévétiracétam. Les tumeurs des souris traitées par acide valproïque contenaient plus de macrophages de type « attaque » et moins de macrophages de type protecteur.
Vers des choix thérapeutiques plus personnalisés
Pris ensemble, les résultats suggèrent que, pour les gliomes envahis par des macrophages, l’acide valproïque pourrait jouer un double rôle : contrôler les crises tout en réarmant les cellules immunitaires entourant la tumeur afin que la chimiothérapie fonctionne comme prévu. Le lévétiracétam peut rester utile pour les tumeurs dont la résistance est davantage dictée par des voies internes de réparation de l’ADN que par leur voisinage cellulaire. Ce travail ne change pas encore la prise en charge standard, mais il propose une idée claire et testable pour des essais cliniques futurs : adapter le choix de l’anti‑épileptique à la biologie tumorale, en privilégiant l’acide valproïque lorsque les macrophages dominent, afin de transformer les anciens assistants de la tumeur en partenaires de sa destruction.
Citation: Ni, X., Chen, W., Xu, P. et al. Valproic acid reverses macrophage-mediated temozolomide resistance in macrophage-rich gliomas. npj Precis. Onc. 10, 120 (2026). https://doi.org/10.1038/s41698-026-01325-0
Mots-clés: glioblastome, résistance au témozolomide, microenvironnement tumoral, macrophages, acide valproïque