Clear Sky Science · fr
Prédire la déficience de recombinaison homologue et les réponses au traitement à l’aide d’un modèle de base basé sur la tomodensitométrie : une étude préclinique
Pourquoi cela compte pour les patients et les médecins
Les traitements du cancer qui endommagent l’ADN, comme certains chimiothérapies et de nouveaux médicaments ciblés, peuvent être particulièrement efficaces sur des tumeurs dont les systèmes de réparation sont déjà déficients. Le défi consiste à identifier quelles tumeurs présentent ces faiblesses cachées sans recourir à des biopsies répétées et invasives. Cette étude explore si des examens d’imagerie courants chez la souris, interprétés par un puissant modèle d’intelligence artificielle, peuvent révéler la vulnérabilité d’une tumeur et prédire sa réponse à un nouveau médicament expérimental.
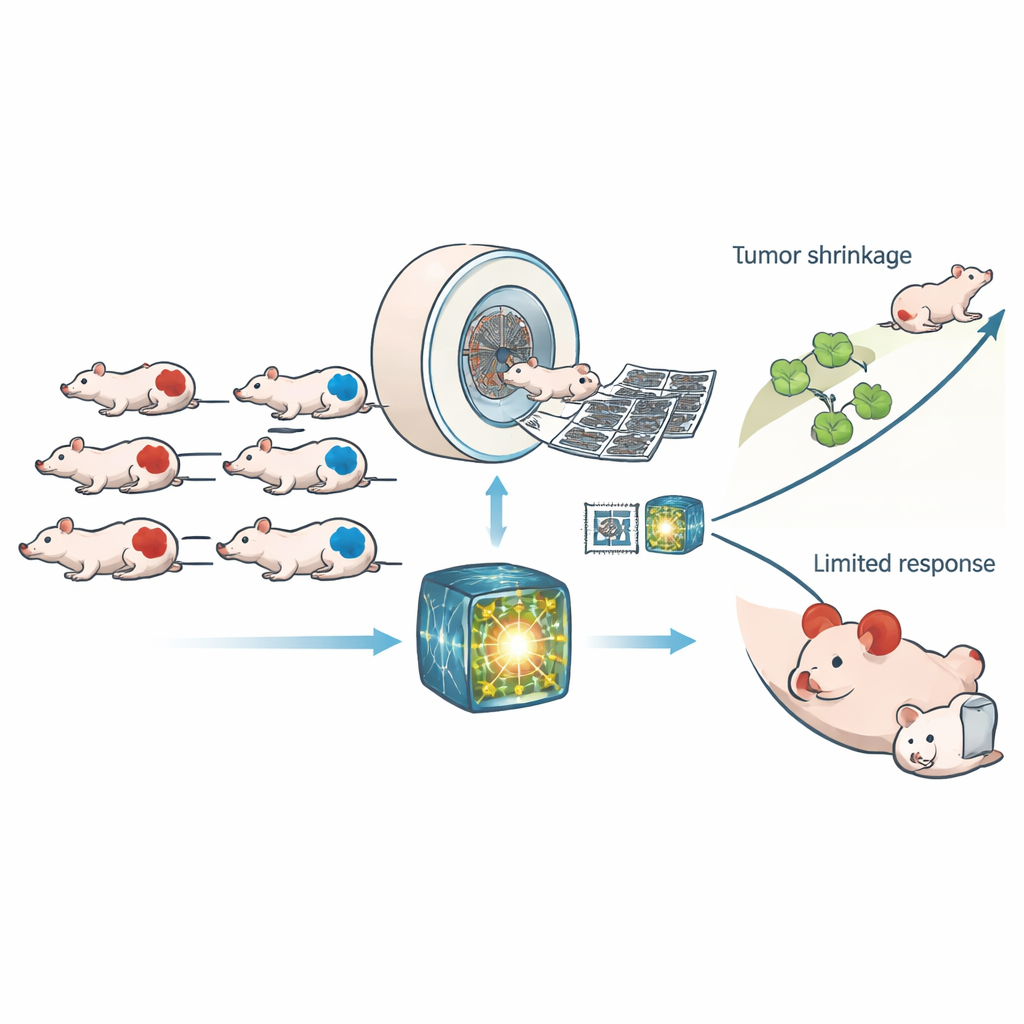
Un point faible caché dans les cellules cancéreuses
De nombreuses tumeurs présentent des défauts dans une voie clé de réparation de l’ADN appelée recombinaison homologue. Lorsque cette voie fait défaut, les cellules accumulent des lésions dans leur matériel génétique, une situation appelée déficience de recombinaison homologue, ou HRD. La HRD peut favoriser l’apparition de cancers, mais elle constitue aussi un talon d’Achille : des médicaments qui endommagent davantage l’ADN peuvent pousser ces cellules déjà stressées au-delà de leur seuil de survie, les tuant plus efficacement que les cellules saines. Aujourd’hui, l’identification de la HRD repose généralement sur des tests génétiques ou des essais de laboratoire spécialisés, coûteux, chronophages et souvent dépendants de prélèvements tumoraux. Les auteurs se sont demandés si l’imagerie — le même type de scans tridimensionnels par rayons X largement utilisés en clinique — pouvait offrir une fenêtre rapide et non invasive sur la HRD.
Utiliser des scans intelligents plutôt que davantage de biopsies
Les chercheurs ont travaillé avec 307 souris portant des greffons tumoraux humains, soit déficients en HRD soit normaux en capacité de réparation. Tous les animaux ont subi des tomodensitométries (CT) à haute résolution avant et après avoir reçu soit un traitement témoin, soit le CP‑506, un médicament expérimental qui s’active dans les régions hypoxiques des tumeurs et qui cross‑linke les brins d’ADN. Plutôt que de se limiter à une poignée de mesures d’image conçues manuellement, l’équipe a utilisé un « modèle de base » moderne, préentraîné sur de larges ensembles de CT humains, pour extraire des milliers de motifs subtils de chaque scan. Un classifieur simple a ensuite été entraîné sur ces motifs pour décider si une tumeur était HRD, et les mêmes caractéristiques apprises ont été réutilisées pour prédire l’ampleur des lésions d’ADN et le retard de croissance que provoquerait le CP‑506.
Performance du modèle d’imagerie
Le modèle de base a nettement surpassé à la fois la radiomique traditionnelle et un réseau profond standard entraîné de zéro. Sur de nouveaux scans de test, il a distingué les tumeurs HRD des non‑HRD avec une aire sous la courbe d’environ 0,88, un niveau de précision qui s’est maintenu à différents réglages d’énergie du CT. Lorsque les deux approches d’IA se sont mises d’accord sur le type de tumeur, la performance a encore augmenté. Le score HRD basé sur l’image s’alignait étroitement avec le statut génétique réel dans plusieurs lignées tumorales prostatiques et colorectales, bien qu’une lignée présentant un comportement de réparation atypique soit restée plus difficile à classer. Fait important, les caractéristiques CT associées à la HRD n’étaient pas de simples artefacts statistiques : elles ont également prédit l’ampleur des lésions d’ADN persistantes produites par le CP‑506 48 heures après le traitement et le temps nécessaire aux tumeurs pour repousser jusqu’à quatre fois leur volume dans une expérience parallèle.
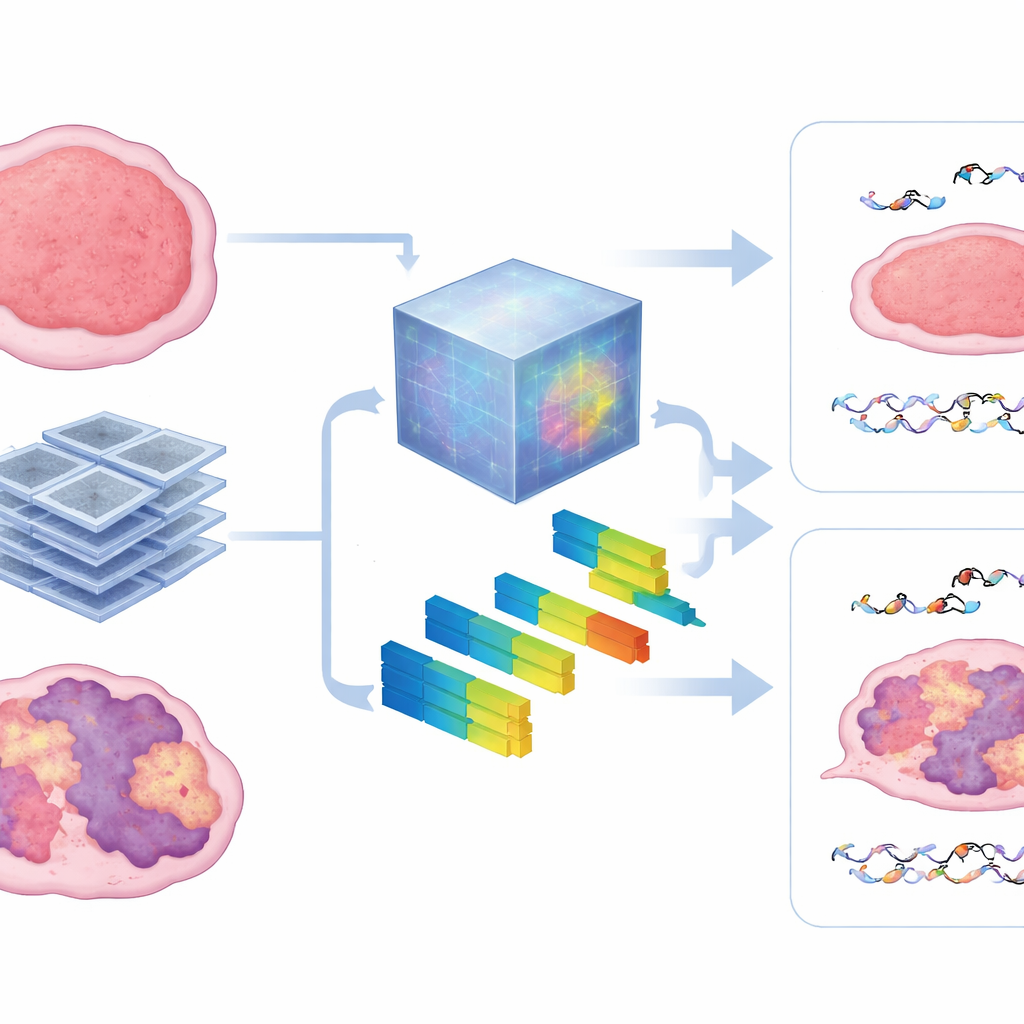
Ce que les scans révèlent à l’intérieur de la tumeur
Pour sonder la « boîte noire », les auteurs ont comparé les motifs appris par le modèle de base avec des caractéristiques radiomiques classiques décrivant la texture et l’intensité de l’image. Ils ont constaté que le modèle s’appuyait fortement sur des mesures d’hétérogénéité — à quel point la tumeur apparaissait en taches, grossière ou irrégulière sur le CT. Les tumeurs présentant des signatures HRD plus marquées avaient tendance à montrer des textures plus désorganisées, et ces mêmes caractéristiques ont aidé à prédire à la fois les lésions microscopiques de l’ADN et le contrôle macroscopique de la tumeur. L’approche est restée robuste lorsque moins de données d’entraînement étaient disponibles, suggérant que de tels modèles préentraînés peuvent surmonter un obstacle majeur des études animales, où il est difficile de collecter de larges jeux de données d’imagerie.
Des expériences sur la souris aux soins futurs des patients
Ce travail préclinique montre qu’un seul scan CT, interprété via une IA puissante et préentraînée, peut capter des signaux de réparation défectueuse de l’ADN et anticiper l’intensité de la réponse d’une tumeur à un médicament endommageant l’ADN. Pour un non‑spécialiste, la conclusion est que des scans apparemment standard pourraient bientôt remplir une double fonction — localiser la tumeur et révéler sa fragilité — sans procédures supplémentaires. Avant que cela n’intègre la pratique courante, la méthode doit être testée et validée chez l’humain. Si ces efforts réussissent, des empreintes digitales IA de la HRD basées sur le CT pourraient aider les médecins à adapter plus précisément les patients à des traitements comme le CP‑506 et des thérapies apparentées, améliorant les résultats tout en épargnant à d’autres des médicaments inefficaces et toxiques.
Citation: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Mots-clés: déficience de recombinaison homologue, imagerie du cancer, radiomique, modèles de base, thérapie endommageant l’ADN