Clear Sky Science · fr
Développement et validation d’un modèle basé sur l’intelligence artificielle pour diagnostiquer les masses annexielles bénignes, borderline et malignes
Pourquoi cela compte pour la santé des femmes
Les masses ovariennes et autres masses annexielles sont des découvertes fréquentes à l’échographie pelvienne, mais distinguer celles qui sont inoffensives de celles qui signalent un cancer précoce reste difficile, même pour les experts. Cette étude présente un nouveau système d’intelligence artificielle (IA), nommé Clinical‑OMTA, qui interprète les images échographiques et aide les médecins à classer ces masses en trois groupes clés — bénin, borderline et malin — afin que les patientes reçoivent le traitement adapté tout en évitant des chirurgies inutiles.
Trois types de lésions, trois décisions très différentes
Toutes les masses annexielles ne se valent pas. Les lésions bénignes peuvent souvent être surveillées ou enlevées par une intervention simple. Les tumeurs malignes sont des cancers mettant la vie en danger qui nécessitent une chirurgie spécialisée et une chimiothérapie. Les tumeurs borderline se situent entre les deux : elles peuvent récidiver mais touchent souvent des femmes plus jeunes qui souhaitent préserver leur fertilité, si bien que les chirurgiens cherchent à n’enlever que le strict nécessaire. Malheureusement, à l’échographie ces trois catégories peuvent paraître très similaires. Les tumeurs borderline en particulier peuvent mimer soit un kyste bénin soit un cancer agressif, rendant les décisions thérapeutiques stressantes pour les patientes et les cliniciens.
Transformer des examens complexes en réponses plus claires
L’échographie est généralement le premier et le plus accessible examen pour les masses annexielles, mais interpréter des images granuleuses et très variables demande beaucoup d’expérience. Les systèmes de score et calculateurs de risque existants, comme le modèle ADNEX largement utilisé, combinent des caractéristiques échographiques spécifiques et des informations cliniques simples comme l’âge et un marqueur sanguin (CA125), mais ils reposent toujours sur l’observateur humain pour décrire correctement les images. Les avancées récentes en apprentissage profond — une branche de l’IA qui apprend des motifs directement à partir des pixels — offrent la possibilité de réduire cette subjectivité en entraînant des ordinateurs à reconnaître des signatures d’image subtiles propres à différents types tumoraux.
Un assistant IA entraîné dans de nombreux hôpitaux
S’appuyant sur des travaux antérieurs, les auteurs ont conçu Clinical‑OMTA, un modèle IA à double voie qui sépare d’abord les masses bénignes des masses non bénignes, puis distingue les lésions borderline des lésions malignes. Le système analyse des images échographiques en niveaux de gris et peut aussi prendre en entrée, de façon optionnelle, l’âge et les valeurs de CA125. Pour entraîner et tester le modèle, l’équipe a constitué un vaste jeu de données diversifié : 2381 femmes provenant de 23 hôpitaux à travers la Chine, examinées avec 38 types d’appareils échographiques. La plupart des cas disposaient d’une confirmation chirurgicale du diagnostic ; un plus petit groupe de kystes clairement bénins a été confirmé par au moins six mois de suivi échographique. Les données ont été réparties en ensembles d’entraînement, en jeux de test internes et en deux cohortes de test externes totalement indépendantes, comprenant à la fois des images fixes et de courtes vidéos balayées des ovaires. 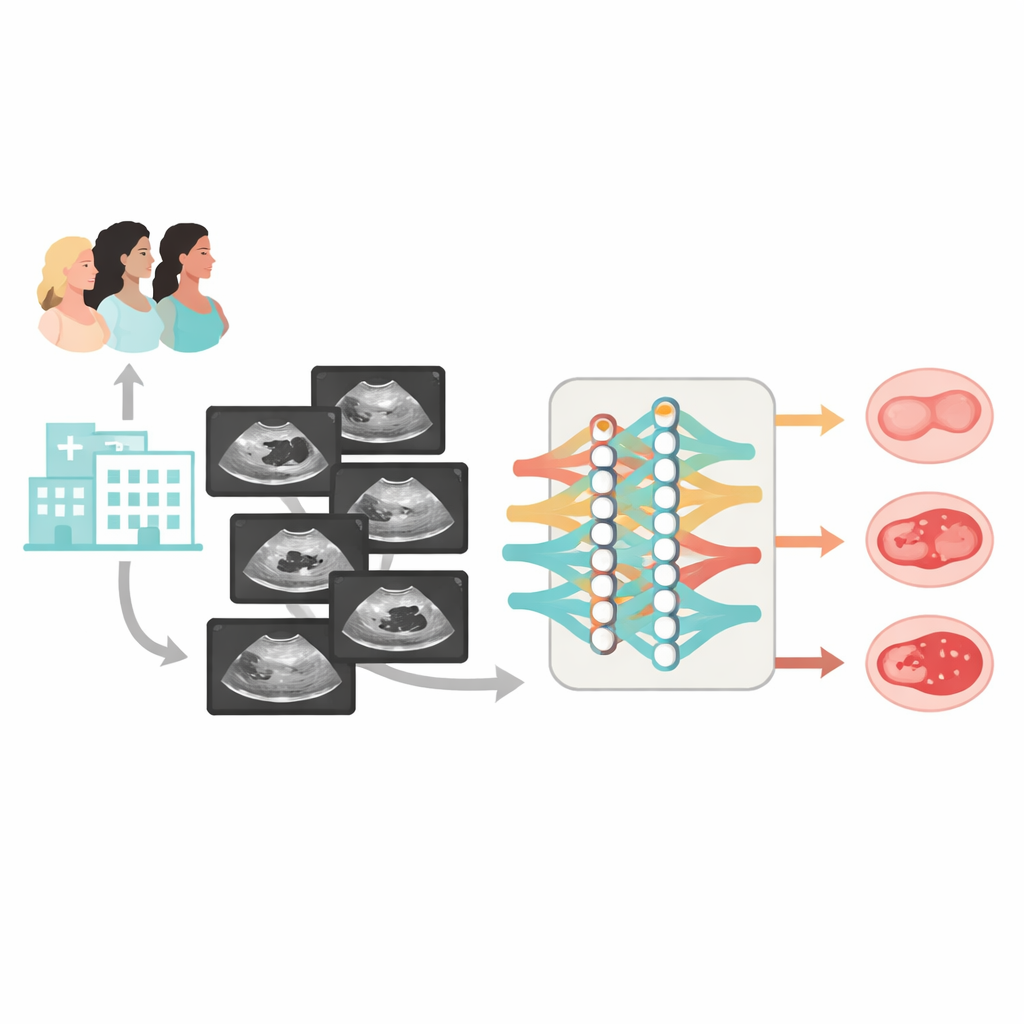
Performance de l’IA en conditions réelles
Sur les images de test externes, Clinical‑OMTA a correctement différencié les masses bénignes, borderline et malignes avec une précision comparable à celle du modèle ADNEX et au jugement d’un examinateur échographique expert. Ses performances se sont montrées stables entre différentes marques d’appareils, modes d’examen (abdominal ou transvaginal) et entre les deux hôpitaux externes, ce qui suggère que le modèle n’est pas excessivement adapté à un appareil ou centre particulier. Le système a également bien fonctionné sur des clips vidéo, pas seulement sur des images fixes. Fait intéressant, l’ajout de l’âge et du CA125 n’a pas amélioré ses décisions par rapport à l’utilisation des images échographiques seules, confirmant des études antérieures montrant que ce marqueur sanguin apporte peu dès lors que l’imagerie est de haute qualité. 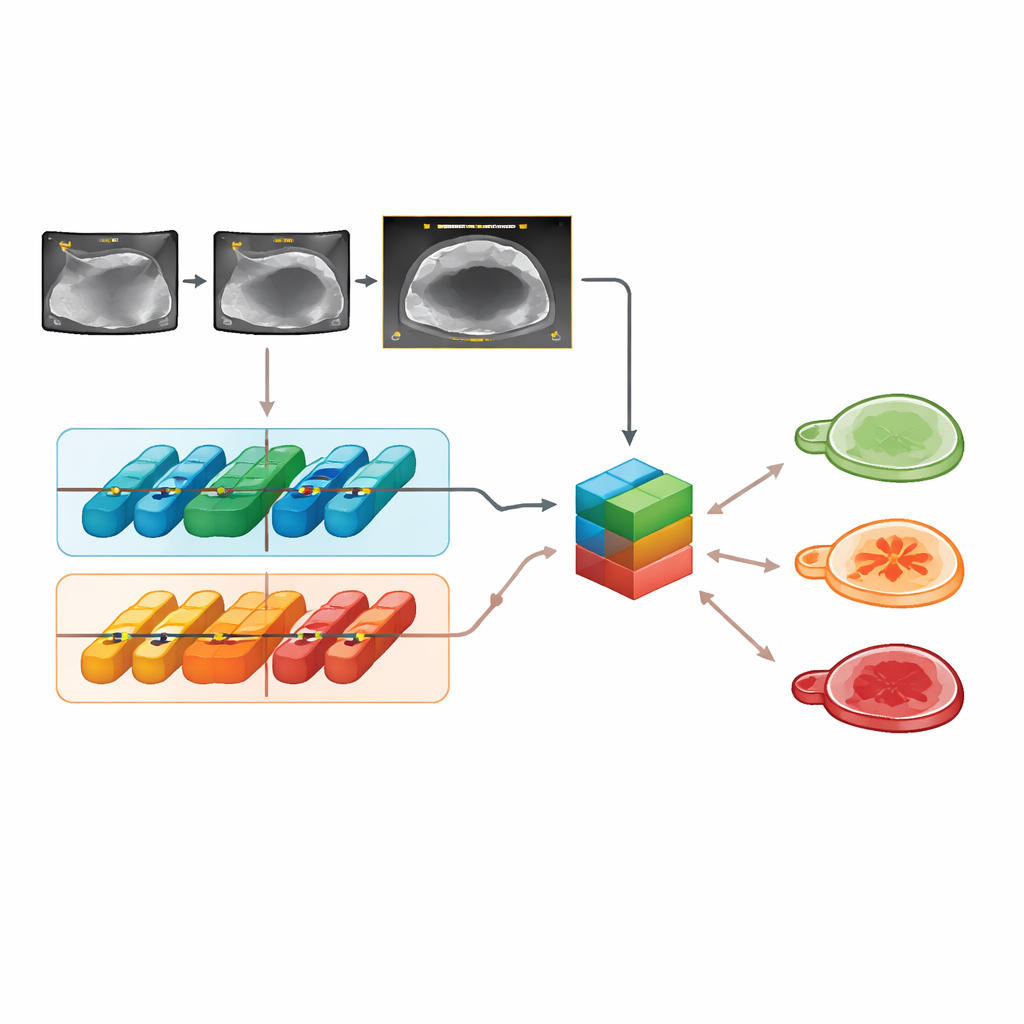
Aider les médecins moins expérimentés, et ses limites
Les chercheurs ont ensuite demandé à 11 radiologues — juniors, intermédiaires et très expérimentés — de classer les mêmes cas, d’abord sans aide puis en disposant de la sortie de l’IA et de cartes de chaleur (heat‑maps) qui mettent en évidence les régions de l’image jugées importantes par le modèle. Avec l’aide de Clinical‑OMTA, la précision des médecins juniors a augmenté d’environ 18 à 20 points de pourcentage, et les lecteurs intermédiaires se sont également nettement améliorés, atteignant des performances proches de celles des experts. L’accord entre lecteurs, qui était auparavant seulement faible à modéré, est passé à des niveaux très élevés lorsqu’ils utilisaient l’outil. En revanche, l’étude note que cette forte convergence peut refléter un « biais d’automatisation », où les cliniciens s’appuient trop sur l’IA, en particulier pour les cas borderline les plus ambigus. Les auteurs insistent donc sur le fait que les cartes de chaleur sont des outils de recherche et non des explications autonomes, et que l’intégration de l’IA dans la formation clinique et la prise de décision doit être faite avec prudence.
Ce que cela signifie pour les patientes
En résumé, Clinical‑OMTA montre qu’un système d’IA entraîné sur des données échographiques diverses peut égaler la performance des experts pour classer les masses annexielles en catégories bénigne, borderline et maligne, tout en améliorant notablement les compétences et la cohérence des radiologues moins expérimentés. Parce qu’il fonctionne sur différents appareils et dans différents centres, le modèle pourrait éventuellement être intégré directement aux échographes ou utilisé comme logiciel autonome pour soutenir les médecins dans des cliniques surchargées ou sous‑équipées. Les auteurs mettent en garde qu’il faudra des études prospectives supplémentaires et des validations internationales avant un usage routinier, notamment dans des contextes avec du matériel d’entrée de gamme ou des opérateurs non spécialistes. Néanmoins, leur travail ouvre la voie vers un futur où davantage de femmes, quel que soit leur lieu de prise en charge, pourraient bénéficier d’une interprétation de niveau expert des échographies ovariennes et d’un soin plus personnalisé et plus rapide.
Citation: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Mots-clés: échographie ovarienne, intelligence artificielle, masses annexielles, tumeurs ovariennes borderline, support à la décision clinique