Clear Sky Science · fr
La délétion liée au chromosome Y du gène EIF1AY provoque des différences entre les sexes dans le myélome multiple
Pourquoi certains cancers du sang touchent davantage les hommes
Le myélome multiple est un cancer des cellules productrices d’anticorps dans la moelle osseuse. Dans le monde, les hommes développent et décèdent de cette maladie plus souvent que les femmes, mais les raisons en restent obscures. Cette étude explore un suspect surprenant : le chromosome Y. Les auteurs dévoilent comment la perte d’un seul gène lié au Y, nommé EIF1AY, contribue à orienter l’environnement immunitaire chez l’homme vers un soutien de la croissance tumorale, révélant une cible potentielle pour des traitements plus précis.
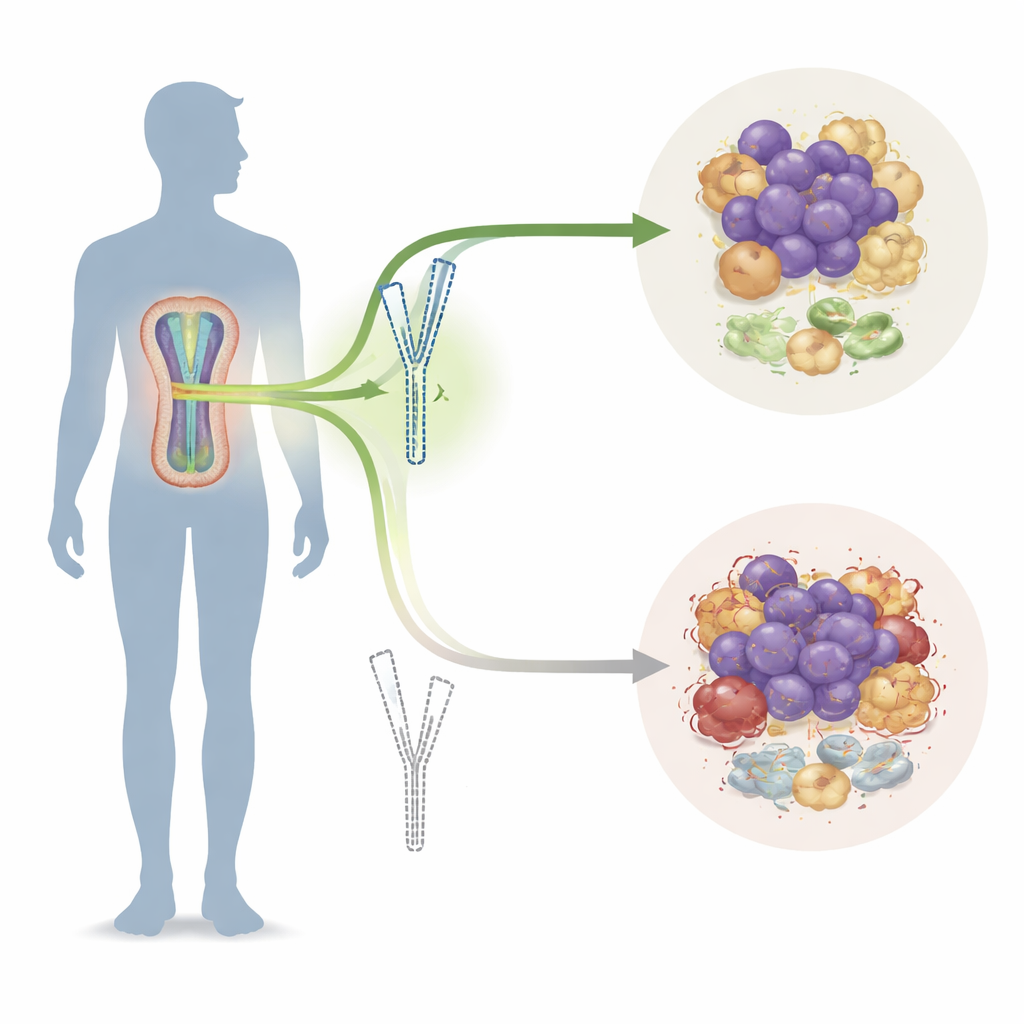
Un indice lié au sexe caché dans l’ADN tumoral
Les chercheurs ont d’abord confirmé que les hommes atteints de myélome multiple ont tendance à avoir un pronostic plus mauvais que les femmes : incidence plus élevée, maladie plus avancée au diagnostic et survie plus courte. Ils ont ensuite exploré de larges bases de données génétiques et cliniques à la recherche de gènes différant entre patients masculins et féminins. Parmi de nombreux candidats, trois gènes liés au chromosome Y ressortaient comme étant plus faibles chez les hommes atteints de formes agressives de la maladie, EIF1AY apparaissant comme le meilleur prédicteur d’un mauvais pronostic. Dans des échantillons de sang et de moelle osseuse prélevés chez des patients masculins, EIF1AY était souvent partiellement délété du chromosome Y, en particulier chez les hommes âgés et chez ceux présentant un myélome avancé et des altérations chromosomiques complexes. Les patients présentant de faibles niveaux d’EIF1AY avaient une charge tumorale plus élevée et de moins bonnes réponses aux thérapies, faisant de ce gène un facteur protecteur majeur que certaines tumeurs parviennent à perdre.
Comment les cellules immunitaires peuvent devenir des alliées du cancer
L’équipe a ensuite cherché à savoir comment EIF1AY influence le microenvironnement tumoral, en particulier les macrophages : des cellules immunitaires pouvant soit attaquer le cancer (état « M1 »), soit le soutenir (état « M2 »). Les analyses des jeux de données de patients ont montré que les échantillons de myélome masculins étaient enrichis en macrophages de type M2 par rapport aux échantillons féminins. Dans des modèles de laboratoire, des cellules de myélome modifiées pour exprimer davantage d’EIF1AY croissaient plus lentement en culture et chez la souris. Les macrophages environnants étaient moins susceptibles d’adopter le programme M2 favorisant la tumeur et étaient moins recrutés dans les tumeurs. Lorsque EIF1AY était réduit ou perdu, l’effet inverse se produisait : davantage de macrophages polarisés en M2 s’accumulaient aux marges et à l’intérieur des masses tumorales, et ces macrophages conditionnés libéraient à leur tour des facteurs qui stimulaient la prolifération des cellules myélomateuses. En substance, EIF1AY agissait comme un frein à un partenariat délétère entre cellules cancéreuses et macrophages.
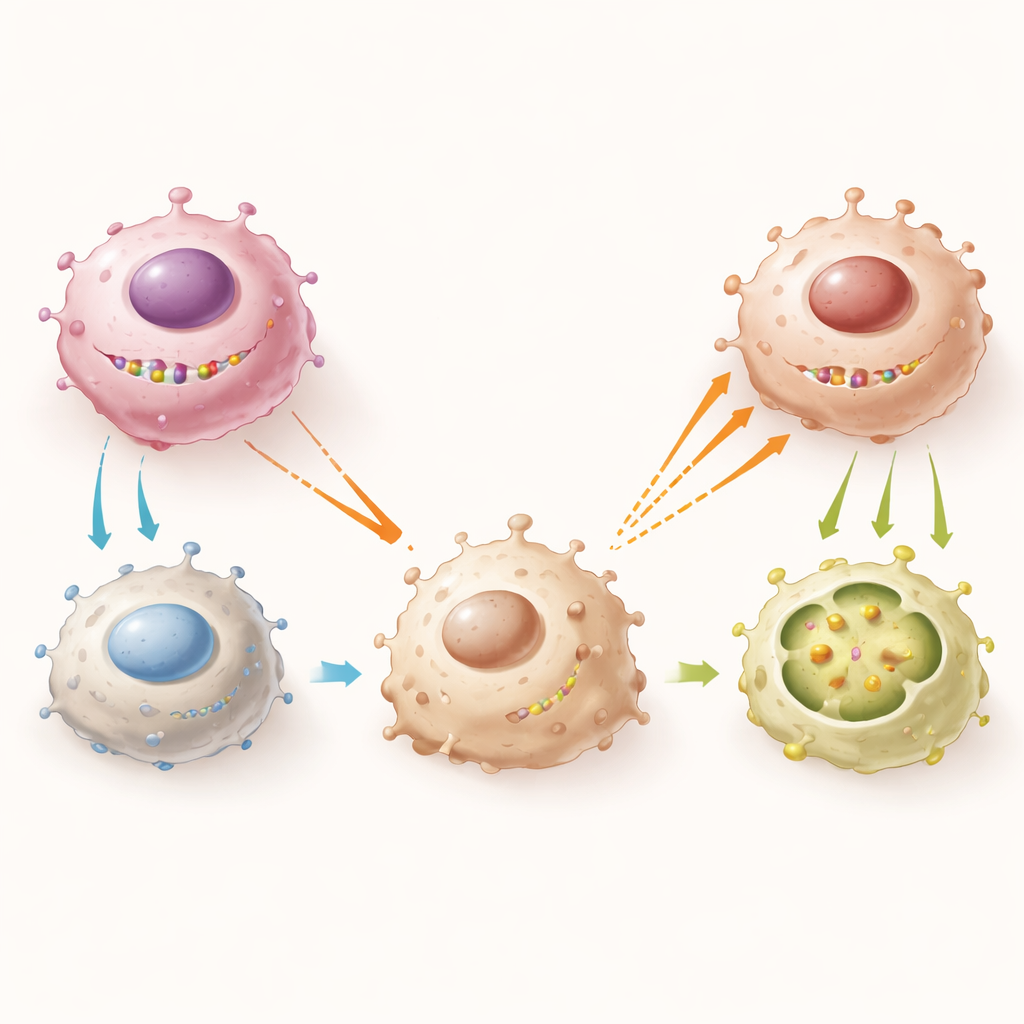
Une réaction en chaîne moléculaire de la cellule tumorale au macrophage
En approfondissant, les auteurs ont cartographié la chaîne moléculaire reliant un gène du chromosome Y à l’intérieur d’une cellule tumorale au comportement des cellules immunitaires voisines. EIF1AY s’associe à une autre protéine liée au Y, RPS4Y1, pour former un complexe qui se lie physiquement et stabilise l’ARNm d’un récepteur de surface nommé CD134 sur les cellules de myélome. Lorsque EIF1AY et RPS4Y1 sont présents, CD134 est maintenu à des niveaux plus élevés. Cela empêche les cellules tumorales de libérer de fortes quantités de deux protéines de signalisation, IL‑4 et IL‑13. Des niveaux faibles d’IL‑4 et d’IL‑13 signifient que les macrophages expriment moins d’un récepteur détectant le collagène appelé DDR1, sont moins enclins à devenir de type M2 et sont moins attirés vers la tumeur. Lorsque EIF1AY est délété, tout cet axe s’effondre : les niveaux de CD134 chutent, IL‑4 et IL‑13 augmentent, DDR1 augmente sur les macrophages et davantage de macrophages M2 affluent pour nourrir la tumeur.
Mise en relation des versions masculines et féminines d’un même dispositif de protection
Fait intéressant, les femmes ne portent pas EIF1AY ni RPS4Y1, mais elles possèdent des gènes étroitement liés sur le chromosome X, EIF1AX et RPS4X. L’étude a montré que des niveaux élevés de ces homologues liés au X chez les patientes atteintes de myélome étaient également associés à de meilleurs résultats. Lorsque les chercheurs ont réduit expérimentalement EIF1AX ou RPS4X dans des lignées de myélome d’origine féminine, les cellules proliféraient plus rapidement, reproduisant ce qui se passe chez les hommes lorsque EIF1AY et RPS4Y1 sont perdus. Cela suggère que les deux sexes disposent d’une voie protectrice similaire, mais que les hommes sont particulièrement vulnérables parce que le chromosome Y peut être partiellement perdu dans les cellules sanguines vieillissantes, supprimant EIF1AY et RPS4Y1, alors que les gènes liés au X chez les femmes sont plus stablement maintenus.
Ce que cela implique pour les patients et les traitements futurs
Concrètement, ce travail montre que de nombreux patients masculins atteints de myélome perdent un circuit protecteur qui commande normalement aux cellules tumorales de se tenir à l’écart et empêche les macrophages voisins de devenir des complices du cancer. Lorsque la voie EIF1AY–RPS4Y1–CD134 est intacte, elle maintient certains signaux immunitaires à faible niveau, prévient l’adoption d’une identité favorable à la tumeur par les macrophages et ralentit la croissance du myélome. Lorsque des parties du chromosome Y — et en particulier EIF1AY — sont délétées, ce frein est levé, permettant une boucle auto‑entretenue de signaux inflammatoires et de macrophages protecteurs qui accélère la maladie. Ces résultats contribuent à expliquer pourquoi les hommes ont un pronostic moins favorable que les femmes dans le myélome multiple et suggèrent que l’évaluation du statut d’EIF1AY, ou la restauration de sa voie d’action en aval, pourrait orienter des immunothérapies plus personnalisées pour les patients masculins.
Citation: Feng, Z., Bai, J., Li, Y. et al. Y chromosome-linked EIF1AY deletion drives sex differences in multiple myeloma. npj Precis. Onc. 10, 131 (2026). https://doi.org/10.1038/s41698-026-01317-0
Mots-clés: myélome multiple, chromosome Y, microenvironnement tumoral, polarisation des macrophages, différences sexuelles dans le cancer