Clear Sky Science · fr
Généralisation de la segmentation automatique des tumeurs dans les lames entières histopathologiques à travers plusieurs types de cancer
Pourquoi c’est important pour la prise en charge du cancer
Le diagnostic du cancer repose encore sur l’examen attentif par des experts de lames de verre de tissus colorés au microscope — une tâche longue, rendue plus difficile par l’augmentation du nombre de cas et la pénurie de pathologistes. Cette étude pose une question simple mais puissante : un seul système d’intelligence artificielle peut‑il repérer de manière fiable les zones cancéreuses dans des images microscopiques numériques pour de nombreux types de tumeurs, au lieu de développer un outil distinct pour chaque cancer ? Si la réponse est oui, cela pourrait alléger la charge de travail, accélérer le diagnostic et étendre les analyses avancées même aux cancers plus rares quand les données font défaut.
Des lames de verre aux assistants numériques
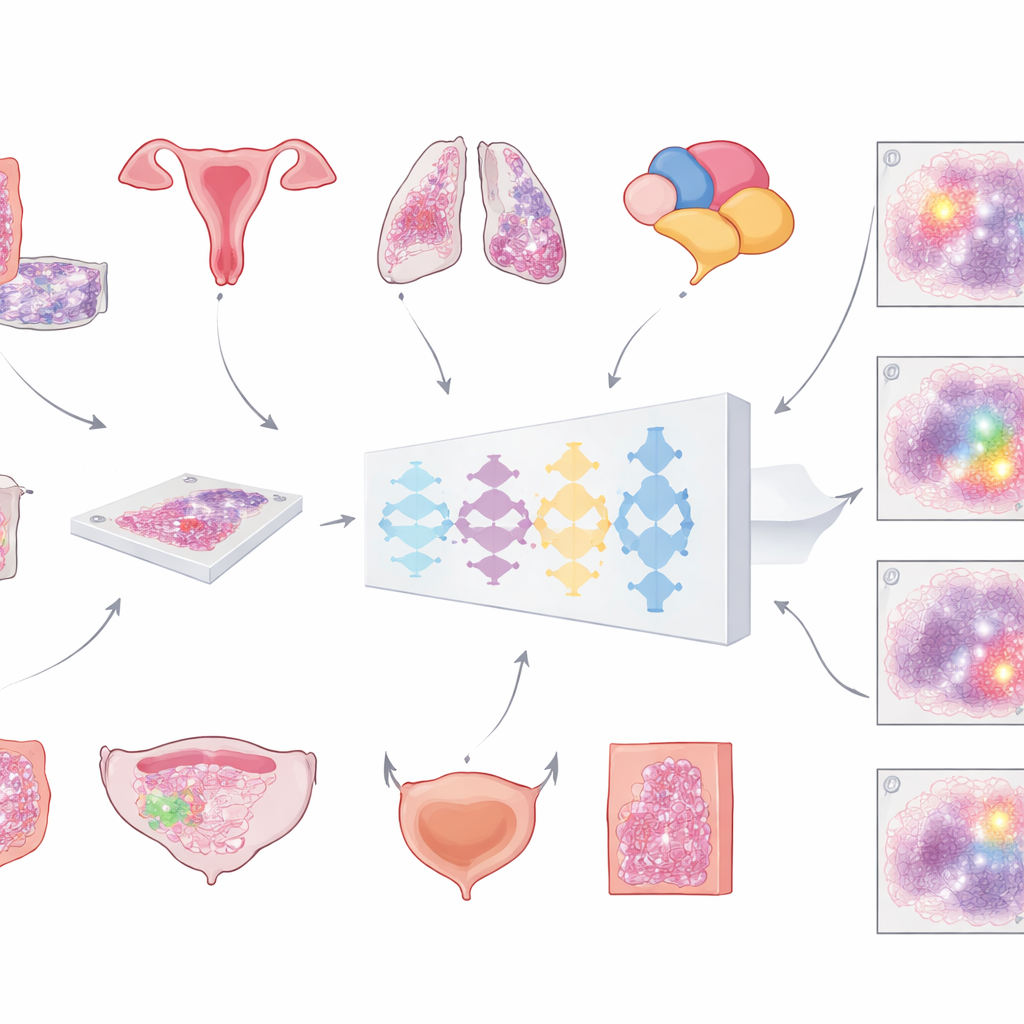
Les hôpitaux modernes numérisent de plus en plus les lames de microscope pour créer d’immenses images détaillées « de lames entières » des tumeurs. La première étape cruciale pour toute analyse assistée par ordinateur consiste à séparer le tissu tumoral de tout le reste — cellules normales, graisse, verre vide et artefacts. Jusqu’à présent, la plupart des outils automatisés ont été entraînés sur un seul type de cancer, ce qui limite leur champ d’application. L’équipe à l’origine de ce travail s’est donnée pour objectif de construire un modèle unique et universel capable de repérer les régions tumorales dans plusieurs cancers courants sur des lames colorées avec les colorants usuels hématoxyline‑éosine. Leur ambition était un outil général pouvant s’intégrer à de nombreux flux de travail diagnostiques sans le repenser à chaque fois.
Entraîner un modèle pour reconnaître plusieurs cancers
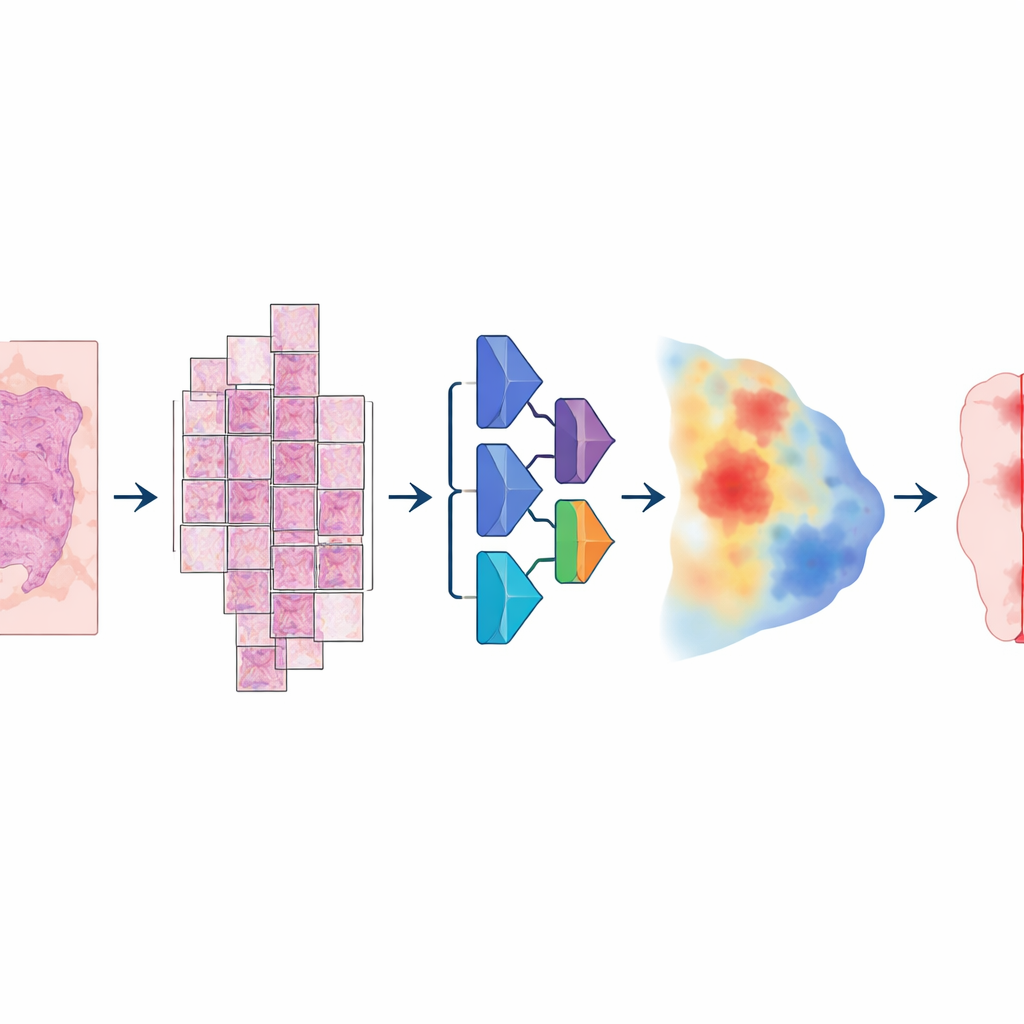
Pour construire ce modèle, les chercheurs ont rassemblé une collection exceptionnellement grande et variée d’images de lames numériques : plus de 20 000 images de lames entières provenant de plus de 4 000 patients atteints de cancers colorectal, endométrial, pulmonaire et de la prostate. Tous les échantillons provenaient de tissus fixés au formol et inclus en paraffine et ont été numérisés sur deux scanners haute résolution différents. Un pathologiste a soigneusement tracé les zones tumorales sur chaque lame, fournissant la « vérité de terrain » dont l’ordinateur s’est servi pour apprendre. Le modèle suivait une chaîne de traitement en plusieurs étapes : chaque image immense était découpée en larges tuiles chevauchantes, passée dans un réseau neuronal profond qui estimait, pour chaque pixel, la probabilité d’être tumoral, puis réassemblée en une carte lisse finalement convertie en un masque net tumeur contre non‑tumeur.
Mettre le système à l’épreuve
De manière cruciale, l’équipe ne s’est pas arrêtée aux performances d’entraînement. Ils ont testé le même modèle sur plus de 3 000 patients supplémentaires répartis sur six types de cancer — y compris des cancers du sein et de la vessie jamais utilisés pendant l’entraînement — et sur des lames provenant de plusieurs hôpitaux et scanners. La précision a été mesurée principalement avec un score d’overlap standard (le coefficient de Dice), qui atteint 100 % lorsque le contour tumoral de l’ordinateur correspond parfaitement à celui du pathologiste. Pour de grands échantillons tumoraux intacts dans les cancers colorectal, endométrial, pulmonaire, de la prostate et du sein, le recouvrement moyen dépassait 80 % et atteignait souvent 90 % ou plus. Dans de grandes collections externes issues de The Cancer Genome Atlas, rassemblant des laboratoires et scanners du monde entier, les performances sont restées au‑dessus de 80 %, suggérant que le modèle se généralise bien au‑delà de son institution d’origine.
Où il montre ses limites et comment il se compare
La principale faiblesse est apparue dans les cancers de la vessie de stade précoce prélevés par une procédure qui produit de petites fragments tissulaires. Dans ces cas, le modèle n’a souvent marqué aucune tumeur, surtout lorsque la zone cancéreuse était très petite. Pourtant, lorsqu’il détectait une tumeur, le recouvrement avec les contours du pathologiste était élevé, et de simples ajustements des seuils finaux amélioraient les résultats — ce qui laisse entendre que le réseau sous‑jacent reconnaissait le motif mais que le post‑traitement était trop strict. Les chercheurs ont aussi entraîné quatre modèles « spécialistes », chacun sur un seul type de cancer, et ont constaté qu’aucun ne surpassait de manière significative le modèle général dans son domaine propre. En revanche, ces systèmes spécialisés échouaient largement lorsqu’ils étaient appliqués à d’autres types de cancer, tandis que le modèle général restait robuste. Comparé à un outil de segmentation médicale générique populaire nécessitant des indications de l’utilisateur, le nouveau modèle a généralement obtenu des performances équivalentes ou supérieures tout en restant entièrement automatique.
Ce que cela signifie pour les patients et les médecins
Pour les non‑spécialistes, la conclusion principale est qu’un système d’IA bien conçu peut mettre en évidence de manière fiable le tissu cancéreux sur des lames numériques pour plusieurs grands types de tumeurs, sans nécessiter de versions personnalisées pour chaque maladie ou scanner. Il ne remplace pas le pathologiste, mais il peut pré‑marquer les régions susceptibles d’être tumorales, soutenir des mesures cohérentes et permettre aux spécialistes de se concentrer sur les cas les plus complexes. La version actuelle manque encore certains très petits cancers ou cancers de stade précoce — en particulier les échantillons vésicaux fragmentés et probablement d’autres tissus de type biopsie — elle n’est donc pas encore adaptée à la détection des traces les plus faibles de cancer. Néanmoins, l’étude montre que la segmentation tumorale large, « pan‑cancer », est réalisable en conditions réelles et peut constituer une première étape robuste pour de futurs outils automatisés évaluant le grade tumoral, prédisant la réponse au traitement ou guidant des thérapies de précision.
Citation: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
Mots-clés: pathologie numérique, apprentissage profond, segmentation des tumeurs, imagerie de lames entières, modèle pan‑cancer