Clear Sky Science · fr
Analyse unicellulaire à grande échelle et perturbation in silico révèlent l’évolution dynamique du CHC : de l’initiation au ciblage thérapeutique
Pourquoi la vie interne du foie cancéreux compte
Le carcinome hépatocellulaire, la forme la plus fréquente de cancer du foie, est notoirement difficile à traiter. De nombreux patients ne répondent pas bien aux traitements actuels, et les tumeurs récidivent ou se disséminent souvent. Une grande raison est que chaque tumeur est un mélange chaotique de cellules différentes qui évoluent au fil du temps et dialoguent en permanence avec leur environnement. Cette étude utilise des technologies puissantes de lecture des gènes au niveau unicellulaire et spatial pour observer cette évolution, cellule par cellule, depuis la croissance tumorale précoce jusqu’à la maladie avancée résistante aux traitements, et pour identifier des points faibles que de nouvelles thérapies pourraient exploiter.
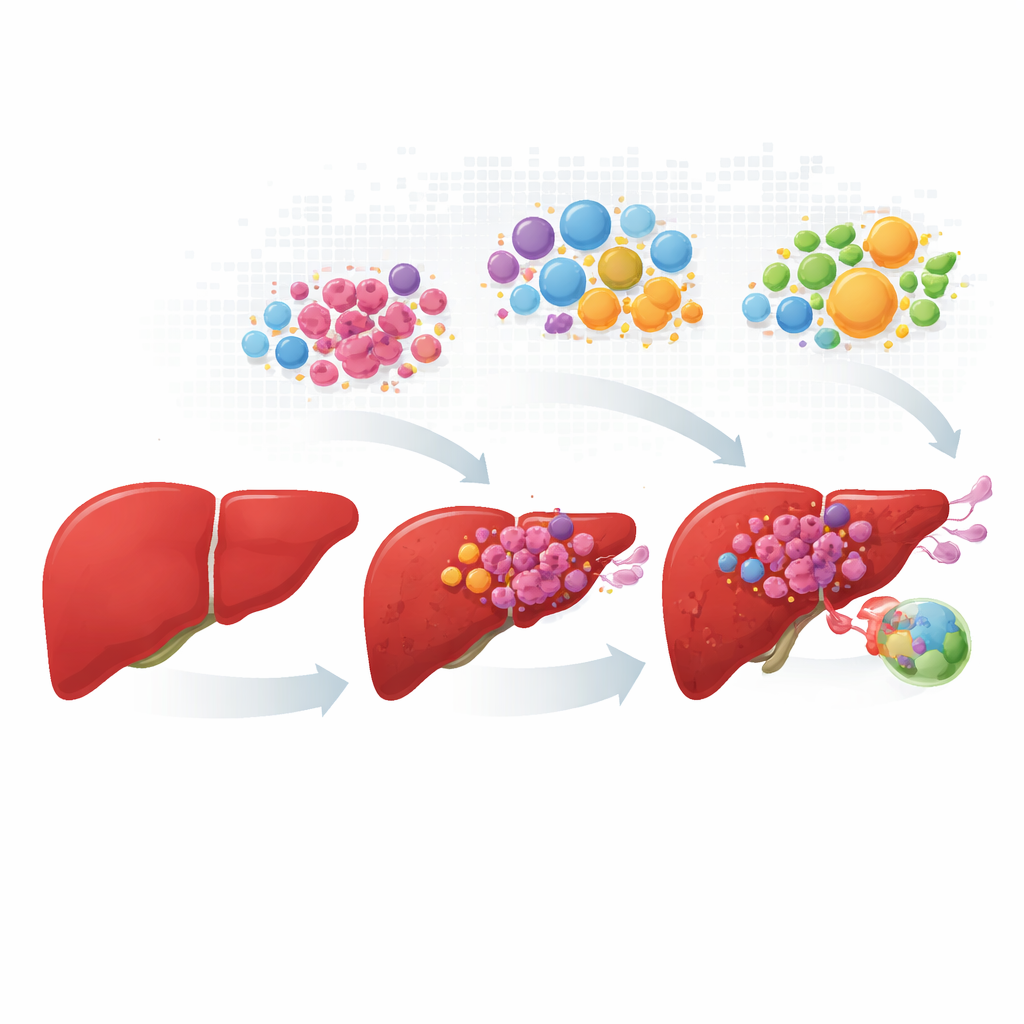
Suivre les cellules cancéreuses depuis les premiers changements jusqu’à la dissémination
Les chercheurs ont rassemblé et harmonisé des données de plus d’une centaine de patients, couvrant le foie normal, les tumeurs primaires, les lésions dans les vaisseaux sanguins et les métastases ganglionnaires. Plutôt que de considérer chaque tumeur comme une masse uniforme, ils ont profilé des centaines de milliers de cellules individuelles, puis cartographié la position de ces cellules dans de véritables coupes tissulaires. Les cellules hépatiques cancéreuses se répartissaient en quatre « personnalités » récurrentes. Un groupe conservait de nombreuses fonctions hépatiques normales et tâches métaboliques ; les trois autres présentaient une croissance induite par le stress, une forte activité de la voie de croissance MYC, ou un comportement invasif lié à l’inflammation. Ces quatre états apparaissaient en proportions variables au fur et à mesure de la progression de la maladie, avec une prédominance des cellules à forte prolifération et invasives dans les lésions vasculaires et ganglionnaires.
Quatre personnalités tumorales aux destins différents
Ces quatre états des cellules cancéreuses n’étaient pas de simples catégories théoriques : ils se corrélaient avec le pronostic des patients. Les tumeurs riches en l’état de type hépatique, métaboliquement actif, étaient associées à une meilleure survie, tandis que celles dominées par les trois états agressifs avaient tendance à de moins bons résultats. Pourtant, même l’état « favorable » présentait une particularité : il était fortement enrichi chez les patients qui ne bénéficiaient pas du sorafénib, médicament contre le cancer du foie, probablement parce que ces cellules conservent des mécanismes de détoxification capables d’inactiver les médicaments. En reconstituant les trajectoires de développement cellulaire, l’équipe a montré que les cellules invasives et inflammatoires pouvaient bifurquer vers des états plus différenciés ou vers des états à haute prolifération, suggérant que les cellules tumorales peuvent changer d’identité et échapper potentiellement à des thérapies ciblant un seul état.
La troupe d’appoint : complices immunitaires et stromaux
Les cellules tumorales n’agissent pas seules. L’étude a mis en évidence des cellules immunitaires spécialisées et des cellules de soutien qui combattent les tumeurs ou, silencieusement, les favorisent. Parmi les macrophages, les éboueurs et sentinelles du tissu, certains types produisaient des signaux inflammatoires pouvant soutenir l’immunité anti‑tumorale, tandis que d’autres étaient métaboliquement réorientés, supprimaient les signaux bénéfiques et favorisaient l’angiogenèse et l’invasion. Ces macrophages « mauvais acteurs » se sont étendus dans les échantillons avancés. De même, certains types d’endothéliales (revêtement des vaisseaux) et de fibroblastes (constructeurs de la matrice) formaient des sous‑ensembles distincts associés à un mauvais pronostic. Dans la maladie avancée, une sous‑population endothéliale particulière et deux types de fibroblastes formaient des hubs étroitement connectés qui remodelaient le réseau extracellulaire, alimentaient la néoangiogenèse et se corrélaient avec les états cellulaires tumoraux les plus agressifs.
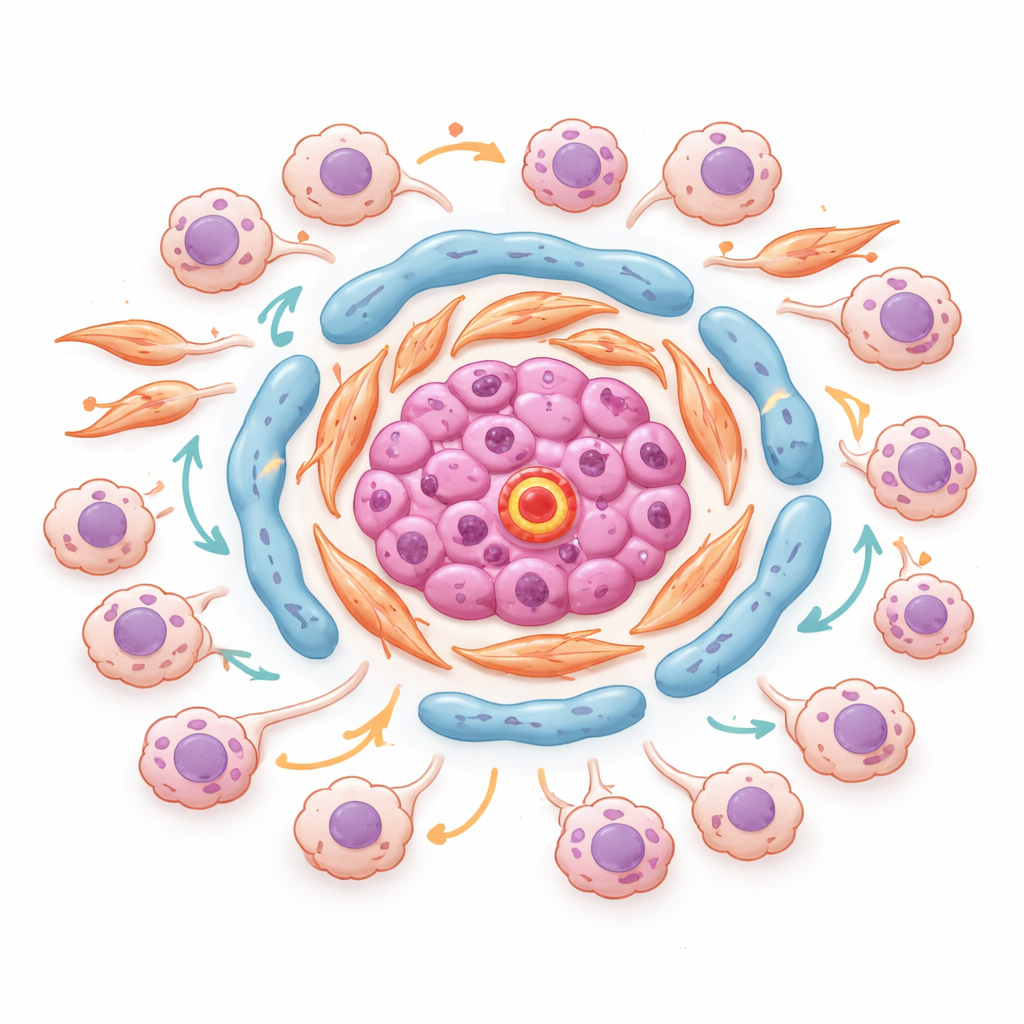
Repérer les quartiers dangereux à l’intérieur des tumeurs
Grâce à la transcriptomique spatiale, qui mesure l’activité génique sans perdre la carte des emplacements tissulaires, les auteurs ont identifié des « quartiers » organisés à l’intérieur des tumeurs. Dans une tumeur représentative, des cellules endothéliales riches en une molécule appelée ESM1 se regroupaient avec des fibroblastes avides de lipides et producteurs de matrice au cœur d’îlots stromaux. Autour de ces noyaux s’accumulaient des cellules tumorales induites par le stress et invasives, dans des régions marquées par une forte activité de la voie TGF‑bêta et des signaux d’hypoxie. Des facteurs de transcription clés qui régulent la réponse au stress et à l’inflammation étaient partagés entre ces états tumoraux et étaient les plus actifs précisément là où les cellules tumorales touchaient ces hubs stromaux. Cela suggère que des micro‑niches spécifiques aux frontières tumeur–stroma encouragent activement la transition des cellules vers des états plus agressifs et résistants aux traitements.
Identifier une faiblesse commune pour de nouveaux traitements
Pour passer de la description à l’intervention, l’équipe a utilisé un modèle d’apprentissage automatique entraîné sur des millions de cellules pour simuler des « knockouts virtuels » de gènes et prédire quels changements pourraient ramener les cellules nocives vers des états plus sains. En comparant macrophages, cellules endothéliales et cellules cancéreuses, ils ont trouvé un petit ensemble de gènes dont l’inhibition aidait à normaliser les trois types. Parmi eux, HSP90B1 s’est distingué : les lignées cellulaires cancéreuses en dépendent fortement, il est surexprimé dans les tumeurs hépatiques, particulièrement dans celles résistantes aux thérapies ciblées et à l’immunothérapie, et des niveaux élevés prédisent une survie plus faible. HSP90B1 code pour une chaperonne gérant le stress dans l’usine de pliage des protéines cellulaires, soutenant de nombreux récepteurs de surface et voies de signalisation. Comme des inhibiteurs sélectifs de cette chaperonne existent déjà et peuvent aussi remodeler l’environnement immunitaire, l’étude propose HSP90B1 comme une cible prometteuse pour surmonter la résistance, notamment en combinaison avec les traitements actuels du cancer du foie.
Ce que cela signifie pour les patients et les thérapies
Dans l’ensemble, ce travail montre que le cancer du foie n’est pas une seule maladie mais un écosystème dynamique d’états cellulaires et de micro‑niches qui évoluent au fur et à mesure de la croissance et de la dissémination tumorales. En reliant des personnalités cellulaires tumorales spécifiques, des cellules de soutien et des quartiers spatiaux au pronostic et à la réponse aux médicaments, l’étude offre une feuille de route pour des traitements plus précis : adapter les thérapies aux états cellulaires dominants, perturber les hubs stromaux qui cultivent des comportements agressifs, et cibler des dépendances partagées comme HSP90B1 sur lesquelles reposent de nombreuses cellules tumorales et du microenvironnement. Bien que des tests complémentaires en laboratoire et en clinique soient nécessaires, l’atlas construit par l’équipe fournit un plan détaillé pour transformer la complexité interne de la tumeur d’un obstacle en une opportunité pour des thérapies du cancer du foie plus intelligentes et plus durables.
Citation: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Mots-clés: carcinome hépatocellulaire, analyse unicellulaire, microenvironnement tumoral, transcriptomique spatiale, HSP90B1