Clear Sky Science · fr
Traduction des signatures de transcriptomique spatiale dans le carcinome adénosquameux en biomarqueurs pronostiques en masse dans l’adénocarcinome pulmonaire : une approche ascendante
Signaux d’alerte cachés à l’intérieur des tumeurs pulmonaires
Le cancer du poumon reste l’un des cancers les plus meurtriers, en partie parce que les tumeurs sont des mélanges de nombreux types de cellules. Certaines de ces cellules peuvent discrètement pousser la maladie à devenir plus agressive ou à résister aux traitements, mais elles sont trop rares ou trop intégrées pour être détectées par les tests de laboratoire classiques. Cette étude montre comment des « cartes » ultra-détaillées de l’activité génique à l’intérieur des tumeurs peuvent révéler ces fauteurs de trouble cachés et les transformer en marqueurs simples utilisables en laboratoire pour mieux prédire le pronostic des patients atteints de cancer du poumon.
Examiner de plus près une tumeur rare et mixte
Les chercheurs se sont concentrés sur un cancer pulmonaire rare appelé carcinome adénosquameux, qui combine deux types principaux de cancer bronchique non à petites cellules dans une même masse : l’adénocarcinome aux formes glandulaires et le carcinome squameux aux cellules plus plates et proches de l’épiderme. Parce que ces deux composantes coexistent côte à côte dans la même tumeur, ce cancer est un modèle idéal pour étudier comment les cellules tumorales peuvent basculer d’une identité à l’autre en devenant plus malignes. À l’aide d’une méthode d’imagerie appelée transcriptomique spatiale, l’équipe a mesuré quels gènes étaient activés dans des milliers de cellules individuelles tout en préservant leur position exacte dans des coupes fines de tissu tumoral. Parallèlement, ils ont utilisé des colorations diagnostiques classiques pour deux marqueurs courants, TTF‑1 (pour l’adénocarcinome) et p40 (pour les cellules squameuses), afin d’ancrer leurs cartes haute technologie dans la pratique pathologique de routine. 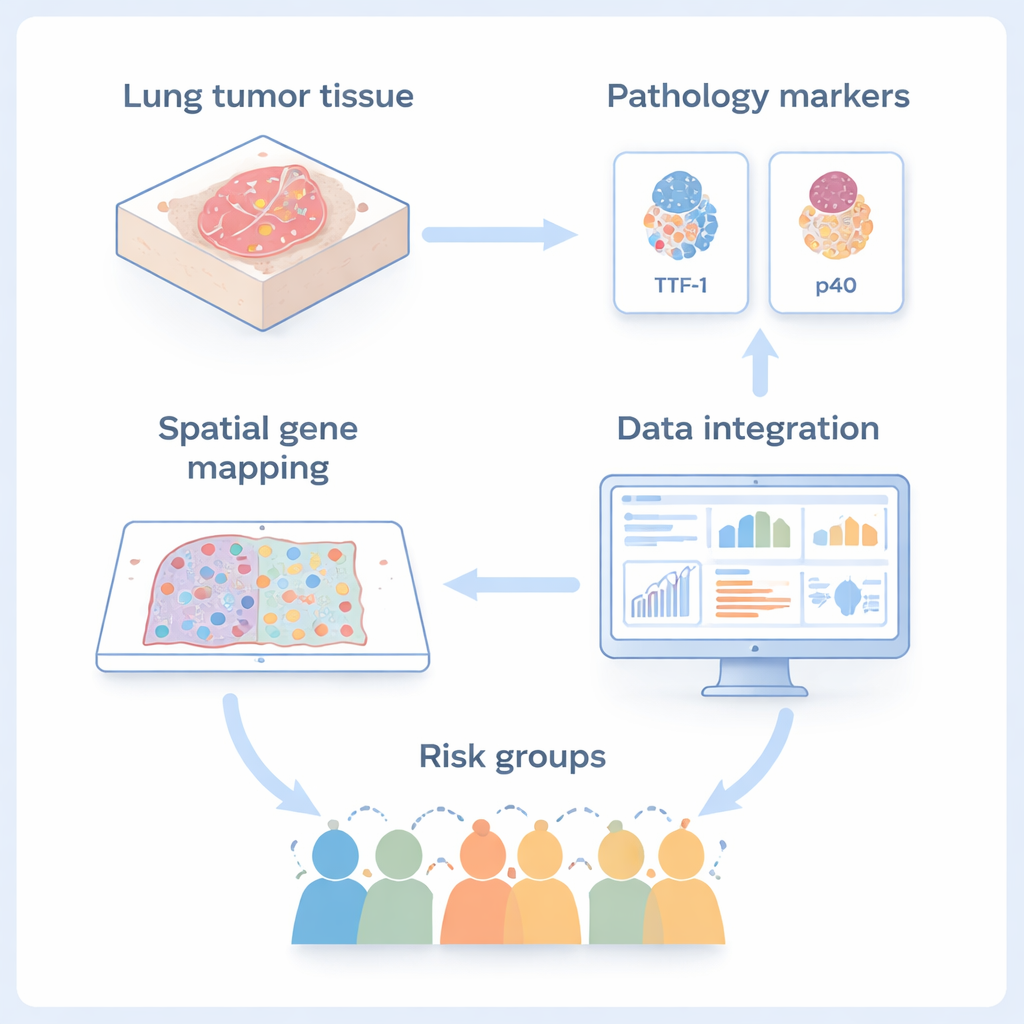
Coder les cellules tumorales par couleur pour repérer les éléments atypiques
Grouper simplement les cellules selon leurs profils géniques ne suffisait pas, car les cellules pulmonaires normales et les cellules tumorales peuvent parfois présenter des lectures géniques similaires. Pour affiner leur vision, l’équipe a utilisé une astuce de visualisation qu’ils appellent RGB‑UMAP. Dans cette approche, le profil global d’activité génique de chaque cellule est compressé en trois nombres puis traduit en une couleur rouge‑vert‑bleu. Les cellules qui se comportent de manière semblable apparaissent dans des couleurs proches lorsqu’elles sont projetées à nouveau sur l’image tissulaire. Cela a permis aux scientifiques de repérer des poches de cellules normales dissimulées parmi les cellules tumorales et de les exclure de leur analyse, garantissant ainsi qu’ils étudiaient de véritables cellules cancéreuses plutôt que des cellules saines environnantes.
Découverte d’un état cellulaire hybride et d’un portail sucré clé
Après avoir filtré les cellules normales, les chercheurs ont cherché des gènes fortement et systématiquement actifs uniquement dans les cellules tumorales. Parmi ceux-ci, ils ont découvert un groupe de cellules tumorales qui étaient négatives pour TTF‑1 et p40 mais présentaient un profil génique mixte, partageant des caractéristiques de l’adénocarcinome et du carcinome squameux. Un gène s’est démarqué dans ce groupe hybride : SLC2A1, qui code pour une protéine connue sous le nom de GLUT1. GLUT1 fonctionne comme une porte laissant entrer le glucose, le carburant cellulaire, depuis le sang. Dans plusieurs tumeurs, SLC2A1 était abondant dans les zones squameuses et dans les zones négatives pour TTF‑1/p40, mais presque absent du tissu pulmonaire normal. L’équipe a confirmé ce schéma dans plusieurs échantillons de patients, suggérant que des taux élevés de SLC2A1 marquent une sous‑population de cellules tumorales d’allure squameuse et métaboliquement active.
Des cartes microscopiques aux résultats cliniques des patients
Pour vérifier si cette découverte microscopique a un impact chez de vrais patients, les scientifiques se sont tournés vers de grands jeux de données existants où l’expression génique en masse (moyennée sur des échantillons tumoraux entiers), les altérations d’ADN et les issues cliniques étaient disponibles pour des centaines de personnes atteintes d’adénocarcinome pulmonaire. Lorsqu’ils ont regroupé ces patients selon les niveaux de SLC2A1 dans leurs tumeurs, ceux présentant des niveaux plus élevés de SLC2A1 avaient davantage d’altérations géniques typiquement observées dans les cancers squameux, une signature plus marquée d’un métabolisme avide en glucose, et une survie significativement plus mauvaise. Ce lien persistait même en tenant compte de facteurs tels que l’âge, le stade, l’antécédent tabagique et le sexe, et il a été confirmé dans un jeu de données public indépendant. En revanche, dans les tumeurs purement squameuses, les niveaux de SLC2A1 n’ont pas clairement distingué les patients en termes de pronostic, ce qui souligne que ce marqueur est particulièrement informatif au sein des adénocarcinomes. 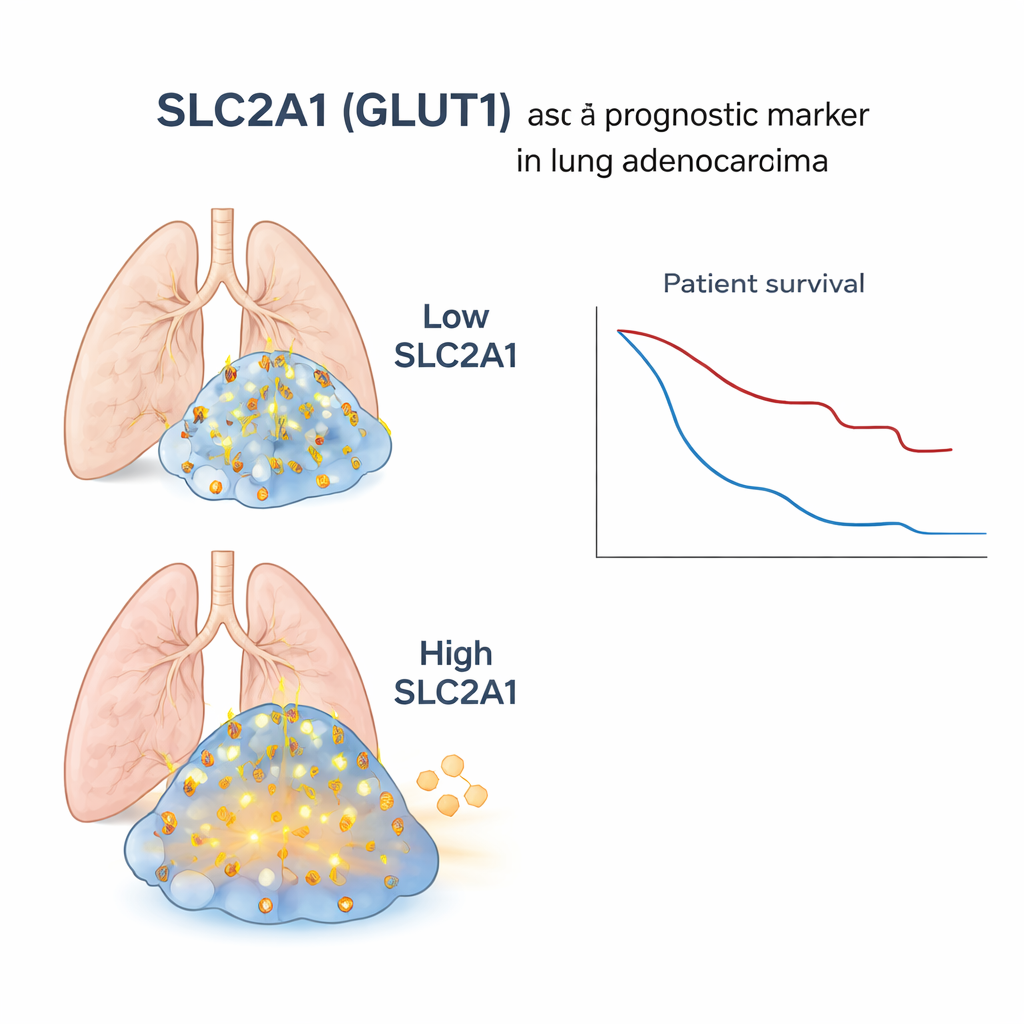
Ce que cela signifie pour les patients atteints d’adénocarcinome pulmonaire
Pour un non‑spécialiste, le message clé est que, au sein de ce qui ressemble à un seul type de cancer du poumon au microscope, il peut exister des poches cachées de cellules qui se comportent davantage comme un autre type, plus agressif. En utilisant une cartographie génique à haute résolution, les chercheurs ont identifié SLC2A1 comme un signe simple et mesurable de ces cellules d’allure squameuse, avide en carburant, nichées à l’intérieur des adénocarcinomes. Des niveaux élevés de ce gène dans des échantillons de tissu standard signalent des patients dont les tumeurs sont plus susceptibles d’être agressives et qui pourraient nécessiter un suivi plus étroit ou des stratégies thérapeutiques différentes. Plus largement, l’étude illustre une voie « ascendante » — de la cellule unique dans une coupe de tissu aux tests réalisables sur la tumeur entière — qui pourrait être appliquée à d’autres cancers pour révéler des états cellulaires dangereux que les méthodes de routine manquent actuellement.
Citation: Hatakeyama, K., Kawata, T., Muramatsu, K. et al. Translating spatial transcriptomic signatures in adenosquamous carcinoma into bulk prognostic biomarkers in lung adenocarcinoma: a bottom-up approach. npj Precis. Onc. 10, 77 (2026). https://doi.org/10.1038/s41698-026-01297-1
Mots-clés: adénocarcinome pulmonaire, transcriptomique spatiale, carcinome adénosquameux, SLC2A1 GLUT1, biomarqueurs du cancer