Clear Sky Science · fr
Profilage multimodal unicellulaire révèle un dialogue entre macrophages et cellules du stroma chez des patients atteints de cholangiocarcinome de mauvais pronostic
Le quartier caché du cancer
Le cholangiocarcinome, un cancer des voies biliaires du foie, est rare mais souvent mortel, et les options thérapeutiques efficaces sont limitées. De nombreux patients ne répondent pas aux médicaments d’immunothérapie modernes qui libèrent le système immunitaire contre les tumeurs. Cette étude pose une question simple mais cruciale : que se passe-t-il à l’intérieur du « quartier » tumoral qui empêche les cellules de défense de l’organisme de faire leur travail — et pourquoi certains patients évoluent-ils plus mal que d’autres ?
Pourquoi les cellules immunitaires restent bloquées à la porte
Plutôt que d’être un agglomérat lâche de cellules cancéreuses, le cholangiocarcinome est riche en tissu de soutien, appelé stroma, et en une variété de cellules immunitaires. En profilant des cellules individuelles issues des tumeurs, du tissu hépatique adjacent et du sang, les chercheurs montrent que le centre tumoral est pauvre en les mêmes lymphocytes T qui sont les plus efficaces pour tuer le cancer. Ces lymphocytes T dits « mémoire effecteurs » restent principalement dans le foie environnant plutôt que d’entrer dans la tumeur. En revanche, les lymphocytes T régulateurs — des cellules immunitaires qui font office de frein — s’accumulent à l’intérieur de la tumeur. Beaucoup des lymphocytes T qui parviennent à pénétrer affichent plusieurs « interrupteurs d’arrêt » à leur surface, signes qu’ils sont épuisés et incapables de combattre.
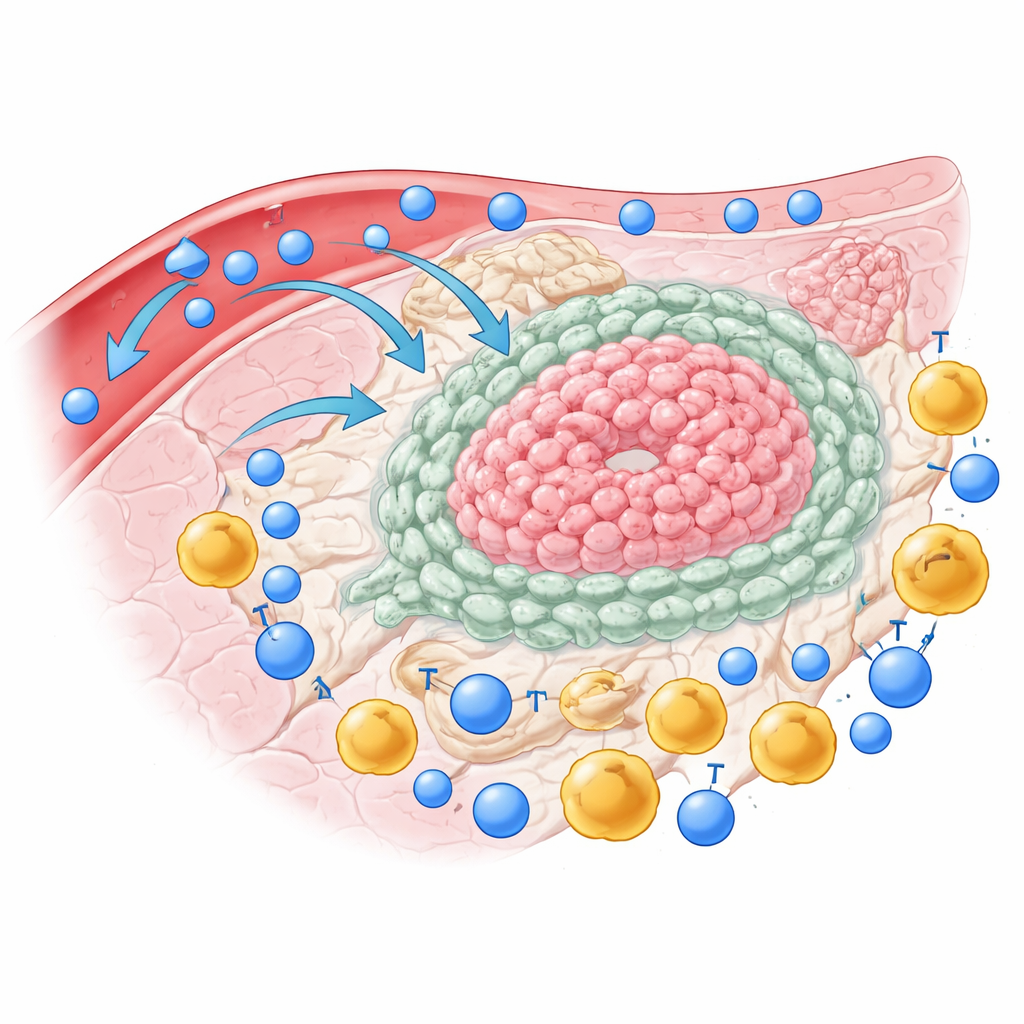
L’alliance suppressive de la tumeur
Pour aller au‑delà des lymphocytes T, l’équipe a cartographié des milliers de cellules individuelles provenant des tumeurs des patients au niveau de l’activité génique. Ils ont trouvé non seulement plusieurs variantes de cellules cancéreuses, mais aussi des groupes distincts de cellules de soutien, telles que des fibroblastes associés au cancer, des cellules étoilées hépatiques, des cellules endothéliales vasculaires et des macrophages — des cellules immunitaires qui peuvent soit attaquer soit aider les tumeurs. Chez les patients présentant des issues particulièrement défavorables, un sous‑ensemble particulier de cellules cancéreuses montrait une communication renforcée avec les cellules stromales et les macrophages. Plutôt que d’agir de façon indépendante, ces types cellulaires formaient un réseau serré qui semblait conçu pour empêcher les lymphocytes T attaquants d’entrer et pour les désactiver.
Signaux silencieux qui coupent les défenses
En analysant ces conversations, les scientifiques ont identifié des « poignées de mains » moléculaires clés échangées entre cellules. Les cellules cancéreuses produisaient de la versicane, une protéine matricielle adhésive qui interagit avec des capteurs sur les macrophages et des récepteurs de croissance sur les cellules stromales, remodelant le tissu de manière à favoriser la croissance tumorale et à atténuer l’attaque immunitaire. Les macrophages produisaient du TGF‑bêta, un signal puissant connu pour générer davantage de lymphocytes T régulateurs et affaiblir les lymphocytes T cytotoxiques. Une autre voie impliquait le ligand GAS6 se liant au récepteur AXL sur les macrophages, les fibroblastes et les cellules cancéreuses, une combinaison associée dans d’autres cancers à un comportement agressif et à l’évasion immunitaire. Ensemble, ces signaux créent une boucle de rétroaction : le stroma et les macrophages remodèlent l’environnement, renforcent les freins immunitaires et aident les cellules cancéreuses à prospérer.
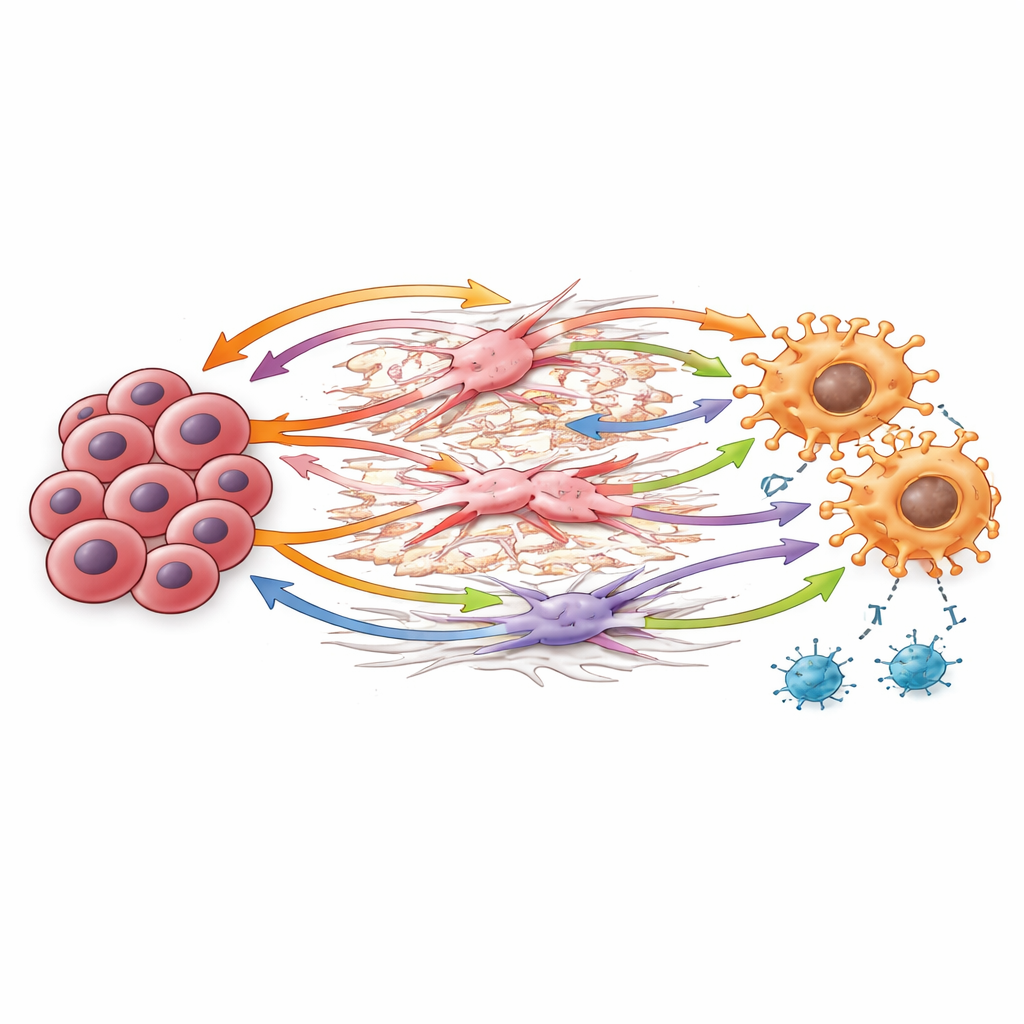
Un schéma qui va au‑delà d’un petit groupe
Bien que le travail unicellulaire ait été réalisé sur un nombre modeste de patients, l’équipe a vérifié ses observations par rapport à un jeu de données public beaucoup plus large de prélèvements de cholangiocarcinome extra‑hépatique. En estimant mathématiquement quels types cellulaires étaient présents dans chaque tumeur, ils ont découvert un groupe notable de patients dont les tumeurs étaient riches en cellules stromales et en macrophages et exprimaient des niveaux élevés des mêmes molécules clés — versicane, GAS6, AXL et le récepteur de croissance EGFR. Cela suggère que le réseau suppressif mis au jour dans la petite étude n’est pas une curiosité rare mais pourrait définir un sous‑groupe cliniquement important de patients avec une biologie tumorale particulièrement agressive.
Ce que cela implique pour les traitements futurs
Pour les personnes atteintes de cholangiocarcinome, ces résultats contribuent à expliquer pourquoi les inhibiteurs de point de contrôle immunitaire standards échouent souvent : le problème n’est pas seulement un frein unique sur les lymphocytes T, mais un véritable quartier de cellules collaborant pour maintenir le système immunitaire en échec. L’étude met en lumière plusieurs voies de signalisation — telles que les axes GAS6–AXL, versicane–TLR2 et TGF‑bêta–EGFR — qui pourraient être ciblées en association avec les inhibiteurs de point de contrôle pour affaiblir le bouclier protecteur tumoral. Elle souligne également la nécessité de tests qui examinent non seulement les cellules tumorales mais aussi le tissu hépatique environnant pour vérifier si des lymphocytes T agressifs sont présents mais empêchés d’entrer. À long terme, le décodage de cette communication cellulaire complexe pourrait conduire à des méthodes plus précises pour sélectionner les patients pour l’immunothérapie et pour concevoir des traitements combinés donnant à leur système immunitaire une réelle chance de contre‑attaquer.
Citation: Heij, L., Hayat, S., Reichel, K. et al. Multimodal single-cell profiling reveals crosstalk between macrophages and stromal cells in poor prognostic cholangiocarcinoma patients. npj Precis. Onc. 10, 105 (2026). https://doi.org/10.1038/s41698-026-01292-6
Mots-clés: cholangiocarcinome, microenvironnement tumoral, profilage unicellulaire, épuisement immunitaire, macrophages associés aux tumeurs