Clear Sky Science · fr
La progression métastatique du phéochromocytome et du paragangliome se produit par évolution parallèle
Pourquoi ces tumeurs rares sont importantes
Les phéochromocytomes et les paragangliomes sont des tumeurs rares issues de cellules nerveuses productrices d’hormones situées en profondeur dans l’organisme. Elles peuvent provoquer des pics sévères de tension artérielle et d’autres symptômes dangereux, souvent chez des adultes relativement jeunes. Jusqu’à un quart des patients développent finalement une dissémination vers des organes distants, alors que les options médicamenteuses efficaces sont limitées. Cette étude pose une question simple mais cruciale : comment et quand ces tumeurs deviennent‑elles métastatiques — et leur ADN pourrait‑il révéler de nouvelles voies thérapeutiques ?
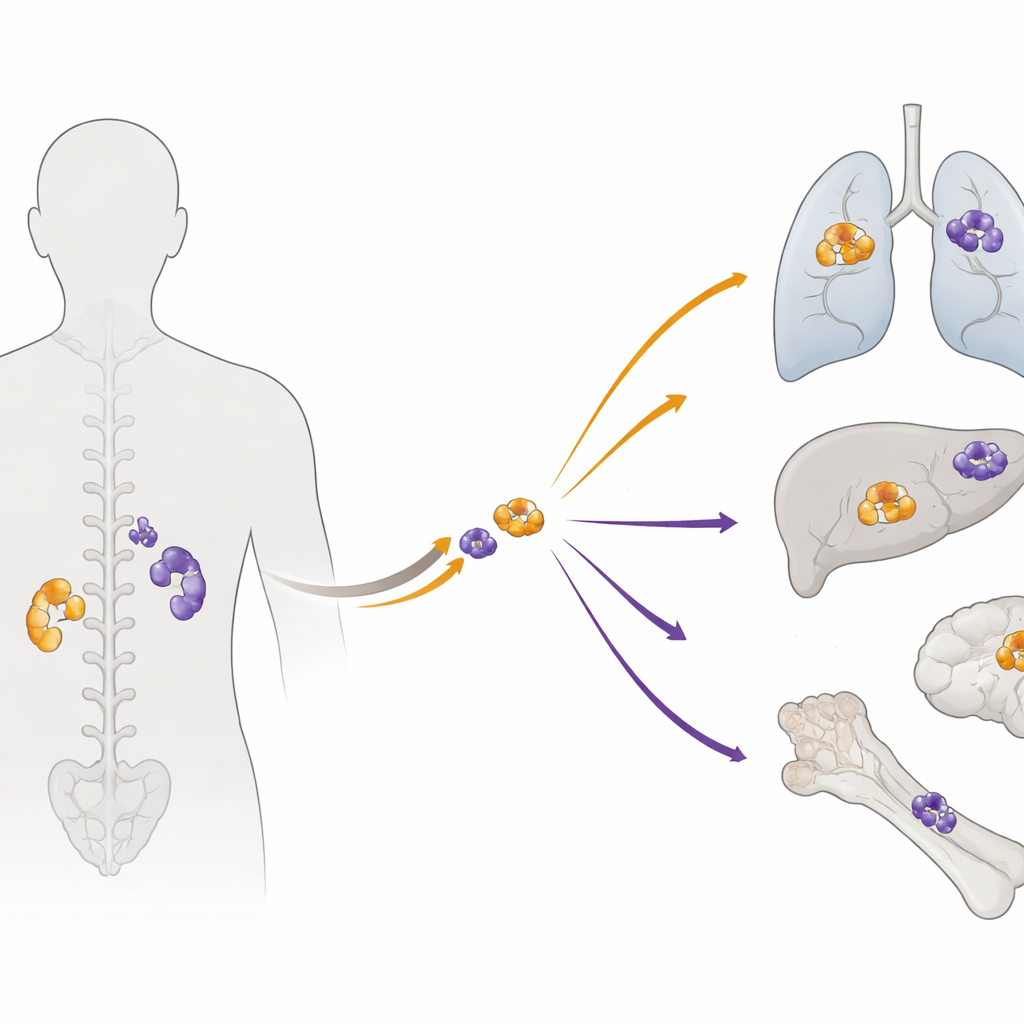
Sur la piste de l’ADN du cancer
Les chercheurs ont analysé des échantillons tumoraux appariés provenant de 27 personnes dont la maladie s’était déjà propagée. Pour de nombreux patients, ils disposaient de l’ADN à la fois de la tumeur primaire et de ses métastases ultérieures, ainsi que de tissus normaux en comparaison. En utilisant le séquençage de l’exome entier — une technique qui lit tous les gènes codant pour des protéines — ils ont catalogué des milliers de mutations et des gains et pertes d’ADN de plus grande échelle. Ils ont ensuite appliqué des outils statistiques pour distinguer les altérations probablement « conductrices » qui font progresser le cancer du bruit de fond, et pour reconstruire l’ordre dans lequel les événements génétiques clés sont survenus.
Failles cachées dans les défenses tumorales
Un des schémas frappants était la fréquence élevée des atteintes dans des gènes qui aident à empaqueter l’ADN et à le réparer lorsqu’il se casse. Près de 40 % des tumeurs présentaient des altérations délétères dans des gènes de remodelage de la chromatine ou de réparation des dommages de l’ADN. Cela inclut ATRX et des gènes de réparation bien connus tels que BRCA1, BRCA2, ATM et ATR. De nombreux patients présentaient également des mutations héréditaires dans les gènes SDHx, déjà associés à ces tumeurs. L’association d’un métabolisme défaillant lié à SDHx et d’une réparation de l’ADN altérée suggère que certaines tumeurs pourraient être particulièrement vulnérables à des médicaments exploitant ces fragilités, notamment les inhibiteurs de PARP et d’autres thérapies ciblant la machinerie de réparation de l’ADN.
Évasion précoce et longue croissance silencieuse
Lorsque l’équipe a comparé chaque tumeur primaire à ses métastases, elle a constaté une surprenante faiblesse de recoupement pour les mutations de plus petite échelle. En moyenne, moins de 10 % des altérations potentiellement importantes étaient partagées. Pourtant des contrôles rigoureux ont confirmé que chaque paire provenait bien du même patient. En utilisant des méthodes d’« horloge moléculaire » qui infèrent le moment à partir du nombre de mutations accumulées, les auteurs estiment que les cellules fondatrices des métastases se sont souvent séparées très tôt — environ 18 ans avant le diagnostic de la tumeur primaire. Dans de nombreux cas, le véritable ensemencement des sites distants est survenu plus d’une décennie avant que les médecins ne découvrent la masse initiale. Les altérations à grande échelle de l’ADN, telles que les gains et pertes de chromosomes entiers, ont tendance à survenir tôt et à être partagées, tandis que la plupart des mutations plus petites apparaissent plus tard et de manière distincte à chaque emplacement.
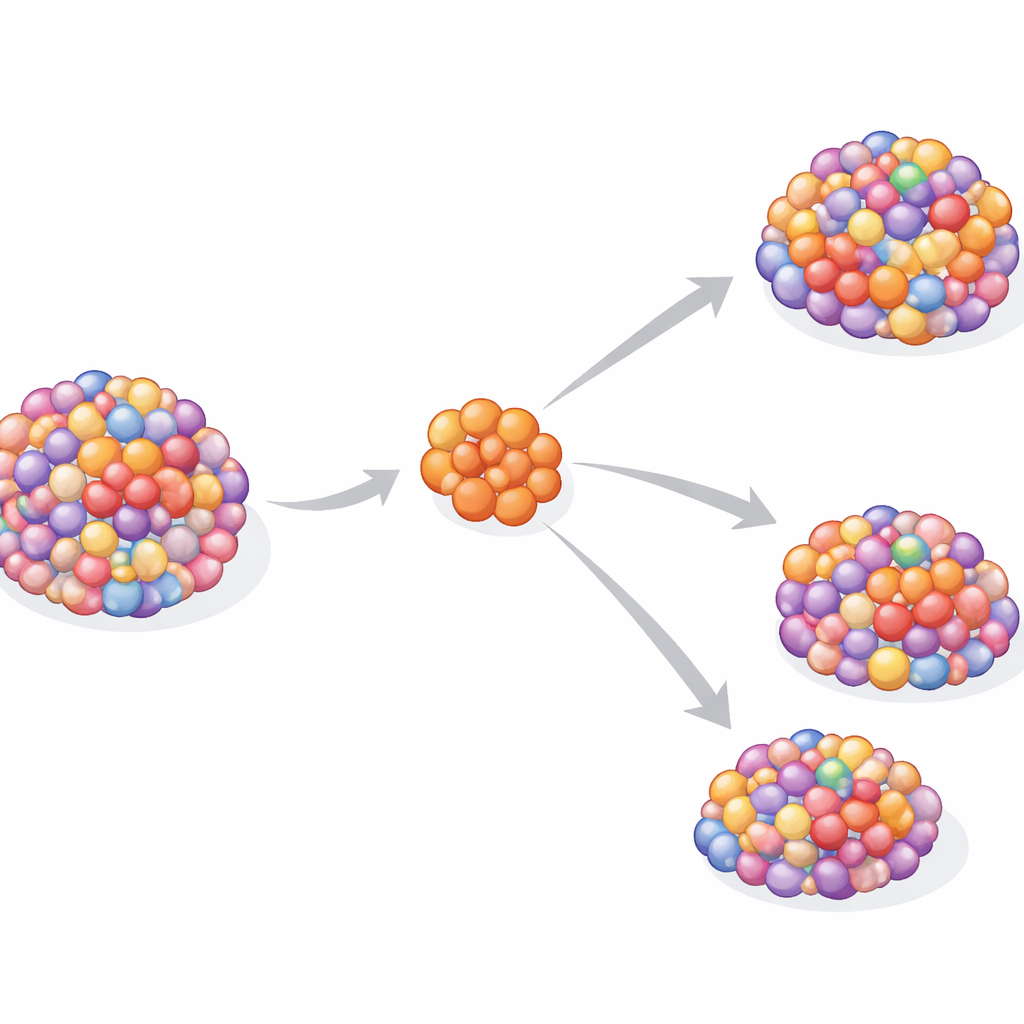
Un clone, de nombreux parcours séparés
Malgré la diversité génétique, les données suggèrent que chaque métastase a généralement commencé à partir d’une seule cellule ancestrale plutôt que d’un mélange. Ce schéma d’« ensemencement monoclonal » contraste avec certains autres cancers, où plusieurs branches de la tumeur primaire peuvent coloniser conjointement de nouveaux sites. Ici, un unique rameau semble quitter la tumeur précoce, s’établir ailleurs dans l’organisme, puis évoluer en grande partie de façon autonome pendant des années. Le résultat est une évolution parallèle : la tumeur primaire et les métastases partagent des changements structuraux précoces de l’ADN mais divergent ensuite, chacune acquérant au fil du temps son propre ensemble de mutations et de sensibilités potentielles aux traitements.
Ce que cela signifie pour les patients et le traitement
Pour les personnes confrontées à un phéochromocytome ou un paragangliome, ce travail brosse un tableau à la fois préoccupant et instructif. Les métastases ne sont pas simplement des ramifications tardives d’une tumeur primaire avancée ; ce sont des voyageurs précoces qui peuvent croître silencieusement pendant des années avant que quiconque ne sache qu’ils existent. En parallèle, l’étude révèle des atteintes récurrentes dans des gènes liés à la réparation de l’ADN et à la chromatine, ouvrant de nouvelles pistes thérapeutiques. Ensemble, ces résultats plaident en faveur d’une étude génétique plus approfondie des lésions métastatiques elles‑mêmes et soutiennent des essais de médicaments ciblant la réparation de l’ADN et les voies associées. Comprendre quand et comment ces tumeurs se propagent pourrait ultimement conduire à une détection plus précoce et à des traitements plus précis et personnalisés pour les patients.
Citation: Pregnall, A.M., Wubbenhorst, B., D’Andrea, K. et al. Metastatic progression of pheochromocytoma and paraganglioma occurs via parallel evolution. npj Precis. Onc. 10, 101 (2026). https://doi.org/10.1038/s41698-026-01291-7
Mots-clés: phéochromocytome, paragangliome, métastase, évolution tumorale, réparation de l’ADN