Clear Sky Science · fr
La perte du microARN-29b favorise la régulation à la baisse de STING médiée par DNMT3b pour atténuer l’immunité antitumorale induite par la radiothérapie dans le cancer colorectal muté sur KRAS
Pourquoi cette recherche est importante
Pour de nombreuses personnes atteintes de cancer du rectum ou du côlon, la radiothérapie constitue un élément clé du traitement avant la chirurgie. Pourtant, certaines tumeurs diminuent à peine et le cancer récidive ou se propage souvent. Cette étude examine un mécanisme associé à une altération génétique fréquente dans le cancer colorectal — la mutation KRAS — pour expliquer pourquoi ces tumeurs résistent souvent à la radiothérapie et aux immunothérapies récentes, et propose une stratégie pour réactiver le système immunitaire contre elles.
Une mutation fréquente qui cache les tumeurs aux attaques immunitaires
Le cancer colorectal présente fréquemment des mutations du gène KRAS, un moteur majeur de la croissance et de la dissémination tumorale. Les cliniciens avaient déjà constaté que les tumeurs mutées sur KRAS répondent moins bien aux traitements ciblés et à la radiothérapie. En exploitant de larges bases de données et en examinant des échantillons de patients, les auteurs ont constaté que les tumeurs porteuses de KRAS mutant présentent moins de lymphocytes CD8 tueurs de cancer et une activité plus faible des signaux immunostimulants de type interféron. Chez les patients ayant reçu la chimioradiothérapie standard avant la chirurgie du cancer rectal, ceux avec un KRAS normal avaient une augmentation bien plus marquée de CD8 intratumoraux après traitement que ceux porteurs de mutations KRAS, ce qui explique en partie leurs meilleurs résultats.
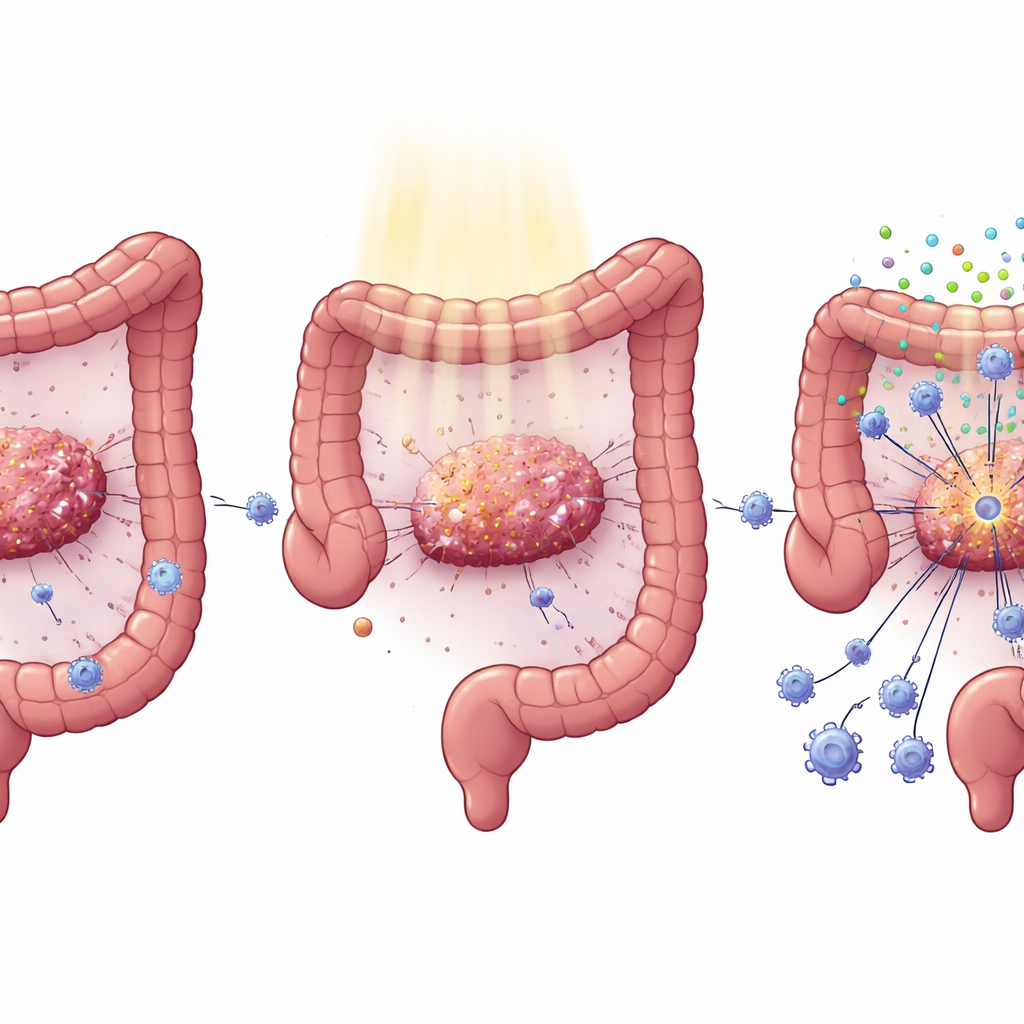
Le système d’alarme manquant à l’intérieur des cellules cancéreuses
La radiothérapie endommage non seulement l’ADN tumoral ; elle agit aussi comme une fusée éclairante, en provoquant la libération de fragments d’ADN qui déclenchent une voie d’alarme interne appelée cGAS–STING. Quand STING est actif, les cellules produisent des interférons de type I et d’autres signaux qui attirent et activent les cellules immunitaires, y compris les lymphocytes T et les cellules dendritiques. Les chercheurs ont montré que, dans des cellules de cancer colorectal génétiquement modifiées pour porter KRAS mutant, ce système d’alarme est affaibli : après irradiation, ces cellules produisent beaucoup moins d’interféron et de molécules associées. Chez la souris, la suppression de KRAS dans les tumeurs a restauré les niveaux de STING, renforcé les signaux d’interféron et entraîné une augmentation des lymphocytes CD4 et CD8, une diminution des lymphocytes T régulateurs et un meilleur contrôle tumoral — non seulement dans les tumeurs irradiées, mais aussi dans des tumeurs « abscopiques » distantes non irradiées.
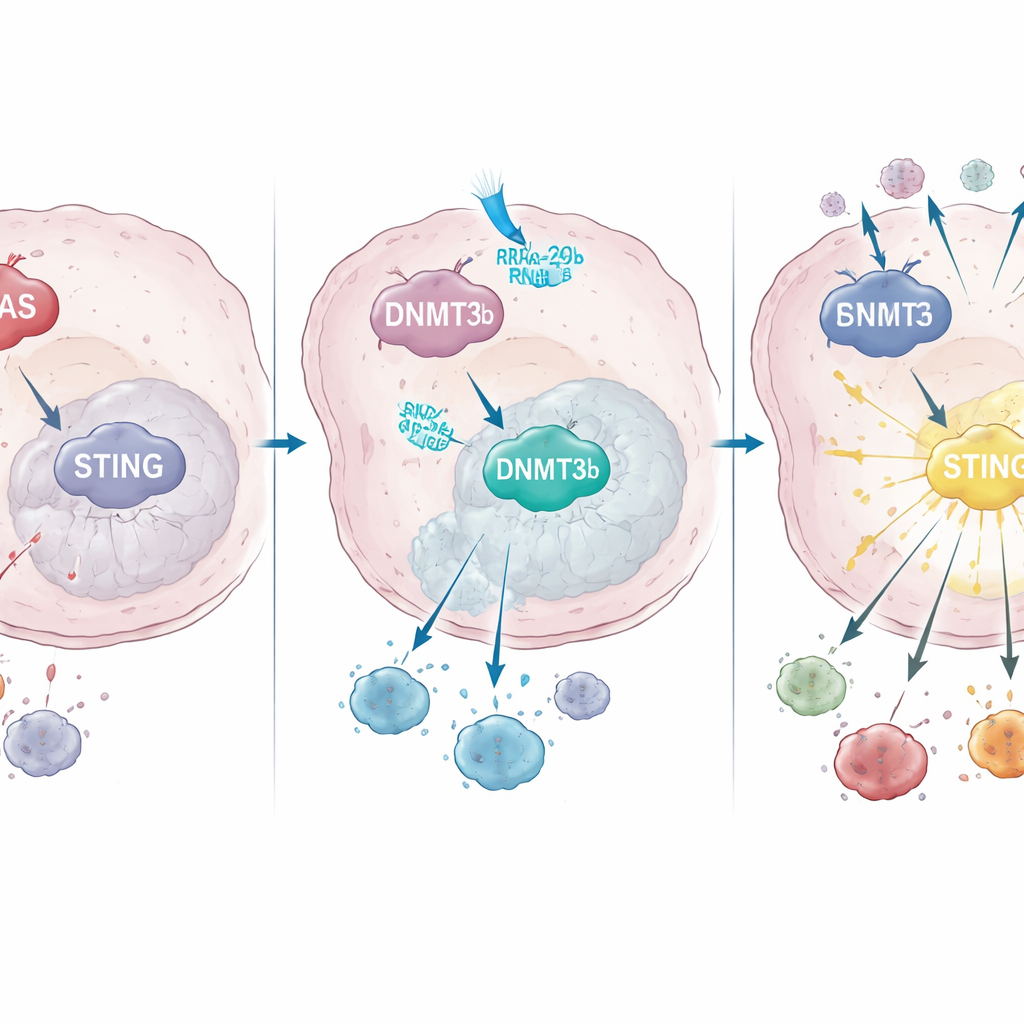
Comment KRAS reconfigure le contrôle génique pour éteindre STING
En approfondissant l’analyse, l’équipe a découvert que KRAS mutant augmente l’activité d’une enzyme modifiant l’ADN appelée DNMT3b, qui ajoute des groupes méthyle à certaines régions de l’ADN et réprime ainsi les gènes voisins. Tant dans des lignées cellulaires que dans des échantillons de patients, des niveaux élevés de DNMT3b allaient de pair avec une faible expression de STING. Une portion clé du promoteur de STING — la région « marche/arrêt » de l’ADN — était fortement méthylée dans les tumeurs KRAS-mutées, mais pas dans celles à KRAS normal. Les patients dont les tumeurs pouvaient encore réguler à la hausse STING après chimioradiothérapie présentaient une infiltration plus importante de cellules T CD8 et une survie meilleure, soulignant l’importance de cette voie pour l’efficacité du traitement.
Un petit ARN capable de réactiver l’alarme
Les auteurs se sont ensuite demandé pourquoi DNMT3b est si abondant dans les cancers KRAS-mutés. Par séquençage des microARN, ils ont identifié un petit ARN régulateur, le microARN‑29b‑3p, qui maintient normalement DNMT3b sous contrôle mais est fortement réprimé par KRAS mutant. Restaurer ce microARN dans des cellules KRAS-mutées cultivées en laboratoire a diminué DNMT3b, ravivé STING et augmenté la production d’interféron après irradiation ; l’inhiber produisait l’effet inverse. Dans des échantillons tumoraux, les patients KRAS-mutés avaient tendance à présenter de faibles niveaux de microARN‑29b‑3p, un DNMT3b élevé et un STING bas, et ceux avec des niveaux plus élevés de microARN‑29b‑3p vivaient plus longtemps, reliant cette chaîne moléculaire aux résultats cliniques.
Une approche de délivrance génique ciblée qui potentialise radiothérapie et immunothérapie
Pour traduire ces découvertes en traitement potentiel, l’équipe a conçu un adénovirus adéno-associé (AAV) inoffensif qui délivre le microARN‑29b‑3p sous le contrôle d’un promoteur principalement actif dans les cellules du cancer colorectal. Dans des modèles murins portant des tumeurs colorectales KRAS-mutées, l’administration de cet AAV en association avec une radiothérapie localisée a considérablement réduit à la fois les tumeurs irradiées et les tumeurs distantes non irradiées. Les tumeurs présentaient une baisse de DNMT3b, une augmentation de STING, des signaux d’interféron renforcés et une forte infiltration de lymphocytes T et autres cellules immunitaires. Lorsque le même traitement par microARN‑29b‑3p était combiné à un inhibiteur de point de contrôle immunitaire ciblant PD‑1, la survie s’est encore améliorée ; ce bénéfice dépendait des lymphocytes CD8, confirmant que le système immunitaire était l’effecteur principal.
Ce que cela pourrait signifier pour les patients
En termes simples, cette étude révèle comment les cancers colorectaux mutés sur KRAS « coupent le fil » d’un système d’alarme interne que la radiothérapie déclenche normalement, leur permettant d’échapper à l’attaque immunitaire. En restaurant un seul petit ARN, le microARN‑29b‑3p, les chercheurs ont pu réduire DNMT3b, réveiller STING et transformer des tumeurs immunologiquement « froides » en tumeurs « chaudes » mieux réceptives à la radiothérapie et au blocage des points de contrôle. Bien que ce travail soit encore préclinique, il oriente vers des traitements futurs associant radiothérapie et thérapie génique ciblée sur la tumeur pour surmonter la résistance dans le cancer colorectal KRAS‑muté, et rendre potentiellement les thérapies existantes efficaces pour beaucoup plus de patients.
Citation: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Mots-clés: cancer colorectal muté sur KRAS, résistance à la radiothérapie, voie STING, microARN-29b, immunologie tumorale