Clear Sky Science · fr
Une atlas intégré du cancer du poumon au niveau unicellulaire révèle des phénotypes de fibroblastes distincts entre adénocarcinomes et carcinomes épidermoïdes
Pourquoi le voisinage autour d'une tumeur importe
Le cancer du poumon n'est pas composé uniquement de cellules cancéreuses. Il ressemble plutôt à une ville dense où les cellules tumorales coexistent avec des vaisseaux sanguins, des cellules immunitaires et des cellules de soutien. Cette étude pose une question étonnamment simple mais lourde de conséquences : les deux formes majeures du cancer du poumon non à petites cellules — l'adénocarcinome et le carcinome épidermoïde — construisent-elles des « quartiers » différents dans le poumon, et ces différences pourraient-elles aider à expliquer pourquoi les patients ont des trajectoires différentes ? En utilisant des outils puissants de lecture de l'ADN à l'échelle unicellulaire, les chercheurs cartographient des centaines de milliers de cellules individuelles pour révéler comment un groupe clé de cellules de soutien, appelées fibroblastes, se comporte très différemment dans ces deux cancers.
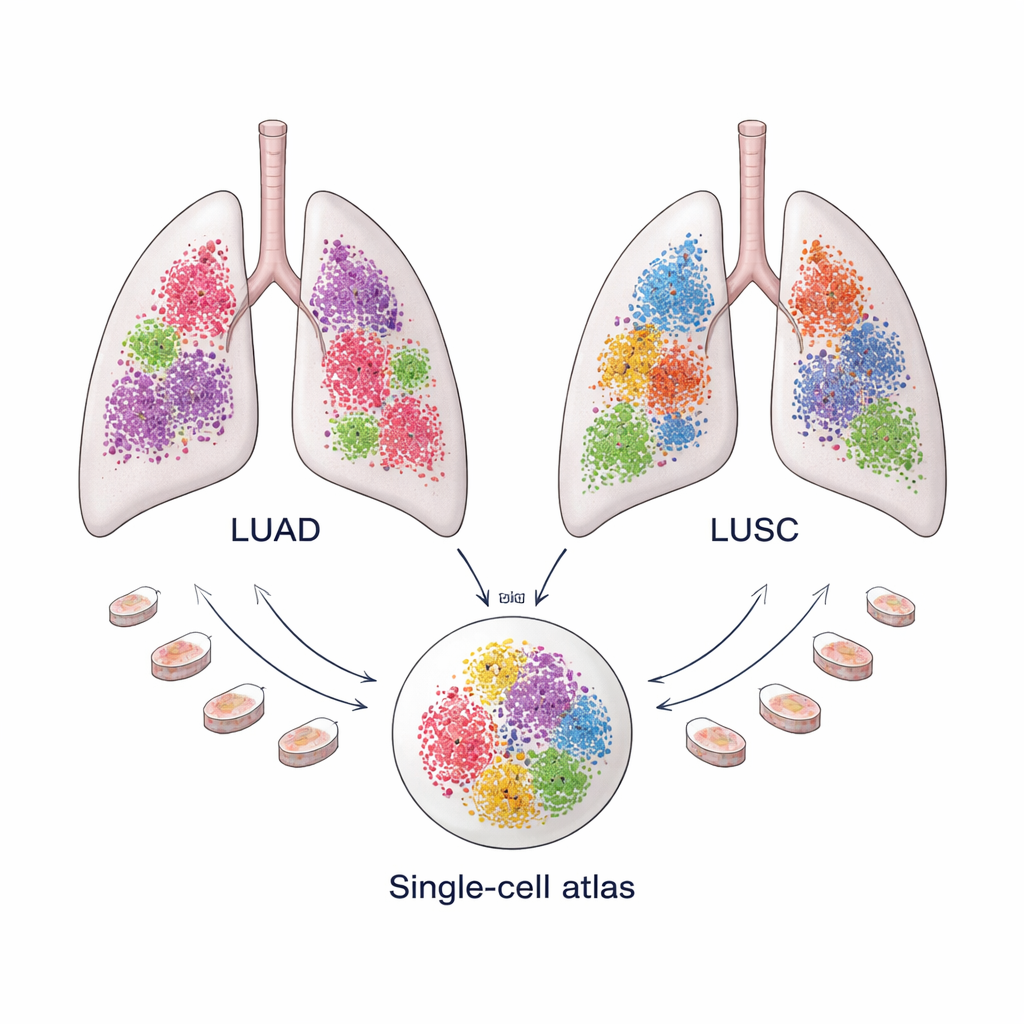
Deux cancers pulmonaires fréquents, deux écosystèmes distincts
Le cancer du poumon non à petites cellules représente environ 85 % des cancers pulmonaires et est dominé par deux types : l'adénocarcinome pulmonaire (LUAD), qui apparaît souvent dans les zones périphériques du poumon, et le carcinome épidermoïde pulmonaire (LUSC), qui a tendance à survenir plus centralement. Bien que les deux soient aujourd'hui traités sous une même étiquette générale, ils répondent différemment aux thérapies et présentent des résultats à long terme distincts. Des preuves croissantes suggèrent que ces différences ne sont pas seulement dues aux cellules cancéreuses elles-mêmes, mais aussi au « microenvironnement tumoral » — le mélange de cellules immunitaires, de vaisseaux sanguins et de cellules structurelles qui entourent et interagissent avec la tumeur.
Construire un atlas unicellulaire du cancer du poumon
Pour comprendre ces microenvironnements en détail, l'équipe a assemblé un vaste « atlas » de données de séquençage d'ARN unicellulaire : 366 652 cellules provenant de 175 échantillons de LUAD et 125 238 cellules provenant de 74 échantillons de LUSC, extraites de dix jeux de données publics. Le profil d'expression génique de chaque cellule a servi d'empreinte permettant aux chercheurs de classer les cellules en grands groupes tels que les cellules immunitaires, les cellules vasculaires, les cellules cancéreuses et les cellules structurelles ou « stromales ». Des méthodes informatiques sophistiquées ont ensuite supprimé le bruit technique et aligné les échantillons afin que les cellules de différents patients puissent être comparées directement. Cette ampleur est cruciale, car certains types cellulaires — en particulier les fibroblastes — sont rares et difficiles à isoler en nombre suffisant dans une seule étude.
Les fibroblastes : les façonneurs du paysage tumoral
Les fibroblastes sont des cellules de soutien qui construisent et remodelent le tissu conjonctif. Dans les tumeurs, ils deviennent des fibroblastes associés au cancer (CAF), qui peuvent soit freiner, soit favoriser la croissance tumorale selon leur état. En se concentrant sur plus de 8 700 fibroblastes, les auteurs ont identifié cinq sous-types majeurs de CAF : les CAF myofibroblastiques (mCAF), les CAF inflammatoires (iCAF), les CAF associés aux vaisseaux (vCAF), les CAF en cycle (cCAF) et les CAF présentant des antigènes (apCAF). L'équilibre entre ces sous‑types différait de façon marquée entre LUAD et LUSC. Les tumeurs LUAD avaient tendance à abriter davantage d'iCAF, qui sécrètent de fortes quantités de molécules inflammatoires, tandis que les tumeurs LUSC étaient plus riches en mCAF, qui produisent un tissu dur et fibreux et contribuent à façonner l'échafaudage physique de la tumeur.
Les cellules cancéreuses enseignent aux fibroblastes leurs rôles
Pour tester si les cellules cancéreuses elles‑mêmes instruisent les fibroblastes à adopter ces identités, les chercheurs ont cultivé des fibroblastes pulmonaires normaux en présence de lignées cellulaires LUAD ou LUSC. Exposés aux cellules LUAD, les fibroblastes ont activé des gènes typiques des iCAF, y compris des signaux inflammatoires bien connus tels que IL‑6 et certaines chimiokines. Associés aux cellules LUSC, les mêmes fibroblastes ont plutôt exprimé des gènes mCAF impliqués dans la contraction de type musculaire et la production de collagène. Des analyses de la communication cellule à cellule ont suggéré que les cellules LUAD utilisent des cytokines telles que IL‑1, LIF et OSM pour induire l'état inflammatoire iCAF, tandis que les cellules LUSC s'appuient davantage sur des signaux mécaniques et la signalisation WNT non canonique pour pousser les fibroblastes vers l'état mCAF axé sur la matrice.
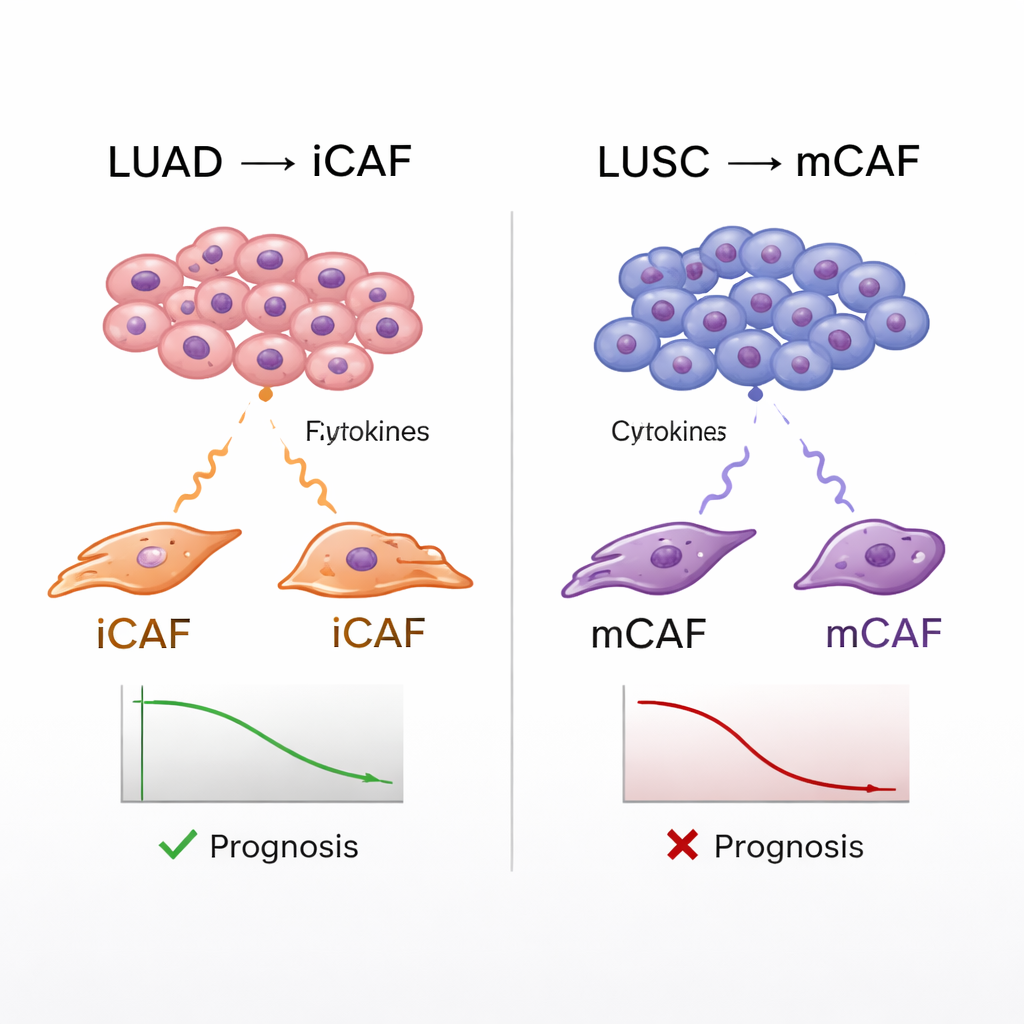
Relier les types de fibroblastes aux résultats des patients
L'atlas a aussi permis à l'équipe de relier les sous‑types de CAF aux données cliniques réelles. En utilisant de larges bases de données sur le cancer, ils ont estimé à quel point la tumeur de chaque patient exprimait des signatures géniques correspondant aux différents types de fibroblastes, puis ont comparé ces scores à la survie. Dans les deux groupes LUAD et LUSC, les tumeurs enrichies en mCAF étaient associées à des résultats plus défavorables, ce qui concorde avec l'idée qu'une capsule dense et fibreuse autour des tumeurs peut favoriser la progression tumorale et bloquer l'attaque immunitaire. Les iCAF, en revanche, présentaient une personnalité partagée : dans le LUSC, des signatures iCAF élevées prédisaient également une survie plus mauvaise, alors que dans le LUAD elles étaient associées à de meilleurs résultats. Des analyses supplémentaires ont suggéré que, dans le LUSC, les iCAF contribuent à attirer des neutrophiles — des cellules immunitaires qui, dans ce contexte, semblent supprimer les lymphocytes T utiles — créant un environnement particulièrement hostile aux réponses immunitaires efficaces.
Ce que cela signifie pour les soins futurs du cancer du poumon
Pour un non‑spécialiste, le message clé est que les cellules de soutien dans les tumeurs pulmonaires ne sont pas toutes identiques, et qu'un même sous‑type de fibroblaste peut avoir des significations opposées selon le contexte tumoral. LUAD et LUSC ne diffèrent pas seulement par l'ADN de leurs cellules cancéreuses ; ils construisent des écosystèmes microscopiques différents qui influencent la croissance tumorale et le pronostic des patients. En cartographiant ces écosystèmes cellule par cellule, cette étude identifie des populations de fibroblastes spécifiques qui pourraient servir de marqueurs pronostiques ou de cibles pour de futures thérapies — permettant idéalement d'adapter les traitements non seulement au type de cancer, mais aussi au mélange de cellules qui l'entourent et le soutiennent.
Citation: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Mots-clés: cancer du poumon, microenvironnement tumoral, fibroblastes, séquençage d'ARN unicellulaire, pronostic du cancer