Clear Sky Science · fr
Traitement néoadjuvant par sintilimab, paclitaxel lié à l’albumine et carboplatine pour un carcinome épidermoïde œsophagien localement avancé et résécable : étude clinique et exploration mécanistique
Renverser la tendance face à un cancer de la gorge mortel
Le cancer de l’œsophage est l’un des cancers les plus mortels au monde, souvent découvert seulement après qu’il s’est profondément étendu dans le thorax. De nombreux patients restent candidats à la chirurgie, mais même avec la chimiothérapie et la radiothérapie actuelles, le risque de récidive demeure élevé. Cette étude teste une nouvelle façon de renforcer les défenses de l’organisme avant l’intervention et examine au microscope comment les tumeurs et leurs cellules environnantes évoluent en réponse. Les résultats suggèrent des traitements plus efficaces et ouvrent la voie à des soins véritablement personnalisés.
Un nouveau protocole en trois médicaments avant la chirurgie
Les chercheurs ont inclus 24 personnes en Chine atteintes d’une forme courante et agressive de cancer œsophagien, le carcinome épidermoïde. Toutes avaient des tumeurs localement avancées mais encore résécables. Avant l’intervention, chaque patient a reçu trois cycles d’un traitement combiné : sintilimab, un anticorps stimulant le système immunitaire qui aide les lymphocytes T à reconnaître le cancer ; plus deux chimiothérapies standard, le paclitaxel lié à l’albumine et le carboplatine. Après cette phase néoadjuvante, les patients ont subi une chirurgie d’ablation de la tumeur œsophagienne, et la plupart ont ensuite poursuivi le sintilimab en post-opératoire.
Réduction tumorale plus marquée et survie encourageante
Lorsque chirurgiens et pathologistes ont examiné les tumeurs retirées, ils ont constaté que ce schéma préopératoire avait entraîné une forte régression chez de nombreux patients. Environ 42 % ont présenté ce que les cliniciens appellent une réponse pathologique majeure, signifiant qu’il ne restait qu’une faible fraction de cellules tumorales viables. Un patient sur trois n’avait plus de cellule tumorale détectable dans la zone principale de la tumeur. Sur les images et le suivi clinique, les résultats étaient également prometteurs : trois ans après le traitement, approximativement trois patients sur quatre étaient en vie sans signe de récidive, et près de quatre sur cinq étaient encore vivants. Fait important, les effets indésirables de ce protocole intensifié étaient acceptables, sans décès liés au traitement et avec une résection chirurgicale restée sûre et réalisable.
Comment le voisinage tumoral façonne la réponse
Tous les patients n’ont pas bénéficié de la même façon, et l’équipe a cherché à comprendre pourquoi. Ils se sont concentrés sur le microenvironnement tumoral — le voisinage complexe de cellules cancéreuses, de cellules immunitaires et de molécules de signalisation. En utilisant des mesures ciblées de protéines sur des échantillons tumoraux minutieusement disséqués, ils ont comparé les bons répondeurs aux non-répondeurs. Avant le traitement, ils ont identifié 14 protéines différentielles entre ces deux groupes. Une protéine de surface, CD44, s’est particulièrement distinguée : les tumeurs avec des niveaux plus élevés de CD44 avaient tendance à mieux répondre à la thérapie à base de sintilimab. Après le traitement, de nombreuses protéines impliquées dans l’activité immunitaire et la réparation de l’ADN étaient réduites chez les répondeurs, suggérant que la thérapie combinée avait perturbé les systèmes de soutien du cancer et remodelé le paysage immunitaire local.
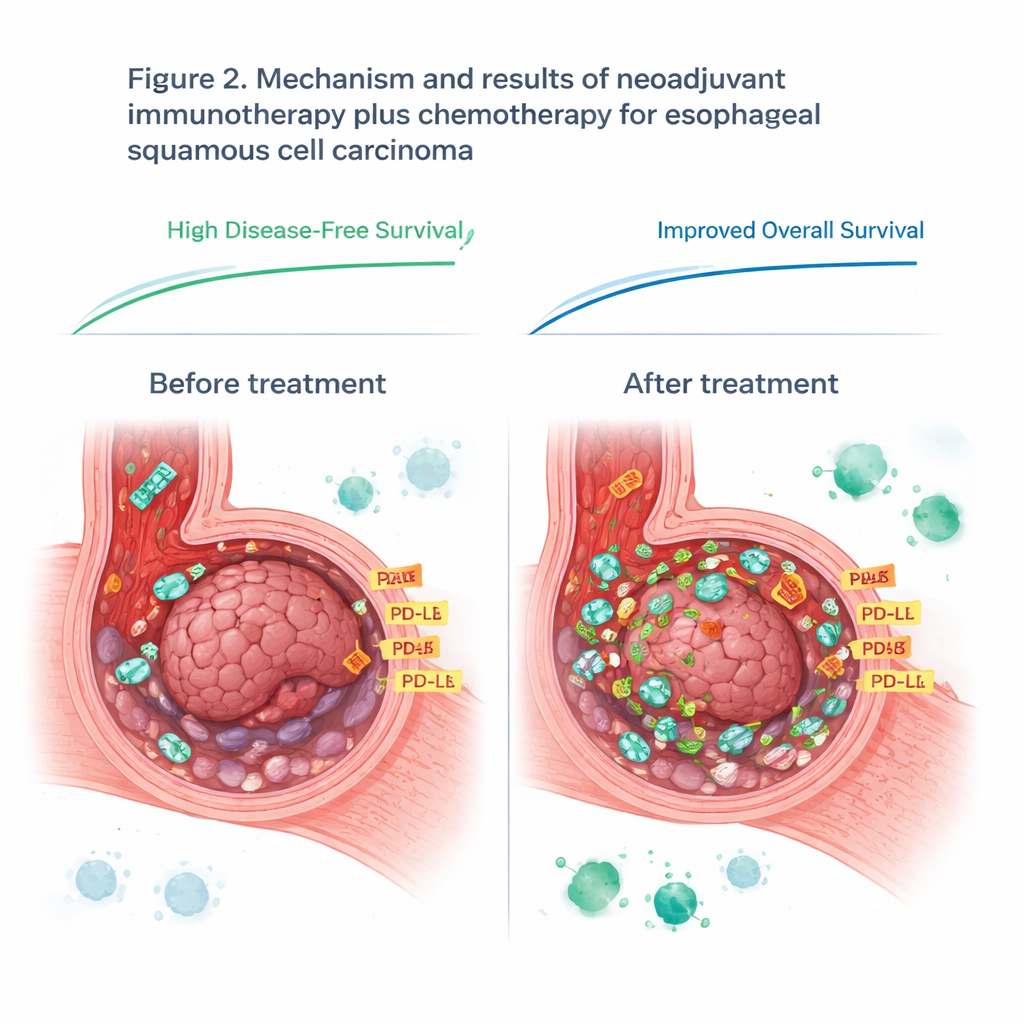
Repenser un marqueur immunitaire populaire
L’étude a également examiné le PD-L1, une protéine souvent utilisée comme indicateur pour décider qui pourrait bénéficier des inhibiteurs de point de contrôle immunitaire. Avant le traitement, les niveaux de PD-L1 sur les échantillons tumoraux n’ont pas prédit les bons résultats, remettant en question la pratique actuelle pour ce type de cancer. Cependant, les niveaux de PD-L1 ont augmenté chez tous les patients pendant le traitement, probablement parce que le système immunitaire activé a inondé la tumeur de signaux inflammatoires. Après la thérapie, des niveaux plus élevés de PD-L1 dans les tissus tumoraux résiduels étaient davantage corrélés à l’efficacité de l’immunothérapie. Cela suggère que le moment d’évaluation est important : une mesure unique du PD-L1 avant le traitement peut manquer des changements cruciaux qui se produisent une fois le système immunitaire activé.
Ce que cela signifie pour les patients et l’avenir
Pour les personnes candidates à une chirurgie pour un cancer œsophagien avancé, cette étude véhicule deux messages encourageants. D’une part, l’association du sintilimab avec la chimiothérapie avant la chirurgie semble induire des régressions tumorales plus profondes et pourrait améliorer les chances de survie à long terme, sans entraîner d’effets secondaires dangereux supplémentaires. D’autre part, les travaux montrent que la tumeur et son microenvironnement ne sont pas immuables ; ils sont remodelés par le traitement de manières traçables par des protéines comme PD-L1 et CD44. À l’avenir, ces empreintes moléculaires pourraient aider les médecins à sélectionner et adapter les thérapies en temps réel, transformant davantage de tumeurs « froides » — qui ignorent le système immunitaire — en tumeurs « chaudes » qui suscitent une attaque immunitaire puissante et durable.
Citation: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Mots-clés: cancer de l’œsophage, immunothérapie, traitement néoadjuvant, inhibiteurs de PD-1, microenvironnement tumoral