Clear Sky Science · fr
La transcriptomique spatiale révèle l'hétérogénéité moléculaire et des cibles thérapeutiques spécifiques aux sous‑types dans le cancer du poumon à petites cellules
Pourquoi cette étude sur le cancer du poumon est importante
Le cancer du poumon à petites cellules est l’une des formes les plus meurtrières de cancer, touchant principalement des personnes ayant un passé tabagique et réapparaissant souvent rapidement après chimiothérapie. Les cliniciens savent que tous les cancers à petites cellules ne se comportent pas de la même façon, mais ils manquaient d’outils pour observer comment différents types de cellules tumorales et cellules immunitaires sont organisés à l’intérieur d’une tumeur. Cette étude a utilisé une nouvelle technologie qui lit l’activité génétique en milliers de petits emplacements à travers une lame tumorale, créant une « carte moléculaire » de chaque échantillon. En associant cela à des analyses informatiques sur mesure, les chercheurs ont mis au jour des motifs cachés susceptibles d’indiquer des traitements plus précis et spécifiques à chaque sous‑type.
Cartographier les tumeurs in situ
L’équipe a analysé des échantillons tumoraux de 21 patients atteints d’un cancer du poumon à petites cellules en stade limité, opérés avant toute prise en charge médicamenteuse. Plutôt que de broyer les tissus et de perdre l’information spatiale, ils ont appliqué la transcriptomique spatiale : une technique qui mesure quels gènes sont activés à de nombreux emplacements définis d’une coupe tissulaire. Chaque point conserve sa position d’origine, ce qui permet aux scientifiques de relier l’activité génique à l’emplacement physique des cellules tumorales, des cellules normales et des cellules immunitaires. Ils ont ajouté deux outils clés : un nouveau score « Edgeindex » pour quantifier l’infiltration des cellules tumorales dans les tissus voisins, et un réseau neuronal artificiel — une forme d’apprentissage automatique — pour marquer automatiquement quels points sont tumoraux et lesquels ne le sont pas.
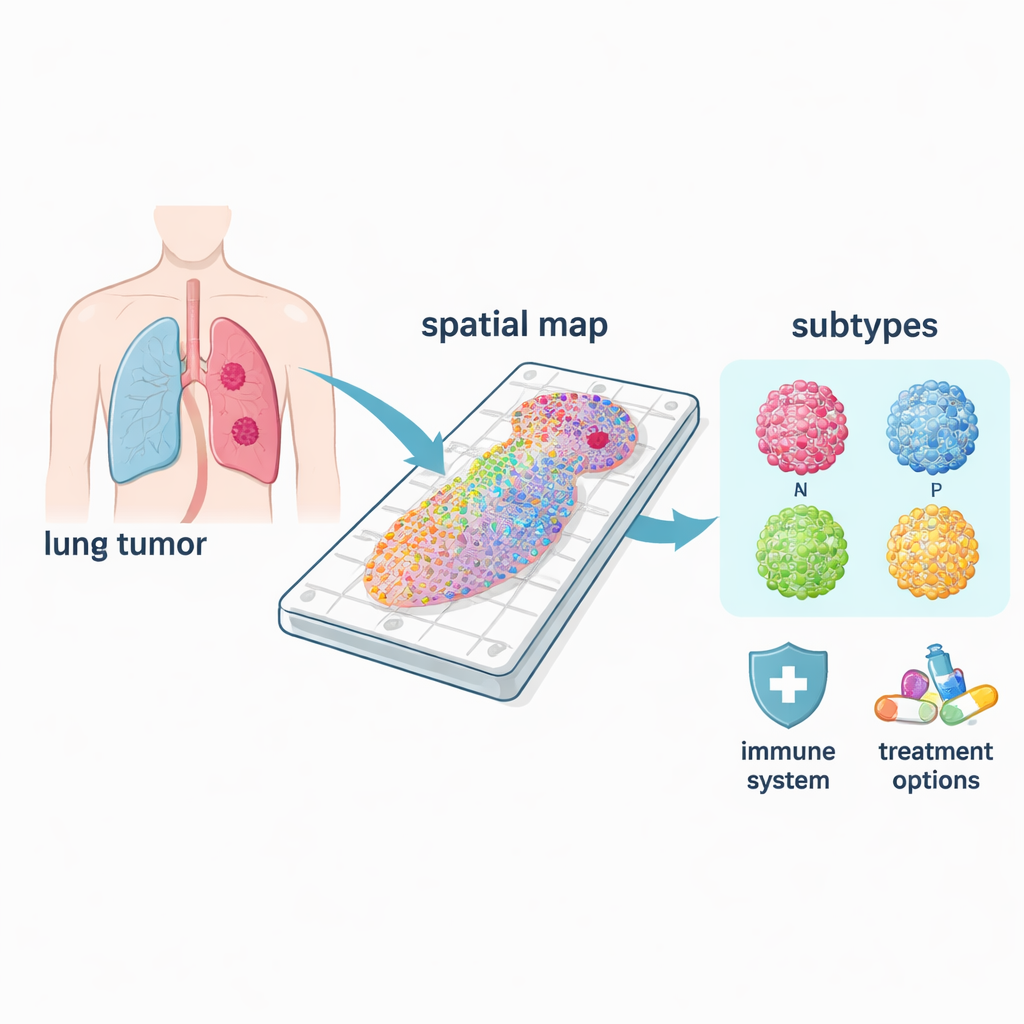
Différents types de cancer dans une même maladie
Le cancer du poumon à petites cellules n’est pas une maladie unique mais comprend au moins quatre sous‑types moléculaires principaux, souvent désignés ASCL1, NEUROD1, POU2F3 et YAP1, d’après des gènes régulateurs clés qui les définissent. Grâce à leurs cartes spatiales, les chercheurs ont pu voir où chaque sous‑type dominait au sein des tumeurs et en quoi leur biologie différait. Les formes courantes ASCL1 et NEUROD1 étaient fortement associées à des programmes de division cellulaire, correspondant à leur réputation de forte prolifération. En revanche, les régions POU2F3 étaient liées à des voies immunitaires, tandis que les zones YAP1 montraient des signaux en lien avec le métabolisme et le remodelage tissulaire, des caractéristiques pouvant être reliées à la dissémination et à la résistance aux traitements. Parce que ces motifs sont résolus dans l’espace, la méthode peut identifier le véritable sous‑type « conducteur » au sein d’une tumeur mixte, ce que les analyses en vrac manquent souvent.
Le front envahissant et le basculement immunitaire
Une des innovations centrales de l’étude, l’Edgeindex, capture le degré d’entremêlement des cellules tumorales avec le tissu non tumoral environnant. Les scores bas reflètent des tumeurs compactes et bien délimitées, tandis que les scores élevés indiquent des îlots dispersés et des bords irréguliers et invasifs. Les tumeurs avec un Edgeindex élevé étaient enrichies en programmes géniques liés à la matrice extracellulaire, à la métastase et à la mort cellulaire. Elles présentaient aussi un paysage immunitaire nettement modifié : moins de lymphocytes T auxiliaires et d’autres acteurs de l’immunité adaptative, mais davantage de cellules innées telles que certains lymphocytes NK et des monocytes. Les auteurs interprètent cela comme un « remodelage du niche immunologique », où la tumeur écarte les réponses immunitaires précises et ciblées au profit d’une défense principalement innée, moins efficace pour contrôler la maladie.
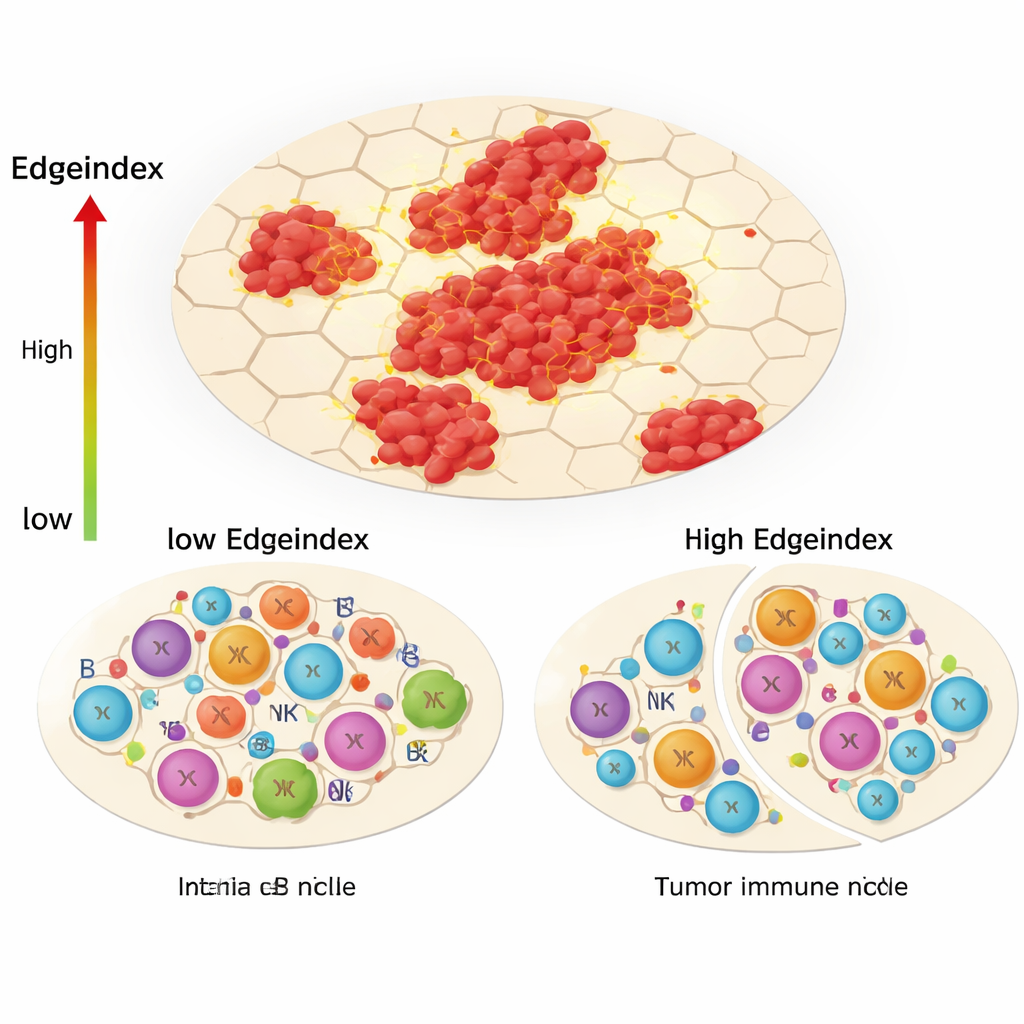
Diversité cachée à l’intérieur et autour des tumeurs
Au‑delà des sous‑types et des schémas d’invasion, les données spatiales ont révélé que tant les populations de cellules tumorales que leurs microenvironnements voisins étaient eux‑mêmes internesment divers. En regroupant les points au sein de chaque tumeur, l’équipe a compté combien de « voisinages » d’expression génique distincts existaient dans les régions tumorales et dans les tissus non tumoraux adjacents. Une diversité plus élevée à l’intérieur de la tumeur était liée à des voies associées à l’immunité, tandis que certains motifs dans le tissu environnant se rattachaient à l’activité du cycle cellulaire et à la régulation génétique. Les chercheurs ont aussi examiné l’intensité de la « communication » entre régions à l’aide de molécules de signalisation connues. Les tumeurs présentant une communication plus intense entre régions avaient tendance à montrer des signaux immunitaires plus forts, renforçant l’idée que l’activité immunitaire et la croissance tumorale sont étroitement imbriquées dans l’espace.
Suivre le développement tumoral au fil du temps
Pour approcher la manière dont les cellules tumorales évoluent avec la progression de la maladie, l’équipe a réalisé une analyse de « pseudotemps » qui ordonne les cellules le long d’un trajet développemental en se basant sur leur activité génique. À travers les échantillons, elles ont identifié de manière récurrente un gène, UCHL1, comme central dans ces trajectoires. Des niveaux élevés d’UCHL1 coïncidaient avec une forte activité du cycle cellulaire dans les points tumoraux, tandis que des niveaux plus bas s’associaient à des voies immunitaires et de mort cellulaire. Comme UCHL1 est une protéine de type neuronale précédemment liée à des cancers pulmonaires agressifs, ces résultats renforcent l’idée qu’elle pourrait constituer une cible médicamenteuse pertinente, en particulier pour les cellules de type neuroendocrine qui pilotent le cancer du poumon à petites cellules.
Ce que cela signifie pour les patients
En termes simples, cette étude transforme des lames microscopiques plates de cancer du poumon à petites cellules en cartes riches et stratifiées qui montrent où se situent les différents sous‑types tumoraux, à quel point ils envahissent, comment ils dialoguent avec leur environnement et comment le système immunitaire répond — ou échoue à répondre. Le nouveau score Edgeindex et l’approche de cartographie mettent en évidence quelles tumeurs sont particulièrement infiltratives et quelles cellules immunitaires sont présentes ou absentes à la frontière. En reliant ces motifs spatiaux à des vulnérabilités spécifiques aux sous‑types — par exemple des médicaments ciblant DLL3, BCL‑2, AURKA, IGF‑1R/PARP ou des points de contrôle immunitaire — le travail rapproche le domaine d’une stratégie thérapeutique adaptée à chaque patient. Bien que ces outils doivent encore être validés dans des études plus larges, ils fournissent une feuille de route pour des thérapies plus précises et potentiellement plus efficaces contre une forme de cancer qui a un besoin urgent de meilleures options.
Citation: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Mots-clés: cancer du poumon à petites cellules, transcriptomique spatiale, hétérogénéité tumorale, microenvironnement immunitaire tumoral, oncologie de précision