Clear Sky Science · fr
Les caractéristiques de pathologie computationnelle de l’architecture immunitaire prédisent des résultats cliniquement pertinents dans le cancer du poumon à petites cellules (CPPC)
Pourquoi les défenseurs de l’organisme comptent dans le cancer du poumon
Le cancer du poumon à petites cellules est l’une des formes les plus agressives de cancer du poumon, se propageant souvent rapidement et revenant après le traitement. Les médecins peuvent observer les tumeurs au microscope, mais les motifs fins de la façon dont les cellules cancéreuses et les cellules immunitaires se côtoient sont trop complexes pour être jugés à l’œil nu. Cette étude présente une méthode informatisée appelée PhenopyCell qui lit ces motifs cachés à partir de lames de biopsie de routine et les utilise pour prédire la durée de survie des patients et la probabilité de réponse à la chimiothérapie. Pour les patients et leurs familles, ce type d’information pourrait un jour aider à adapter les traitements plutôt que de s’en remettre à une approche uniforme.
Un examen approfondi d’un cancer pulmonaire mortel
Le cancer du poumon à petites cellules représente environ 15 % des cancers du poumon mais cause une part importante des décès en raison de sa croissance et de sa dissémination rapides. Il est généralement classé en maladie « limitée », pouvant tenir dans un seul champ de radiothérapie, et en maladie « étendue », ayant diffusé plus largement. Le traitement initial standard implique une chimiothérapie à base de platine puissante, parfois associée à une immunothérapie. De nombreuses tumeurs semblent régresser au début, mais le cancer revient souvent en moins d’un an, et moins d’un patient sur dix survit à long terme. Les tests actuels basés sur la taille de la tumeur, son extension et l’aspect microscopique de base ne rendent pas compte des raisons pour lesquelles certains patients répondent mieux que d’autres aux mêmes médicaments.
Apprendre aux ordinateurs à lire les quartiers tumoraux
Les chercheurs ont développé PhenopyCell pour transformer des lames de tissu colorées standard en une carte détaillée des « quartiers » cellulaires. À l’aide d’outils d’apprentissage profond existants, ils ont d’abord appris à un ordinateur à repérer et à marquer les cellules tumorales et les cellules immunitaires individuelles sur des images numériques de biopsies de 281 patients traités dans trois centres américains. Ils ont ensuite divisé chaque lame en régions tumorales, tissus proches et zones non tumorales éloignées, puis calculé plus d’une centaine de caractéristiques numériques. Ces caractéristiques décrivent, par exemple, la densité d’amas de cellules immunitaires autour des grappes tumorales, la distance entre cellules immunitaires et cellules cancéreuses, la diversité du mélange cellulaire et la régularité de la disposition cellulaire sur la lame.
Des motifs cachés liés à la survie et à la réponse aux médicaments
Avec ces mesures, l’équipe a entraîné des modèles pour séparer les patients en groupes à risque plus ou moins élevé et pour prédire qui répondrait à la chimiothérapie à base de platine. Ils ont entraîné les modèles sur les cas d’un hôpital puis les ont testés sur les patients des deux autres hôpitaux. Sur l’ensemble des jeux de données, les motifs capturés par PhenopyCell étaient fortement corrélés à la survie globale et à l’efficacité de la chimiothérapie. Les patients dont les tumeurs présentaient de nombreux poches organisées de cellules immunitaires entourant étroitement les grappes tumorales avaient tendance à vivre plus longtemps. Ceux avec des cellules immunitaires dispersées ou rares et une distribution très inégale des cellules tumorales avaient plus de risques d’avoir une maladie agressive et des résultats défavorables. Ces associations subsistaient même après prise en compte de l’âge, du sexe et d’autres facteurs cliniques, et elles étaient observées tant dans les stades limités qu’étendus de la maladie.
Au-delà des boîtes noires et des examens microscopiques de routine
L’étude a également comparé PhenopyCell à de nouveaux modèles d’intelligence artificielle « fondamentaux » et aux mesures traditionnelles de cellules immunitaires appelées lymphocytes infiltrant la tumeur. Certains grands modèles d’apprentissage profond atteignaient une forte précision dans le groupe d’entraînement initial mais se comportaient de manière incohérente lorsqu’ils étaient testés sur des patients externes, soulevant des questions de stabilité. Le simple comptage des cellules immunitaires, qu’il soit estimé par ordinateur ou jugé par un pathologiste, ne permettait pas non plus de prédire de manière fiable la survie. En revanche, l’accent mis par PhenopyCell sur la manière dont les cellules immunitaires et tumorales sont disposées dans l’espace, et non seulement sur leur nombre, a fourni des signaux plus fiables et plus faciles à interpréter. Les caractéristiques utilisées peuvent être mises en relation directement avec des concepts biologiques tels que l’exclusion immunitaire, les zones de tissu nécrotique et les formes tumorales variables.
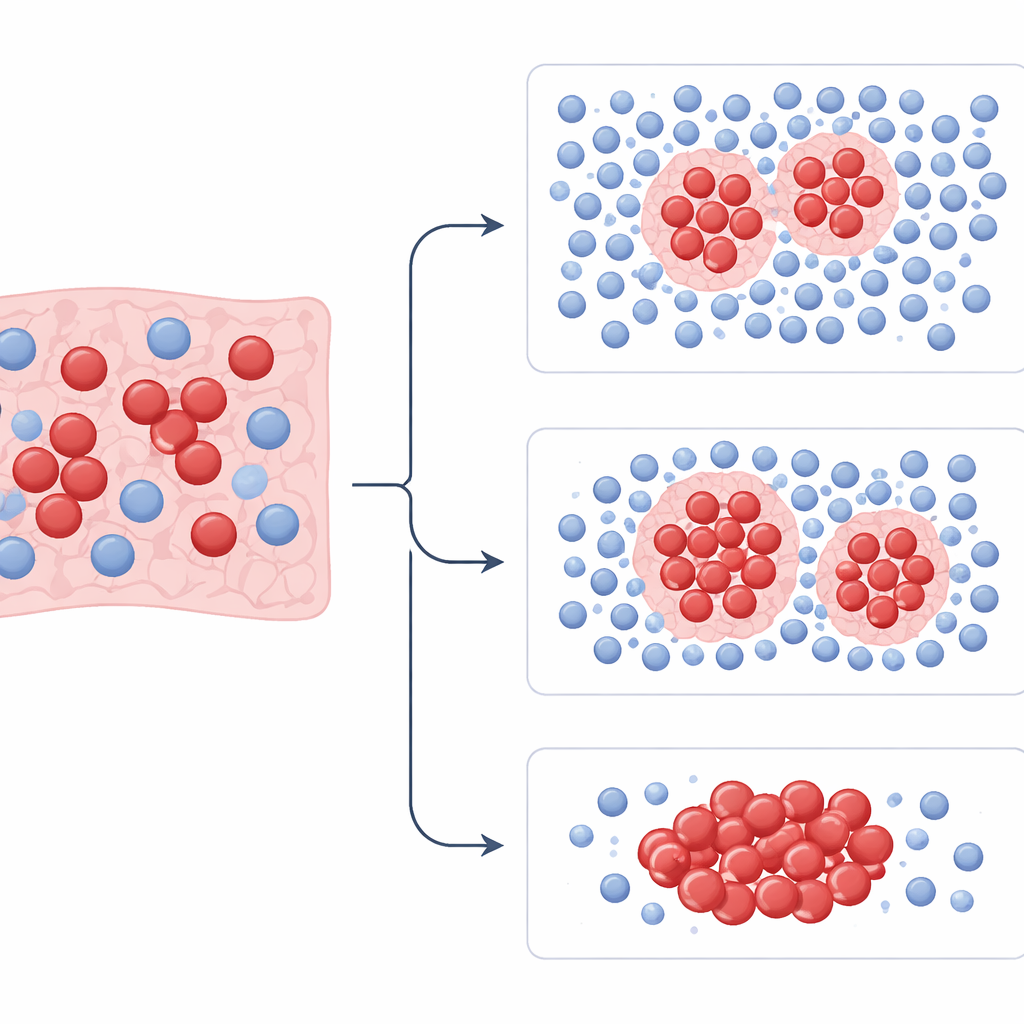
Ce que cela pourrait signifier pour les patients
Pour un non-spécialiste, le message principal est que l’« architecture » d’une tumeur — la façon dont les cellules cancéreuses et les défenseurs de l’organisme occupent le champ de bataille — contient des indices importants sur le comportement de la maladie et sa réponse au traitement. PhenopyCell montre que ces indices peuvent être extraits des mêmes lames de biopsie de routine déjà réalisées dans les soins standards, sans procédures supplémentaires. Bien que l’étude soit rétrospective et basée principalement sur des patients ayant reçu uniquement une chimiothérapie, elle suggère que des outils futurs pourraient aider les médecins à identifier les patients à plus haut risque, ceux qui pourraient bénéficier de traitements plus agressifs ou innovants, et ceux qui pourraient éviter des effets secondaires inutiles. Des études prospectives de plus grande ampleur, en particulier chez des patients recevant des immunothérapies modernes, seront nécessaires avant qu’un tel système puisse guider les décisions quotidiennes, mais ce travail trace une voie claire vers des soins plus personnalisés dans le cancer du poumon à petites cellules.
Citation: Barrera, C., Jain, P., Corredor, G. et al. Computational pathology features of immune architecture predict clinically relevant outcomes in small-cell lung cancer (SCLC). npj Precis. Onc. 10, 119 (2026). https://doi.org/10.1038/s41698-025-01225-9
Mots-clés: cancer du poumon à petites cellules, pathologie computationnelle, microenvironnement tumoral, architecture des cellules immunitaires, prédiction de la réponse au traitement