Clear Sky Science · fr
Vers des méthodes de scoring du microenvironnement tumoral pour la réponse aux inhibiteurs de points de contrôle immunitaire
Pourquoi prédire la réponse aux médicaments anticancéreux est important
Les inhibiteurs des points de contrôle immunitaire constituent une nouvelle classe de médicaments anticancéreux capables de libérer les défenses de l’organisme contre les tumeurs, conduisant parfois à des rémissions spectaculaires et durables. Pourtant, seule une fraction des patients en bénéficie, tandis que d’autres subissent des effets indésirables sans amélioration significative. Cet article pose une question pratique aux conséquences potentiellement vitales : peut‑on utiliser l’« empreinte » moléculaire d’une tumeur et de son tissu environnant pour noter la probabilité qu’un patient réponde à ces traitements avant même le début de la thérapie ?
Prendre le pouls du voisinage tumoral
Chaque tumeur se trouve dans un voisinage animé de cellules cancéreuses, vaisseaux sanguins, cellules immunitaires et tissus de soutien, collectivement appelés microenvironnement tumoral. Les auteurs se concentrent sur des méthodes qui convertissent cet environnement complexe en « scores » numériques en utilisant des mesures d’activité génique issues du séquençage d’ARN en masse, une technologie qui indique quelles géniques sont activées ou non dans un échantillon tumoral. Ils passent en revue et réanalysent 17 systèmes de scoring de ce type, dont beaucoup capturent différents aspects du paysage immunitaire—le nombre de lymphocytes T cytotoxiques présents, si les cellules immunitaires sont actives ou épuisées, ou l’importance du tissu stromal cicatriciel entourant la tumeur. Ces scores visent à prédire qui répondra aux inhibiteurs de points de contrôle immunitaire dans plusieurs cancers, notamment le mélanome, le poumon, la vessie, la tête et le cou, et le rein.
Comment l’étude a mis ces scores à l’épreuve
Pour comparer équitablement des méthodes développées par de nombreux groupes de recherche, les auteurs ont rassemblé des données issues de plusieurs études cliniques dans lesquelles des patients ont reçu des inhibiteurs de points de contrôle immunitaire et ont fait l’objet d’un séquençage d’ARN tumoral. Ils ont construit de grands jeux de données combinés—par exemple en fusionnant quatre études sur le mélanome et plusieurs cohortes de cancers mixtes—et ont également examiné des types de cancers individuels séparément. Parce que chaque étude utilisait des protocoles de laboratoire légèrement différents, ils ont d’abord corrigé les « effets de lot » pour que les différences techniques ne se confondent pas avec la biologie. Ils ont ensuite posé deux questions principales pour chaque score : dans quelle mesure distinguait‑il les répondeurs des non‑répondeurs, et dans quelle mesure prédisait‑il la durée de survie des patients après le traitement ?
Ce qui a fonctionné, ce qui a aidé et ce qui a déçu
L’analyse a révélé un tableau sobre mais instructif. Certains scores ont donné des résultats raisonnables dans des contextes spécifiques : par exemple, des mesures de l’activité cytolytique des lymphocytes T (appelées CYT1 et CYT2) et un score centré sur la dysfonction (TIDE) se sont montrés particulièrement informatifs dans le mélanome. Un simple ratio à deux gènes capturant le comportement des macrophages, connu sous le nom de CS Polarity, s’est distingué dans le large groupe de cancers mixtes, tandis qu’une signature génique de « tumeur chaude » nommée TIP Hot a été systématiquement utile dans plusieurs cancers, notamment la vessie, le poumon et les tumeurs de la tête et du cou. Un autre score, IS_immune, reflétant l’activité immunitaire globale, a bien prédit la survie à la fois dans le cancer de la vessie et dans l’ensemble TCGA non orienté immunothérapie. Cependant, lorsque tous les scores ont été comparés côte à côte, leur capacité à prédire la réponse ou la survie est restée généralement modeste, et aucune méthode unique n’a été de manière fiable performante dans tous les types de cancer.
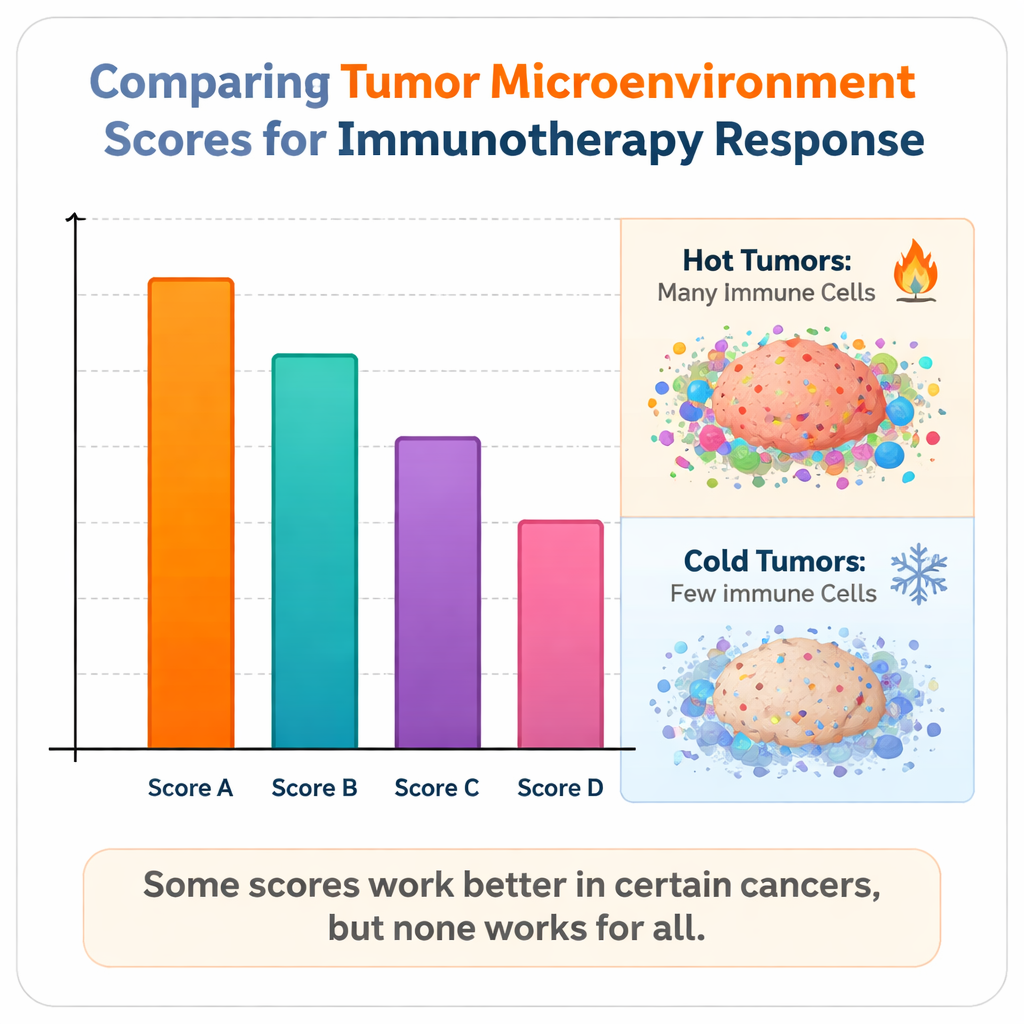
Tumeurs chaudes, tumeurs froides et limites des scores actuels
Les auteurs ont constaté que les scores avaient tendance à mieux fonctionner dans les tumeurs dites « chaudes »—celles déjà infiltrées par de nombreuses cellules immunitaires actives, comme le mélanome, certains cancers du poumon, les cancers de la tête et du cou, et les cancers urothéliaux (vessie). En revanche, dans les tumeurs « froides » comme beaucoup de cancers du rein, où les cellules immunitaires sont rares ou suppressives, tous les scores existants ont peiné. Même lorsque certaines mesures montraient des différences statistiques entre répondeurs et non‑répondeurs, leur pouvoir prédictif en conditions réelles restait faible. L’étude souligne aussi pourquoi des signatures étroites peuvent échouer : des scores bâtis autour d’un seul type cellulaire ou d’une seule voie peuvent manquer des facteurs contextuels importants, par exemple si les lymphocytes T sont épuisés ou si la tumeur a évolué pour les neutraliser. À l’inverse, des modèles extrêmement vastes et complexes risquent le surapprentissage et peuvent mal fonctionner lorsqu’on les applique à de nouveaux groupes de patients.
Ce que cela implique pour les patients et la recherche future
Pour les patients et les cliniciens, le message clé est un optimisme prudent. Les scores du microenvironnement tumoral captent déjà des signaux biologiques pertinents, et quelques‑uns—comme TIP Hot, CS Polarity, TIDE et IS_immune—montrent un potentiel dans certains cancers. Mais ils ne sont pas encore suffisamment précis ni universels pour servir de tests autonomes déterminant qui doit recevoir des inhibiteurs de points de contrôle immunitaire. Les auteurs soutiennent que les progrès futurs nécessiteront des jeux de données plus larges et plus diversifiés, des méthodes plus intelligentes pour réduire la complexité des données géniques, une meilleure intégration des facteurs cliniques et d’autres biomarqueurs (comme des analyses sanguines et des données sur le microbiome), et des modèles prenant en compte l’évolution des tumeurs dans le temps. Avec ces avancées, le scoring du microenvironnement tumoral pourrait devenir un outil puissant pour adapter l’immunothérapie au bon patient et épargner aux autres des traitements inefficaces.
Citation: Zhou, Q., Kirshtein, A. & Shahriyari, L. Towards the tumor microenvironment scoring methods for immune checkpoint inhibitor response. npj Precis. Onc. 10, 88 (2026). https://doi.org/10.1038/s41698-025-01221-z
Mots-clés: microenvironnement tumoral, réponse à l’immunothérapie, inhibiteurs des points de contrôle immunitaire, scores d’expression génique, tumeurs chaudes et froides