Clear Sky Science · fr
Déchiffrer les métastases cérébrales dans le cancer épithélial de l’ovaire : analyse multimodale et biomarqueurs potentiels
Pourquoi cette recherche est importante
Le cancer de l’ovaire est déjà une maladie dangereuse, mais chez un petit nombre de patientes il se manifeste ensuite dans un territoire beaucoup plus fragile : le cerveau. Ces métastases cérébrales sont rares mais souvent mortelles, et les médecins disposent encore de peu de moyens pour prédire qui est à risque ou comment les traiter au mieux. Cette étude suit ce trajet du pelvis au cerveau au niveau moléculaire, en utilisant des outils modernes d’analyse de l’ADN et de l’ARN pour comprendre comment les tumeurs ovariennes s’adaptent au cerveau et pour repérer des signaux d’alerte précoces susceptibles, un jour, d’orienter des soins plus personnalisés.
D’un cancer fréquent à une menace cérébrale rare
Le cancer épithélial de l’ovaire est le cancer gynécologique le plus létal dans les pays développés. La plupart des patientes répondent d’abord à la chirurgie et à la chimiothérapie, mais environ 80 % voient la maladie récidiver et devenir résistante aux médicaments. Les récidives restent généralement dans l’abdomen ; seule une petite fraction de patientes développe des métastases à distance, comme au cerveau. Cependant, à mesure que les traitements s’améliorent et que les femmes vivent plus longtemps, il y a davantage de temps pour que des cellules cancéreuses égarées colonisent le cerveau, et les cliniciens observent ces métastases plus fréquemment. Une fois que des métastases cérébrales apparaissent, la survie typique chute à moins d’un an, ce qui souligne la nécessité de comprendre comment et pourquoi cela se produit.
Une collection tissulaire rare mais précieuse
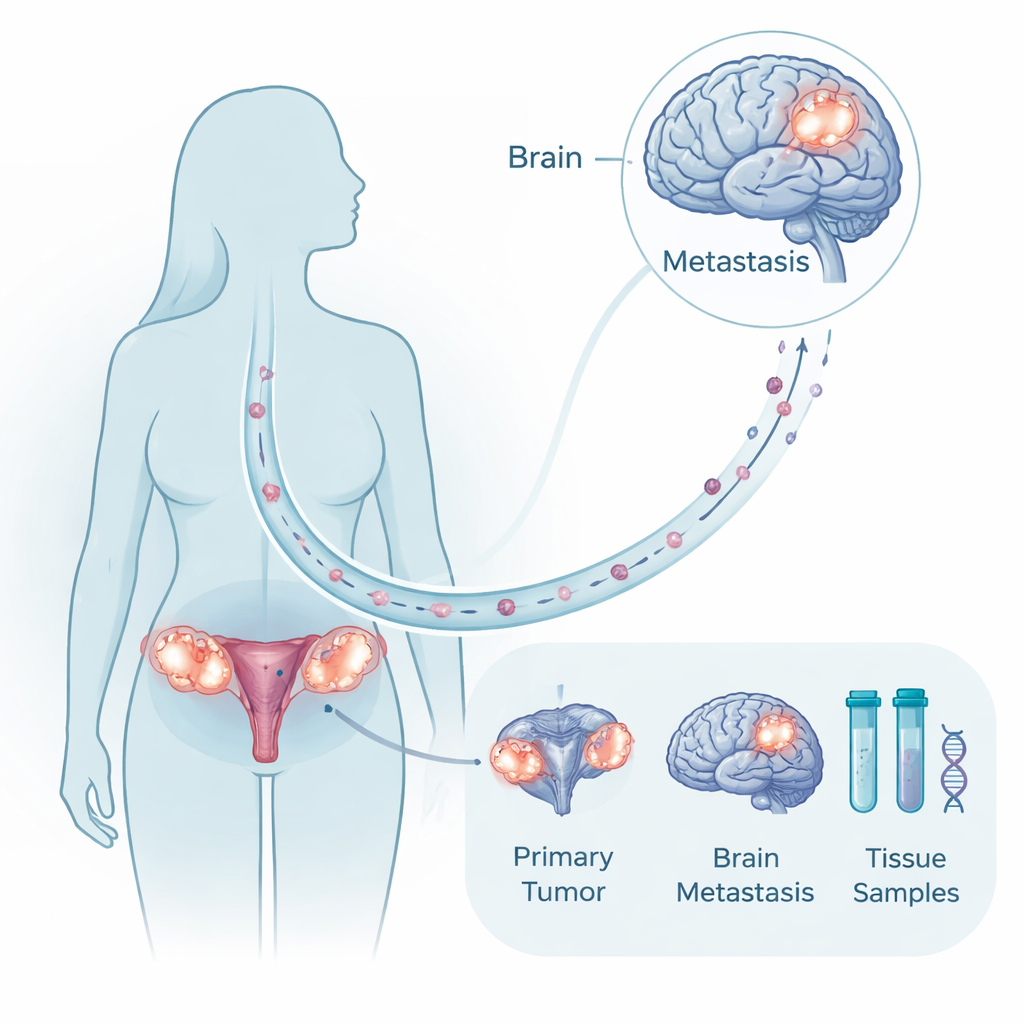
Parce que la chirurgie cérébrale n’est pas possible ou appropriée pour de nombreuses patientes, il est inhabituel de disposer d’échantillons tumoraux à la fois de la masse ovarienne initiale et de son dépôt cérébral apparié chez la même femme. Les chercheurs ont rassemblé précisément ce type de matériel apparié provenant de dix patientes traitées sur deux décennies, ainsi que des échantillons de comparaison de cerveau et d’ovaire sains et d’autres métastases non cérébrales. Ils ont analysé l’ADN tumoral pour rechercher des mutations et des altérations chromosomiques majeures, et profilé l’ARN pour voir quels gènes étaient activés ou éteints. Cette approche multimodale leur a permis de se demander si les tumeurs cérébrales sont des embranchements complètement nouveaux ou des cousins étroitement liés de la tumeur primaire, et quels programmes moléculaires changent lorsque les cellules s’implantent dans le cerveau.
Stabilité génétique, mais comportement nouveau
L’analyse de l’ADN a montré que les tumeurs ovariennes primaires et leurs métastases cérébrales appariées étaient remarquablement similaires. Les deux portaient nombre des mêmes mutations oncogènes, en particulier dans un gène appelé TP53, et partageaient une origine globalement « monoclonale », ce qui signifie que les lésions cérébrales semblaient provenir de la même cellule cancéreuse ancestrale. Les gains et pertes chromosomiques importants étaient un peu plus fréquents dans les lésions cérébrales, mais sans domination nette. Cela suggère que ce n’est pas l’acquisition d’un ensemble entièrement nouveau de mutations qui permet la dissémination au cerveau. Au lieu de cela, le changement critique apparaît au niveau de l’activité génique : quelles instructions sont lues dans l’ADN et utilisées par les cellules cancéreuses pour s’adapter à l’environnement particulier du cerveau.
Comment les tumeurs ovariennes apprennent à vivre dans le cerveau
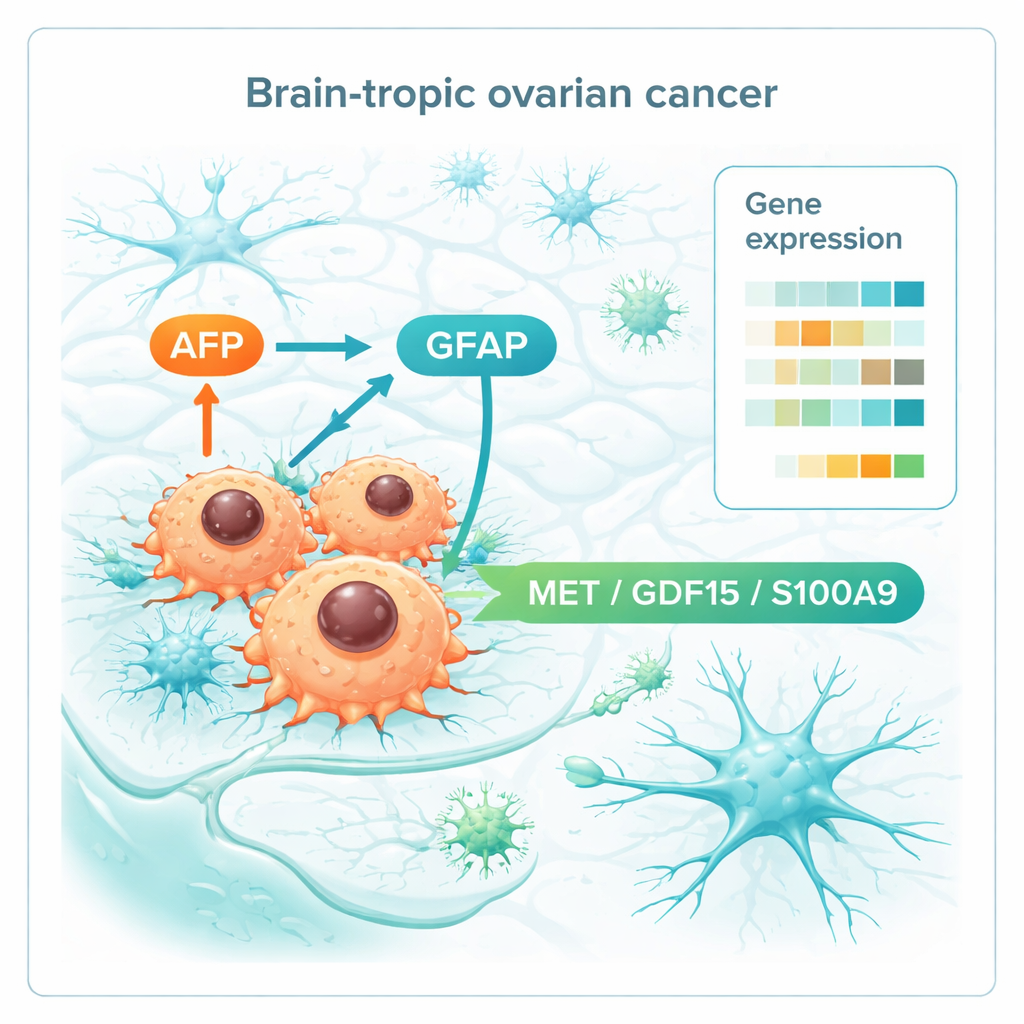
Lorsque l’équipe a comparé l’activité génique entre tous les tissus, un profil distinctif associé aux métastases cérébrales est apparu. Les lésions cérébrales présentaient des signes de croissance agressive, avec l’activation de programmes du cycle cellulaire pilotés par des régulateurs oncogéniques bien connus tels que MYC et E2F. Elles modifiaient aussi les protéines qui forment et remodèlent l’armature tissulaire, aidant les cellules à envahir et à s’ancrer dans la matière cérébrale. De manière frappante, certains gènes liés aux neurones et aux cellules gliales étaient activés, laissant entendre que les cellules du cancer ovarien imitent partiellement des cellules cérébrales pour mieux s’y intégrer. Parmi les plus remarquables figuraient AFP, habituellement active chez le fœtus et dans certains tumeurs, et GFAP, une protéine emblématique des cellules de soutien du cerveau. Les auteurs ont également identifié un petit ensemble de gènes déjà élevés dans les tumeurs ovariennes primaires des patientes qui ont ensuite développé des métastases cérébrales, mais pas chez les survivantes à long terme sans atteinte cérébrale. Ce profil « prémétastatique » impliquait une modulation immunitaire, une communication via des signaux de type nerveux et des changements métaboliques.
Signaux d’alerte précoces et échanges moléculaires
En approfondissant, les chercheurs se sont concentrés sur les molécules situées à la surface cellulaire ou sécrétées, car ce sont des candidates de choix pour des tests sanguins ou des cibles thérapeutiques. Ils ont identifié trois acteurs — MET, GDF15 et S100A9 — qui étaient systématiquement plus élevés à la fois dans les tumeurs primaires destinées au cerveau et dans les métastases cérébrales elles-mêmes. Ces molécules participent au mouvement cellulaire, à la détection du stress et du statut nutritif, et à la modulation de l’environnement immunitaire, ce qui laisse penser qu’elles aident les cellules du cancer ovarien à communiquer avec le tissu cérébral et à le remodeler à leur avantage. Avec AFP et GFAP, elles constituent une courte liste de biomarqueurs potentiels qui pourraient un jour signaler les patientes à haut risque ou indiquer des voies ciblables par des médicaments perturbant la communication tumeur–cerveau.
Ce que cela signifie pour les patientes
Pour l’instant, ce travail ne changera pas immédiatement la prise en charge, et les auteurs reconnaissent que leur cohorte est de petite taille. Néanmoins, en montrant que les cancers ovariens métastatiques au cerveau conservent une grande partie de leur constitution génétique d’origine tout en réorientant l’usage de leurs gènes, l’étude met en lumière de nouvelles façons de repérer précocement les problèmes. Si des recherches ultérieures confirment que des marqueurs tels que AFP, GFAP, MET, GDF15 et S100A9 signalent de manière fiable une tendance à se propager au cerveau, les cliniciens pourraient surveiller certaines patientes plus étroitement, adapter les choix thérapeutiques ou tester des médicaments bloquant ces voies. En substance, l’étude commence à transformer une complication tardive redoutée en un processus mesurable, compréhensible et, éventuellement, interceptable.
Citation: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
Mots-clés: cancer de l’ovaire, métastases cérébrales, biomarqueurs, expression génique, oncologie de précision